摘要:1.强碱弱酸盐的水解 [思考与交流](1) CH3COONa溶液中存在着几种离子?写出电离方程式. (2)溶液中哪些离子可能相互结合.对水的电离平衡有何影响?为什么CH3COONa溶液显碱性? (3)写出CH3COONa溶液水解的化学方程式和离子方程式.
网址:http://m.1010jiajiao.com/timu_id_3830288[举报]
(1)相同温度下,等浓度的CH3COONa和Na2CO3溶液,
(2)升高温度,使盐类的水解平衡向
(3)盐溶液的浓度越小,盐就越
(4)向CH3COONa溶液中加入NaOH溶液,则平衡向
(5)向NH4Cl溶液中加入CH3COONH4晶体,水解平衡向
查看习题详情和答案>>
Na2CO3
Na2CO3
溶液的碱性强.(2)升高温度,使盐类的水解平衡向
正反应方向
正反应方向
移动,即升高温度促进
促进
盐类的水解(填“促进”或“抑制”).(3)盐溶液的浓度越小,盐就越
容易
容易
水解,即加水促进
促进
盐类的水解(填“促进”或“抑制”).(4)向CH3COONa溶液中加入NaOH溶液,则平衡向
逆反应方向
逆反应方向
移动,即加酸能抑制
抑制
强酸弱碱盐的水解,加碱能抑制
抑制
强碱弱酸盐的水解(填“促进”或“抑制”).(5)向NH4Cl溶液中加入CH3COONH4晶体,水解平衡向
逆反应方向
逆反应方向
移动.短周期常见元素形成的纯净物A、B、C、D、E转化关系如图所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的某种相同).

请回答下列问题:
Ⅰ.若A为金属,C是离子化合物,D是一种常见的强碱.
(1)写出A的离子结构示意图
 .C的化学式
.C的化学式
(2)D与等物质的量醋酸反应所得溶液的PH
Ⅱ.若C是一种气体,D是一种强酸,则:
(3)C与水反应的化学方程式为
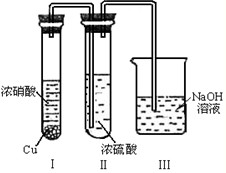
(5)有人认为“浓H2SO4可以干燥气体C”.某同学为了验证该观点是否正确,用如图装置进行实验.实验过程中,浓H2SO4中未发现有气体逸出,且变为红棕色,则你得出的解释和结论是
查看习题详情和答案>>

请回答下列问题:
Ⅰ.若A为金属,C是离子化合物,D是一种常见的强碱.
(1)写出A的离子结构示意图


Na2O2
Na2O2
.(2)D与等物质的量醋酸反应所得溶液的PH
>
>
7,(填“>”,“<”,“=”).原因是(用文字和离子方程式说明)生成的醋酸钠是强碱弱酸盐,水解呈碱性.离子方程式为CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
 CH3COOH+OH-
CH3COOH+OH-生成的醋酸钠是强碱弱酸盐,水解呈碱性.离子方程式为CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
. CH3COOH+OH-
CH3COOH+OH-Ⅱ.若C是一种气体,D是一种强酸,则:
(3)C与水反应的化学方程式为
3NO2+H2O═2HNO3+NO
3NO2+H2O═2HNO3+NO
.(5)有人认为“浓H2SO4可以干燥气体C”.某同学为了验证该观点是否正确,用如图装置进行实验.实验过程中,浓H2SO4中未发现有气体逸出,且变为红棕色,则你得出的解释和结论是
NO2能溶于浓硫酸中,浓硫酸不能干燥NO2
NO2能溶于浓硫酸中,浓硫酸不能干燥NO2
.
碘溶于碘化钾溶液中形成I3-,并建立如下平衡:I3-═I-+I2.实验室可以通过氧化还原滴定法测定平衡时I3-的浓度
实验原理:为了测定平衡时的c(I3-),可用过量的碘与碘化钾溶液一起摇动,达平衡后取上层清液用标准的Na2S2O3滴定:2Na2S2O3+I2=2NaI+Na2S4O6.由于溶液中存在I3-═I-+I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3-的总浓度,设为c1,c1=c(I2)+c(I3-);c(I2) 的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)=c2,c(I3-)=c1-c2;
实验内容:
1.用一只干燥的100mL 碘量瓶和一只250mL碘量瓶,分别标上1、2号,用量筒取80mL 0.0100mol.L-1KI于1号瓶,取200mL 蒸馏水于2号瓶,并分别加入0.5g过量的碘.
2.将两只碘量瓶塞好塞子,振荡30分钟,静置.
3.分别取上层清液20mL用浓度为c mol/L标准Na2S2O3溶液进行滴定.1号瓶消耗V1mL Na2S2O3溶液,2号瓶消耗V2mL Na2S2O3溶液.
4.带入数据计算c(I3-)
试回答下列问题
(1)标准Na2S2O3溶液应装入
(2)碘量瓶在震荡静置时要塞紧塞子,可能的原因是
(3)滴定时向待测液中加入的指示剂是
(4)用c、V1 和V2 表示c(I3-)为
mol?L-1.
(5)若在测定1号瓶时,取上层清液时不小心吸入了少量的I2固体,则测定的c(I3-)
查看习题详情和答案>>
实验原理:为了测定平衡时的c(I3-),可用过量的碘与碘化钾溶液一起摇动,达平衡后取上层清液用标准的Na2S2O3滴定:2Na2S2O3+I2=2NaI+Na2S4O6.由于溶液中存在I3-═I-+I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3-的总浓度,设为c1,c1=c(I2)+c(I3-);c(I2) 的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)=c2,c(I3-)=c1-c2;
实验内容:
1.用一只干燥的100mL 碘量瓶和一只250mL碘量瓶,分别标上1、2号,用量筒取80mL 0.0100mol.L-1KI于1号瓶,取200mL 蒸馏水于2号瓶,并分别加入0.5g过量的碘.
2.将两只碘量瓶塞好塞子,振荡30分钟,静置.
3.分别取上层清液20mL用浓度为c mol/L标准Na2S2O3溶液进行滴定.1号瓶消耗V1mL Na2S2O3溶液,2号瓶消耗V2mL Na2S2O3溶液.
4.带入数据计算c(I3-)
试回答下列问题
(1)标准Na2S2O3溶液应装入
碱式滴定管
碱式滴定管
(填“酸式滴定管”或“碱式滴定管”),原因是Na2S2O3溶液是强碱弱酸盐,水解溶液显碱性
Na2S2O3溶液是强碱弱酸盐,水解溶液显碱性
.(2)碘量瓶在震荡静置时要塞紧塞子,可能的原因是
防止I-被空气中的氧气氧化
防止I-被空气中的氧气氧化
(3)滴定时向待测液中加入的指示剂是
淀粉
淀粉
,到达滴定终点时的现象为溶液恰好由蓝色变成无色,且半分钟内不褪色
溶液恰好由蓝色变成无色,且半分钟内不褪色
.(4)用c、V1 和V2 表示c(I3-)为
| cV1-cV2 |
| 40 |
| cV1-cV2 |
| 40 |
(5)若在测定1号瓶时,取上层清液时不小心吸入了少量的I2固体,则测定的c(I3-)
偏大
偏大
(填“偏大”、“偏小”或“不变”)