摘要:3.温度.压强.浓度.催化剂等外因对化学反应速率的影响,
网址:http://m.1010jiajiao.com/timu_id_3828804[举报]
影响化学反应速率的外因主要有______________、______________、______________和______________等。
(1)浓度:在其他条件不变时,增加反应物浓度,可以____________化学反应速率;减小反应物浓度,可以____________化学反应速率。
(2)压强:对于气体反应,在其他条件不变时,增大压强,反应速率_____________;减小压强,反应速率_____________。
(3)温度:当其他条件不变时,升高温度,反应速率____________。实验测得,温度每升高10 ℃,反应速率通常增大到原来的____________倍。
(4)使用催化剂能大大____________化学反应速率。对于可逆反应,催化剂____________倍数增大正、逆反应速率。
查看习题详情和答案>>硫酸工业中2SO2(g)+O2(g)
2SO3(g);△H<0(放热反应)有关实验数据如下:
(1)在生产中常用过量的空气是为了
(2)高温对该反应有何影响?
(3)增大压强对上述反应有何影响?
(4)常用浓H2SO4而不用水吸收SO3是由于
查看习题详情和答案>>
| 催化剂 |
压强 SO2的 转化率 温度 |
1×105 Pa | 5×105 Pa | 10×105 Pa | 50×105 Pa | 100×105 Pa |
| 450℃ | 97.5% | 98.9% | 99.2% | 99.6% | 99.7% |
| 550℃ | 85.6% | 92.9% | 94.9% | 97.7% | 98.3% |
使平衡正向移动,提高SO2的转化率
使平衡正向移动,提高SO2的转化率
.(2)高温对该反应有何影响?
高温使反应速率加快,缩短了达到平衡所需的时间,但是对SO2的转化不利
高温使反应速率加快,缩短了达到平衡所需的时间,但是对SO2的转化不利
,实际生产中采用400~500℃的温度除了考虑速率因素外,还考虑到催化剂在该温度下活性最强,催化效果最佳
催化剂在该温度下活性最强,催化效果最佳
.(3)增大压强对上述反应有何影响?
加快反应速率,且使平衡正向移动,有利于SO2转化和SO3的生成
加快反应速率,且使平衡正向移动,有利于SO2转化和SO3的生成
,但工业上又常采用常压进行反应,其原因是常压时SO2的转化率已经很高,无采用高压的必要,况且,采用高压还受动力、设备等条件的限制,提高了成本
常压时SO2的转化率已经很高,无采用高压的必要,况且,采用高压还受动力、设备等条件的限制,提高了成本
.(4)常用浓H2SO4而不用水吸收SO3是由于
用水吸收SO3易形成酸雾,吸收效果差,而用浓H2SO4吸收则不易形成酸雾,吸收效果好
用水吸收SO3易形成酸雾,吸收效果差,而用浓H2SO4吸收则不易形成酸雾,吸收效果好
,尾气中SO2必须回收,主要是为了防止空气污染
防止空气污染
.影响化学反应速率的因素
内因:________.
外因
①浓度
在其他条件不变的情况下,增大反应物浓度,可以________化学反应速率;减小反应物浓度,可以________化学反应速率.
②温度
当其他条件不变时,升高温度可以________化学反应速率;降低温度可以________化学反应速率.
③反应物间的接触面积
其他条件不变时,反应物间的接触面积越大,化学反应速率________.
④催化剂
多数情况下,使用催化剂能够________化学反应速率.
⑤压强
对于有气体参加的化学反应,当其他条件不变时,增大压强可以________化学反应速率;减小压强可以________化学反应速率.
⑥光波、电磁波、超声波、溶剂等也会对化学反应速率产生影响.
影响化学反应速率的外部因素主要有
第一步 X+Y═Z
第二步 Y+Z═M+N+X
(1)此反应的总反应式为
(2)反应的中间产物是
(3)反应的催化剂是
查看习题详情和答案>>
温度
温度
、压强
压强
、浓度
浓度
和催化剂等.已知某反应在催化剂作用下按以下两步进行:第一步 X+Y═Z
第二步 Y+Z═M+N+X
(1)此反应的总反应式为
2Y=M+N
2Y=M+N
(2)反应的中间产物是
Z
Z
(3)反应的催化剂是
X
X
.A、B、C、D、E为原子序数依次增大的五种短周期元素.A、E同主族,A能与B、C、D分别形成电子数相等的三种分子,C、D最外层电子数之和与E的核外电子总数相等.
试回答:
(1)化合物ABC中σ键和π键个数比为
 .
.
(2)A、D、E 三种元素可形成一种离子化合物R,用惰性电极电解 R 的稀溶液,电解一段时间后,溶液 pH
(3)在0.1mol?L-1E2BD3的溶液中,各离子浓度由大到小的顺序是
(4)某密闭容器中发生如下反应:C2(g)+3A2(g)?2CA3(g);△H<0.如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是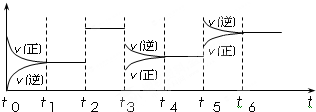
A.t5时增大了压强 B.t3时降低了温度
C.t2时加入了催化剂 D.t4~t5时间内转化率一定最低
(5)单质A的燃烧热为akJ/mol,12gB单质燃烧生成化合物BD放出热量bkJ,1mol化合物A2D由液态变为气态需吸收热量ckJ,写出单质B制水煤气的热化学方程式
查看习题详情和答案>>
试回答:
(1)化合物ABC中σ键和π键个数比为
1:1
1:1
,它属于极性
极性
分子(填“极性”或“非极性”).化合物C2A2是一种高能量分子,且C 原子满足8 电子稳定结构.写出C2A2的电子式

(2)A、D、E 三种元素可形成一种离子化合物R,用惰性电极电解 R 的稀溶液,电解一段时间后,溶液 pH
增大
增大
(填“增大”、“减小”或“不变”).(3)在0.1mol?L-1E2BD3的溶液中,各离子浓度由大到小的顺序是
c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
;分子式为 A2B2D4的化合物,与等物质的量的 KOH 溶液反应后溶液呈酸性,其原因是(用文字填空)HC2O4-的电离程度大于HC2O4-的水解程度
HC2O4-的电离程度大于HC2O4-的水解程度
.(4)某密闭容器中发生如下反应:C2(g)+3A2(g)?2CA3(g);△H<0.如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是
C
C

A.t5时增大了压强 B.t3时降低了温度
C.t2时加入了催化剂 D.t4~t5时间内转化率一定最低
(5)单质A的燃烧热为akJ/mol,12gB单质燃烧生成化合物BD放出热量bkJ,1mol化合物A2D由液态变为气态需吸收热量ckJ,写出单质B制水煤气的热化学方程式
C(s)+H2O(g)=CO(g)+H2(g)△H=(a-b-c)kJ/mol
C(s)+H2O(g)=CO(g)+H2(g)△H=(a-b-c)kJ/mol
.