摘要:1.[江苏省启东中学2009届高三第一学期第二次月考 ]红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料.在印染工业.电镀工业和皮革工业中作助剂.在化学工业和制药工业中也用作氧化剂.应用领域十分广泛. (1) 实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取. ①步骤I中反应的化学方程式为: 4FeO·Cr2O3(s)+8Na2CO3(s)+7O2 8Na2CrO4(s)+2Fe2O3(s)+8CO2,△H<0 该反应的化学平衡常数的表达式为 . ②图1.图2表示该反应在t1时达到平衡.在t2时因改变某个条件而发生变化的曲线: 由图1判断.反应进行至t2 min时.曲线发生变化的原因是 .由图2判断.t2 min到t3 min 的曲线变化的原因可能是 w.w.w.k.s.5.u. c.o.m a.升高温度 b.加了催化剂 c.将原料粉碎 d.缩小容器体积 (2)步骤Ⅱ中所得溶液显碱性.其中除含有Na2CrO4外还含有铝.硅元素的化合物.它们的化学式可能是 . . ①步骤Ⅲ需将溶液的pH调至7~8并煮沸.其目的是 . ②步骤Ⅳ中发生反应的离子方程式为: . 答案..(1)①②t2 时对平衡体系降温 (2)NaA1O2[或NaA1(OH)4].Na2SiO3(各1分.共2分,如写A1O2-.SiO32-给1分) ①除去A1O2-.SiO32-等杂质 ②2CrO42-+2H+=Cr2O72-+H2O
网址:http://m.1010jiajiao.com/timu_id_3825243[举报]
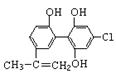
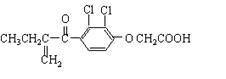
 A.利尿酸分子中有三种含氧官能团,在核磁共振氢谱上共有六个峰
A.利尿酸分子中有三种含氧官能团,在核磁共振氢谱上共有六个峰