网址:http://m.1010jiajiao.com/timu_id_3815245[举报]
A、B、C、D为中学化学中常见的四种气体单质.
(1)已知在空气中A约占21%、C约占78%(均为体积分数);D在标准状况下的密度为3.170 g·L-1.分别写出A、C、D的化学式:A________、C________、D________.SO2通入D的水溶液中,可以发生氧化还原反应,其化学方程式为:________.
(2)在一定条件下B与A、C、D化合分别生成甲、乙、丙.已知甲、乙分子中含有的电子数均与Na+相同;乙与丙可化合生成一种离子化合物.
甲、乙的化学式是:甲________、乙________;丙的电子式是:________.
(3)乙可以发生如下图所示一系列转化(无关物质及反应条件已略去):
单质A与化合物乙反应的化学方程式为________.
Z的稀溶液与过量铁粉反应,当反应中有1.806×1023个电子转移时,被还原的Z物质的量是________mol.
(4)将B、C按体积比为3∶1混合分别装入盛有催化剂的密闭容器Ⅰ和Ⅱ中(容积相同),若反应过程中容器Ⅰ保持温度和压强不变,容器Ⅱ保持温度和容积不变,当反应达平衡时,容器Ⅰ内气体的密度________容器Ⅱ内气体的密度(填“大小”“小于”或“等于”),理由是________.在容器Ⅰ中,当反应达平衡时容积变为起始时的![]() ,则C的转化率为________.
,则C的转化率为________.
| |||||||||||||||||||
A、B、C、D为中学化学中常见的四种气体单质.
(1)已知在空气中A约占21%、C约占78%(均为体积分数);D在标准状况下的密度为3.170 g/L.
分别写出A、C、D的化学式:A________、C________、D________.
SO2通入D的水溶液中,可以发生氧化还原反应,其化学方程式为:
___________________________________
(2)在一定条件下B与A、C、D化合分别生成甲、乙、丙.已知甲、乙分子中含有的电子数均与Na+相同;乙与丙可化合生成一种离子化合物.
甲、乙的化学式是:甲________、乙________;丙的电子式是:________.
(3)乙可以发生如图所示一系列转化(无关物质及反应条件已略)
单质A与化合物乙反应的化学方程式________.
Z的稀溶液与过量铁粉反应,当反应中有1.806×1024个电子转移时,被还原的Z物质的量是________mol.
(4)将B、C按体积比为3∶1混合分别装入盛有催化剂的密闭容器Ⅰ和Ⅱ中(容积相同),若反应过程中容器Ⅰ保持温度和压强不变,容器Ⅱ保持温度和容积不变,当反应达平衡时,容器Ⅰ内气体的密度________容器Ⅱ内气体的密度(填“大于”“小于”或“等于”),理由是________.
在容器Ⅰ中,当反应达平衡时容积变为起始时的![]() ,则C的转化率为________.
,则C的转化率为________.
Ⅰ.通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。下表为一些化学键的键能数据
| 化学键 | Si-Si | O=O | Si-O |
| 键能/kJ·mol-1 | a | b | c |
写出硅高温燃烧的热化学方程式 。
Ⅱ.利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如右图所示的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用。写出下列电解池中总反应的离子方程式:
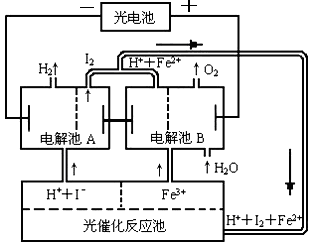
电解池A 。
电解池B 。
(2)若电解池A中生成3.36 L H2(标准状况),计算电解池B中生成Fe2+的物质的量为 mol。
Ⅲ.在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g)
 2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。
2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。
请据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别表示加入的N2、H2 和NH3的体积,如果反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同。
①a=1,c=2,则b= 。在此情况下,反应起始时将向 反应方向(填“正”或“逆”)进行。
②若需规定起始时反应向逆方向进行,则c的取值范围是 。
(2)在上述恒压装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是 ,原因是 。 查看习题详情和答案>>
(1) NO2可用水吸收,相应的化学反应方程式为__________________,
利用反应6NO2+8NH3
 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是_____________L。
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是_____________L。(2)已知:2SO2(g)+O2(g)
 2SO3(g) △H=-196.6kJ·mol-1
2SO3(g) △H=-196.6kJ·mol-12NO(g)+O2(g) = 2NO2(g) △H=-113.0 kJ·mol-1
则反应SO2(g)+NO2(g) = SO3(g)+ NO(g)的△H=________ kJ·mol-1 一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________。
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO2和NO的体积比保持不变
D.每消耗1molSO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=________。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)
 CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H___0(填“>”或“<”)实际生产条件控制在250℃、1.3ⅹ104 kPa左右,选择此压强的理由是_______。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H___0(填“>”或“<”)实际生产条件控制在250℃、1.3ⅹ104 kPa左右,选择此压强的理由是_______。 