网址:http://m.1010jiajiao.com/timu_id_3815244[举报]
(1)水煤气生产原理为:C(s)+H2O(g)
| 高温 |
①该反应自发可能性
②一定温度下,在一个容积不变的密闭容器中进行水煤气生产反应,下列能判断该反应达到化学平衡状态的是
A.容器内压强不变 B.容器内气体密度不变
C.v(CO)正=v(H2O)逆 D.c(CO)=c(H2)
③下列措施能使C(s)+H2O(g)
| 高温 |
A、增加C(s)的量 B、降温 C、升温 D、充入HI
(2)将不同量CO(g)和H2O(g)分别通入到体积为2L的恒容容器中,进行反应
CO(g)+H2O(g)
| 高温 |
| 实验 组别 |
温度℃ | 起始量/mol | 平衡/mol | 达平衡所 需时间/min | ||||
| H2O | CO | H2 | CO2 | H2 | CO2 | |||
| 1 | 650 | 2 | 4 | 0 | a | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0 | b | 0.4 | 1.6 | 3 |
②900℃时,CO2(g)+H2(g)
| 高温 |
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率,为了分别验证温度,催化剂比表面积对化学反应速率的影响规律,至少应该设计
| 组别 | 温度 | 催化剂 | … |
| 1 | |||
| 2 | |||
(1)水煤气生产原理为:C(s)+H2O(g)
 CO(g)+H2(g);△H=+131.3kJ/mol
CO(g)+H2(g);△H=+131.3kJ/mol①该反应自发可能性______(填有或无);
②一定温度下,在一个容积不变的密闭容器中进行水煤气生产反应,下列能判断该反应达到化学平衡状态的是______(填字母);
A.容器内压强不变 B.容器内气体密度不变
C.v(CO)正=v(H2O)逆 D.c(CO)=c(H2)
③下列措施能使C(s)+H2O(g)
 CO(g)+H2(g)正反应速率增大的是_______;
CO(g)+H2(g)正反应速率增大的是_______;A、增加C(s)的量 B、降温 C、升温 D、充入HI
(2)将不同量CO(g)和H2O(g)分别通入到体积为2L的恒容容器中,进行反应
CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:| 实验 组别 | 温度℃ | 起始量/mol | 平衡/mol | 达平衡所 需时间/min | ||||
| H2O | CO | H2 | CO2 | H2 | CO2 | |||
| 1 | 650 | 2 | 4 | a | 1.6 | 2.4 | 5 | |
| 2 | 900 | 1 | 2 | b | 0.4 | 1.6 | 3 | |
②900℃时,CO2(g)+H2(g)
 CO(g)+H2O(g)化学平衡常数为______;
CO(g)+H2O(g)化学平衡常数为______;(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率,为了分别验证温度,催化剂比表面积对化学反应速率的影响规律,至少应该设计______组实验.
| 组别 | 温度 | 催化剂 | … |
| 1 | |||
| 2 | |||
查看习题详情和答案>>
 CO(g) + H2O(g) 其平衡常数K和温度t的关系如下
CO(g) + H2O(g) 其平衡常数K和温度t的关系如下
(2)该反应的正反应为______________反应(“吸热”或“放热”);
(3)能判断该反应是否已经达到化学平衡状态的是:_______________
A.容器中压强不变
B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆
D.c(CO2) = c(CO)
(4)在850℃时,可逆反应:CO2(g) + H2(g)
 CO(g) + H2O(g),在该容器内各物质的浓度变化如下
CO(g) + H2O(g),在该容器内各物质的浓度变化如下
Ⅱ.二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用。工业上以CO和H2为原料生产CH3OCH3的新工艺主要发生三个反应

(5)新工艺的总反应为:3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g) ΔH 该反应ΔH=______________。
CH3OCH3(g)+CO2(g) ΔH 该反应ΔH=______________。 (6)增大压强,CH3OCH3的产率____________(填“增大”、“减小”或“不变”)。
(7)原工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生。新工艺中反应③的发生提高了CH3OCH3的产率,原因是_________________________。
(8)为了寻找合适的反应温度,研究者进行了一系列实验,每次实验保持原料气组成、压强、反应时间等因素不变,试验结果如下图CO转化率随温度变化的规律是_________________________________,原因是_________________________。

(I某氮肥厂氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。在微生物作用下,NH4+经过两步反应被氧化成NO3-,两步反应的能量变化示意图如下:
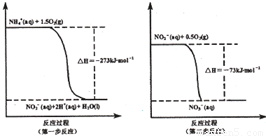
(1)1 mo1NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是 _ 。
(2)在一定条件下,向废水中加入CH3OH,将HNO3还原成 N2,若该反应消耗32gCH3OH转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是_ 。
(B)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术
将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO十2CO 2CO2+ N2 △H
2CO2+ N2 △H
某温度下用气体传感器测得不同的时间的NO和CO浓度如下表:
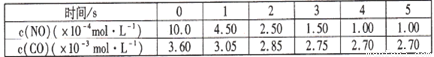
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“=”)
(2)在该温度下,反应的平衡常数K= (只写出计算结果);
(3)某同学设计了三组实验,分别验证温度、催化剂比表面积对化学反应速率的影响规律,
部分实验条件如下表:

该同学画出了表中三个实验条件下,混合气体中NO浓度随时间变化的趋势曲线图,请在图上标明各条曲线的实验编号;
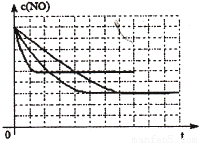
查看习题详情和答案>>
(I某氮肥厂氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。在微生物作用下,NH4+经过两步反应被氧化成NO3-,两步反应的能量变化示意图如下: 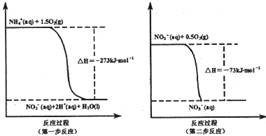
(1)1 mo1NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是 _ 。
(2)在一定条件下,向废水中加入CH3OH,将HNO3还原成 N2,若该反应消耗32gCH3OH转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是_ 。
(B)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术
将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO十2CO 2CO2+ N2 △H
2CO2+ N2 △H
某温度下用气体传感器测得不同的时间的NO和CO浓度如下表: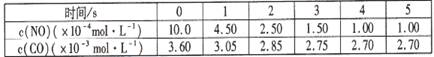
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“=”)
(2)在该温度下,反应的平衡常数K= (只写出计算结果);
(3)某同学设计了三组实验,分别验证温度、催化剂比表面积对化学反应速率的影响规律,
部分实验条件如下表:
该同学画出了表中三个实验条件下,混合气体中NO浓度随时间变化的趋势曲线图,请在图上标明各条曲线的实验编号;