摘要:2.1可逆反应与化学平衡
网址:http://m.1010jiajiao.com/timu_id_3815239[举报]
可逆反应N2+3H2 2NH3是工业上合成氨的重要反应.
2NH3是工业上合成氨的重要反应.

(1)根据图1请写出合成氨的热化学方程式
(2)图1中虚线部分是通过改变化学反应中的
(3)当反应达到平衡位置时不断改变条件(不改变N2、H2和NH3的量),图2表示反应速率与反应过程的关系,其中表示平衡混合物中NH3的含量最高的一段时间是
(4)在一定温度下,若将4a mol H2和2amol N2放入2L的密闭容器中,充分反应后测得N2的转化率为50%,则该反应的平衡常数为
.若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是
(5)将上述实验中产生的NH3通入到0.04mol?L-1的FeCl3溶液中,要使溶液中Fe3+沉淀较完全(即Fe3+浓度降至原来的千分之一),则溶液的pH为
查看习题详情和答案>>
 2NH3是工业上合成氨的重要反应.
2NH3是工业上合成氨的重要反应.
(1)根据图1请写出合成氨的热化学方程式
N2(g)+3H2(g) 2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol
2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol
 2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol
2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/molN2(g)+3H2(g) 2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol
2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol
(热量用E1、E2或E3表示) 2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol
2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol(2)图1中虚线部分是通过改变化学反应中的
催化剂
催化剂
条件,请解释原因因为催化剂能改变反应的路径,使发生反应所需的活化能降低
因为催化剂能改变反应的路径,使发生反应所需的活化能降低
.(3)当反应达到平衡位置时不断改变条件(不改变N2、H2和NH3的量),图2表示反应速率与反应过程的关系,其中表示平衡混合物中NH3的含量最高的一段时间是
t0-t1
t0-t1
(4)在一定温度下,若将4a mol H2和2amol N2放入2L的密闭容器中,充分反应后测得N2的转化率为50%,则该反应的平衡常数为
| 16 |
| a2 |
| 16 |
| a2 |
正向移动
正向移动
(“正向移动”“逆向移动”或“不移动”)(5)将上述实验中产生的NH3通入到0.04mol?L-1的FeCl3溶液中,要使溶液中Fe3+沉淀较完全(即Fe3+浓度降至原来的千分之一),则溶液的pH为
3
3
(已知常温下,Fe(OH)3的溶度积常数Ksp=4×10-38)化学平衡原理在工农业生产中发挥着重要的指导作用.
(1)反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
(2)已知某温度下,反应2SO2(g)+O2 (g)?2SO3(g),的平衡常数K=19,在该温度下的体积固定的密闭容器中充入C(SO2)=1mol?L-1,C(O2)=1mol?L-1,当反应在该温度下SO2转化率为80%时,该反应
(3)对于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H=a kJ?mol-1;若a+b>c+d,增大压强平衡向
查看习题详情和答案>>
(1)反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
=
| c2(CO) |
| c(CO2) |
=
;已知C(s)+H2O(g)?CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)?CO(g)+H2O(g)的平衡常数为K2,则K与K1、K2二者的关系为| c2(CO) |
| c(CO2) |
K=K1×K2
K=K1×K2
.(2)已知某温度下,反应2SO2(g)+O2 (g)?2SO3(g),的平衡常数K=19,在该温度下的体积固定的密闭容器中充入C(SO2)=1mol?L-1,C(O2)=1mol?L-1,当反应在该温度下SO2转化率为80%时,该反应
否
否
(填“是”或“否”)达到化学平衡状态,若未达到,向逆反应
逆反应
(填“正反应”或“逆反应”) 方向进行.(3)对于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H=a kJ?mol-1;若a+b>c+d,增大压强平衡向
正反应
正反应
(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则a<
<
0(填“>”或“<”) 可逆反应A+B?2C,在不同温度下经过一定的时间,混合物C的体积分数与温度的关系如图所示:
可逆反应A+B?2C,在不同温度下经过一定的时间,混合物C的体积分数与温度的关系如图所示:(1)反应在
T3
T3
时达到化学平衡.(2)此反应的正反应为
放
放
热反应.(3)由T1向T2变化时,v(正)
>
>
v(逆)(填“>”、“<”或“=”).可逆反应:mA(s)+nB(g)?eC(g)+fD(g),在反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图1图2所示.下列叙述正确的是( )
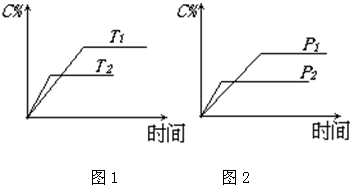

| A、达到平衡后,若升高温度,平衡向逆反应方向移 | B、达到平衡后,增加A的量有利于平衡向正反应方向移动 | C、达到平衡后,加入催化剂则C%增大 | D、化学方程式中n>e+f |
可逆反应N2+3H2![]() 2NH3是工业上合成氨的重要反应。
2NH3是工业上合成氨的重要反应。

(1)根据图1请写出合成氨的热化学方程式 (热量用E1、E2或E3表示)
(2)图1中虚线部分是通过改变化学反应中的 条件,请解释原因
。
(3)当反应达到平衡位置时不断改变条件(不改变N2、H2和NH3的量),图2表示反应速率与反应过程的关系,其中表示平衡混合物中NH3的含量最高的一段时间是
(4)在一定温度下,若将4a mol H2和2amol N2放入2L的密闭容器中,充分反应后测得N2的转化率为50%,则该反应的平衡常数为 。若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是 (“正向移动”“ 逆向移动”或“不移动”)
(5)将上述实验中产生的NH3通入到0.04mol·L-1的FeCl3溶液中,要使溶液中Fe3+沉淀较完全(即Fe3+浓度降至原来的千分之一),则溶液的pH为 (已知常温下,Fe(OH)3的溶度积常数Ksp=4×10-38)
查看习题详情和答案>>