摘要:4.为表示一个原子在第三电子层上有10个电子.可以写成 A.310 B.3d10 C.3s23p63d2 D.3s23p64s2
网址:http://m.1010jiajiao.com/timu_id_3794957[举报]
(1)X原子在第二电子层上只有一个空轨道,则X是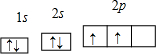
 ;R原子的3p轨道上只有一个未成对电子,则R原子可能是
;R原子的3p轨道上只有一个未成对电子,则R原子可能是
(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:
(3)下列分子中若有手性原子,请用“*”标出其手性碳原子.
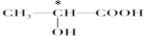
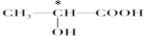
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
(6)根据价层电子对互斥理论判断下列问题:
H2O中心原子的杂化方式为
BF3分子中,中心原子的杂化方式为
(7)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
查看习题详情和答案>>
C
C
;其轨道表示式为

Al
Al
、Cl
Cl
;Y原子的核电荷数为29,其电子排布式是1s22s22p63s23p63d104s1
1s22s22p63s23p63d104s1
,其在元素周期表中的位置是第四周期第ⅠB族
第四周期第ⅠB族
,是属于ds
ds
区的元素.(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:
Co3+
Co3+
、CN-
CN-
、6
6
.(3)下列分子中若有手性原子,请用“*”标出其手性碳原子.

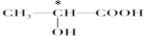
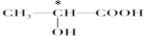
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)
①③④⑦
①③④⑦
.(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
>
>
H2SO3; H3PO4>
>
H3PO3.(6)根据价层电子对互斥理论判断下列问题:
H2O中心原子的杂化方式为
sp3
sp3
杂化,分子的立体构型为V形
V形
.BF3分子中,中心原子的杂化方式为
sp2
sp2
杂化,分子的立体构型为平面正三角形
平面正三角形
.(7)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
水分子之间存在氢键
水分子之间存在氢键
.(1)X原子在第二电子层上只有一个空轨道,则X是
 ;R原子的3p轨道上只有一个未成对电子,则R原子可能是
;R原子的3p轨道上只有一个未成对电子,则R原子可能是
(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:
(3)下列分子中若有手性原子,请用“*”标出其手性碳原子.
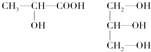
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
(6)根据价层电子对互斥理论判断下列问题:
H2O中心原子的杂化方式为
BF3分子中,中心原子的杂化方式为
(7)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
查看习题详情和答案>>
C
C
;其轨道表示式为

Al
Al
、Cl
Cl
;Y原子的核电荷数为29,其电子排布式是1s22s22p63s23p63d104s1
1s22s22p63s23p63d104s1
,其在元素周期表中的位置是第四周期第IB族
第四周期第IB族
,是属于ds
ds
区的元素.(2)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:
Co3+
Co3+
、CN-
CN-
、6
6
.(3)下列分子中若有手性原子,请用“*”标出其手性碳原子.
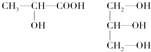
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)
①③④⑦
①③④⑦
.(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
>
>
H2SO3; H3PO4>
>
H3PO3.(6)根据价层电子对互斥理论判断下列问题:
H2O中心原子的杂化方式为
sp3
sp3
杂化,分子的立体构型为V形
V形
.BF3分子中,中心原子的杂化方式为
sp2
sp2
杂化,分子的立体构型为平面正三角形
平面正三角形
.(7)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
水分子之间存在氢键
水分子之间存在氢键
.原子序数依次增加的A、B、C、D、E、F六种常见元素中,A、B、C、D是短周期非金属元素,B、C、D同周期,E、F是第四周期的金属元素,F+的三个能层电子全充满。下表是主要化合价及原子半径数据: -ks5u
| A | B | C | D | E | F | |
| 主要化合价 | -1 | -3 +5 | -2 +6 | -1 +7 | +2 | +1 +2 |
| 原子半径 | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |
(1)B、C、D三种元素第一电离能数值由小到大的顺序是 (填元素符号);
(2)B的氢化物中心原子采取 杂化,空间构型是 形,是 分子(填“极性”或“非极性”);
(3)F2+与NH3 形成配离子的结构式为 ;往某种蓝色溶液中加入氨水,形成蓝色沉淀,继续加入氨水,难溶物溶解变成蓝色透明溶液,可得到含有上述配离子的配合物。写出沉淀溶解的离子方程式 。
(4)A 、E两种元素形成晶体晶胞是下图中的 (填①、②、③或④);
 |
① ② ③ ④
 (5)右图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,请选出C的氢化物所在的折线 (填n、m、x或y)。
(5)右图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,请选出C的氢化物所在的折线 (填n、m、x或y)。