摘要:19.短周期常见元素形成的单质或化合物A.B.C.D.E转化关系如图所示: 物质A与物质B之间的反应不在溶液中进行.E可能与A.B两种物质中的某种相同. 请回答下列有关问题: (1)若C是离子化合物.D是一种强碱.则C物质的电子式为 , (2)若C与水发生复分解反应.E的水溶液呈弱酸性.D既能与强酸反应又能与强碱反应. ①D与NaOH溶液反应的离子方程式为 , ②E与NaOH反应后的溶液中.所有离子浓度之间的关系为 . (3)若C是一种气体.D是一种强酸. ①A与B反应的化学方程式为 . ②组成D的各元素的原子半径由大到小的顺序为 . 解析:(1)C与水反应能形成强碱且生成气体.C应为Na2O2.E为O2.D为NaOH. (2)根据题意.D为两性化合物.为Al(OH)3.E的水溶液显弱酸性.得:C应该是Al2S3.E是H2S.当H2S与NaOH按1?2反应时.应该得到Na2S.由电荷守恒得c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-). (3)C与H2O生成一种强酸和一种气体.C应为NO2.E为NO.化合物D为HNO3. 答案:(1)Na+[?····?····?]2-Na+ 3+OH-===[Al(OH)4]- c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-) (3)①2NO+O2===2NO2 ②N>O>H或N.O.H20.如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去). 已知: (a)A.B.C.D是非金属单质.其中B.C.D在常温常压下是气体. (b)反应①.②是化工生产中的重要反应. (c)化合物E是形成酸雨的污染物之一.化合物K是常用的氮肥. (d)化合物L具有漂白性.可由Cl2与NaOH溶液反应而制得. (e)化合物J由两种元素组成.其相对分子质量为32. 请按要求填空: (1)反应③的化学方程式 . (2)C的结构式 ,H的化学式 . (3)L的溶液与化合物E反应的离子方程式: . (4)化合物J的化学式 . 解析:本题的突破口是E.由于B.C.D是非金属单质.且其中A不是气体.结合“化合物E是形成酸雨的污染物之一 不难推出E为SO2.A为S.B为O2,再根据“反应②是化工生产中的重要反应 及“FK .且“K是常用的氮肥 可推出F为NH3.则C.D为N2.H2,再结合“JC 和“J由两种元素组成.其相对分子质量为32 .可推出C只能为N2.J为N2H4,又根据“L具有漂白性.可由Cl2与NaOH溶液反应而制得“可推出L为NaClO. 答案:(1)2NH3+H2SO4===(NH4)2SO4 (2)N≡N (NH4)2SO3或NH4HSO3 (3)ClO-+SO2+2OH-===Cl-+SO+H2O (4)N2H4
网址:http://m.1010jiajiao.com/timu_id_3793731[举报]
2008年9月25日21时10分,“神舟七号”顺利升空,并实施首次空间出舱活动.飞船的太阳能电池板有“飞船血液”之称,我国在砷化镓太阳能电池研究方面处于国际领先水平,下列有关说法正确的是( )
查看习题详情和答案>>
(2009?乐平市模拟)2008年9月25日21时10分,“神七”顺利升空.飞船的太阳能电池板有“飞船血液”之称,它可将太阳能直接转化为电能,我国在砷化镓太阳能电池研究方面国际领先.砷(As)和镓(Ga)都是第四周期元素,分别属于ⅤA和ⅢA族.下列有关说法正确的是( )
查看习题详情和答案>>
北京时间2008年9月25日21时10分04秒,我国自行研制的神州七号载人飞船在酒泉卫星发射中心发射升空.担任神七飞船发射任务的长征二号F运载火箭.火箭推进剂是偏二甲肼{分子式:C2H8N2}与四氧化二氮.
(1)6.0g液态偏二甲肼与足量的液态四氧化二化氮完全反应生成N2(g)、CO2(g)、H2O(g)、放出225.0kJ的热量.
①写出上述反应的热化学方程式: .
②下列判断正确的是
A、物质的燃烧反应必须有氧气参加
B、该反应中氧化剂与还原剂物质的量之比为2:1
C、偏二甲肼燃烧热为2250kJ/mol
D、偏二甲肼与四氧化二氮作火箭推进剂是二者发生剧烈的氧化还原反放出大量的热和产生大量气体的原因
(2)使用偏二甲肼与四氧化二氮作燃料,使发射场产生棕黄色“蘑菇”云弥漫,损害工作人员的身体健康,带来一些后遗症.产生棕黄色“蘑菇”云的可能原因 .
(3)新的环保低温燃料计划在2014年到2016年使用,将在海南发射场发射中等推力火箭的时候采用,新的低温燃料是液氢.利用核能把水分解,制取氢气,是目前许多国家正在研究的课题.下图是国外正在研究的一种流程(硫-碘热循环法),其中用了过量的碘.
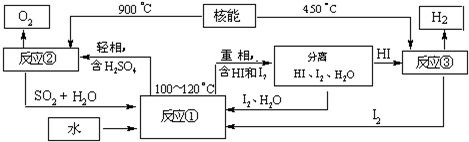
写出①反应的化学方程式 ;
用硫-碘热循环法制取氢最大的优点是 .
查看习题详情和答案>>
(1)6.0g液态偏二甲肼与足量的液态四氧化二化氮完全反应生成N2(g)、CO2(g)、H2O(g)、放出225.0kJ的热量.
①写出上述反应的热化学方程式:
②下列判断正确的是
A、物质的燃烧反应必须有氧气参加
B、该反应中氧化剂与还原剂物质的量之比为2:1
C、偏二甲肼燃烧热为2250kJ/mol
D、偏二甲肼与四氧化二氮作火箭推进剂是二者发生剧烈的氧化还原反放出大量的热和产生大量气体的原因
(2)使用偏二甲肼与四氧化二氮作燃料,使发射场产生棕黄色“蘑菇”云弥漫,损害工作人员的身体健康,带来一些后遗症.产生棕黄色“蘑菇”云的可能原因
(3)新的环保低温燃料计划在2014年到2016年使用,将在海南发射场发射中等推力火箭的时候采用,新的低温燃料是液氢.利用核能把水分解,制取氢气,是目前许多国家正在研究的课题.下图是国外正在研究的一种流程(硫-碘热循环法),其中用了过量的碘.

写出①反应的化学方程式
用硫-碘热循环法制取氢最大的优点是
2008年9月25日21时10分,“神舟七号”顺利升空,并实施我国首次空间出舱活动.飞船的太阳能电池板有“飞船血液”之称,我国在砷化镓太阳能电池研究方面国际领先.下列有关说法正确的是( )
查看习题详情和答案>>
(10分) 在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是 ;X与氢元素形成的化合物的电子式是 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是 ;D与E能形成一种非极性分子,该分子的结构式为 ;D所在族元素的氢化物中,沸点最低的氢化物的化学式是 。
(3)元素W与Y同周期,其单质是一种良好的半导体材料;元素Z的单质分子Z2中由3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是 。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,此反应的离子方程式 。
查看习题详情和答案>>