网址:http://m.1010jiajiao.com/timu_id_3792388[举报]
(12分)有A、B、C、D四种元素,A元素形成的-2价阴离子比氦原子的核外电子数多8个,B 元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质,C为原子核内有12个中子的二价金属,当2 .4克C与足量热水反应时,在标准状况下放出气体2.24L,D的M层上7个电子。(①②③每空1分)
①写出A~D元素符号:A____,B_____,C_____,D_____
②写出A的原子结构示意图: B的离子结构示意图::
D在周期表的位置: C和D所形成的化合物的电子式
③分别写出B 、D的最高价氧化物的水化物的化学式______ ,______
④比较D的气态氢化物与H2S和HF的稳定性:(2分)
查看习题详情和答案>>
((2)题每空3分,其余每空2分,共12分)A、B、C、D均为中学化学常见的物质,它们之间的反应关系如下图:

回答下列问题:
(1)若A是可溶性的强碱,B是酸式盐,D不溶于稀硝酸,则B的化学式为________________,有关的离子方程式为___________________________________ 。
(2)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液。
① 若C为能使澄清石灰水变浑浊的无色无味气体,该反应的离子方程式为
____________________________________________________ 。
②若A是一种淡黄色固体,且A与B以物质的量之比3∶1混合时,推知B的化学式为
_________ _。
(3)若B为Ca(HCO3)2溶液,A与B的溶液反应时只生成气体C、CaCO3和水,则A的化学式为__________________ 。
查看习题详情和答案>>
(每空3分,共12分) A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。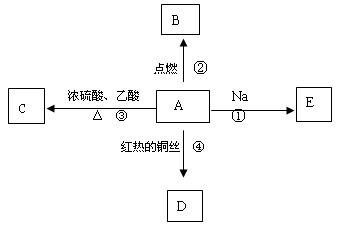
(1)写出A的结构式
(2)写出下列反应的化学方程式(有机物用结构简式表示):
反应①:
反应②:
反应④:
.(12分) 现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产
生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
|
阴离子 |
OH-、C1-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性,C、D、E溶液呈酸性;常温下,0.1 mol/L
B溶液的pH大于13,0.1 mol/L C溶液的pH等于1
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有
气体产生;(沉淀包括难溶物和微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)写出A、B、C、D、E的化学式:A、 B、
C、 D、 E
(2)写出A、E溶液反应的离子方程式:
。
(3)写出B溶液与C溶液恰好完全反应的离子方程式:
_____ 。
(4)将C溶液逐滴加入等体积、等物质量的浓度的A溶液中,反应后溶液中各种离子浓度由小到大的顺序为(带两个单位电荷的离子不参与比较):__________________________________。
查看习题详情和答案>>
(12分) 有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子:(每种物质只含一种阳离子和一种阴离子且互不重复)
| 阳离子 | Na+、Ba2+、NH4+、K+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
已知:①A、C溶液的pH均大于7,B溶液的pH小于7,A、B溶液中水的电离程度相同;D溶液焰色反应显黄色。
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成有刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A的名称是____________。
(2)用离子方程式表示A的水溶液显碱性的原因______________________________。
(3)25 ℃时pH=9的A溶液和pH=9的C溶液中水的电离程度较小的是________(填写A或C的化学式)。
(4)25 ℃时用惰性电极电解D的水溶液,一段时间后溶液的pH________7(填“>”、“<”或“=”)。
(5)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为__________________________________________________。
(6)室温时在一定体积0.2 mol·L-1的C溶液中,加入一定体积的0.1 mol·L-1的盐酸时,混合溶液的pH=13,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是________。 查看习题详情和答案>>