摘要:(1)下列装置能否组成原电池?并判断正负极.
网址:http://m.1010jiajiao.com/timu_id_3783232[举报]
 某化学研究性学习小组进行了一系列“带火星的木炭复燃”的实验,实验装置如右图所示.
某化学研究性学习小组进行了一系列“带火星的木炭复燃”的实验,实验装置如右图所示.(1)甲组同学探究“使带火星木炭复燃时O2的体积分数的极限”.将氧气和空气(假定空气中O2的体积分数为20%)按不同的体积比混合得100mL气体A进行实验,实验记录如下:
| 编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| V(O2)/mL | 60 | 40 | 20 | 12 | 10 |
| V(空气)/mL | 40 | 60 | 80 | 88 | 90 |
| 现象 | 木炭复燃 | 木炭复燃 | 木炭复燃 | 木炭有时燃烧,有时不燃烧 | 木炭 不复燃 |
①使带火星木炭复燃的O2的体积分数最小约为
②用带火星木炭检验集气瓶里是否集满O2,若木炭复燃,能否认为集气瓶里的气体一定是纯净的O2?答:
③若按照3:2的比例混合O2和CO2气体,该混合气体能否使带火星的木炭复燃?
答:
| 编号 | 制取气体A(下列反应产生的混合气体) | B中的现象 | 结论 | ||||
| a | 在烧瓶中加热适量浓HNO3 4HNO3
|
充满红棕色气体,木炭不复燃,火星熄灭 | NO2不支持燃烧 | ||||
| b | 加热AgNO3固体 2AgNO3
|
充满红棕色气体,木炭复燃 | NO2支持燃烧 | ||||
| c | 加热Cu(NO3)2固体 2Cu(NO3)2
|
充满红棕色气体,木炭复燃 | NO2支持燃烧 |
你认为a、b、c三个结论是否可靠?说出你的理由.
a.
b.
c.
已知SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;镁和钠的化学性质也有一定的相似性.氧化铜和氧化铁是碱性氧化物,化学性质相似.三个研究性学习小组分别根据不同的微型课题进行研究,其方案如下:
I.第一个研究性学习小组用如图I所示的装置进行镁与二氧化硫反应的实验.
(1)实验室制取二氧化硫类似于制取二氧化碳,在下列物质中选择合适的试剂制取二氧化硫:
A.10%的硫酸 B.95%的硫酸 C.浓盐酸D.稀硝酸
E.亚硫酸钠固体 F.亚硫酸钙固体 G.饱和亚硫酸钠溶液
(2)反应后,发现B管壁有淡黄色固体粉末产生,取反应后B中固体溶于稀盐酸中,产生具有臭鸡蛋气味的气体,写出在B管中发生的有关化学反应方程式:
(3)提出该装置的不足之处并写出改进方法:
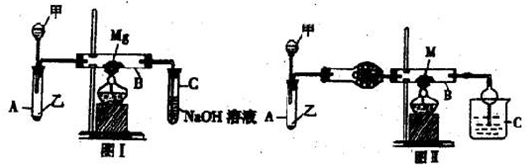
Ⅱ.第二个研究性学习小组利用I装置(图I)进行适当改进(图Ⅱ)来探究氨气的还原性.
(4)分别注明所用试剂:甲
Ⅲ. 第三个研究性学习小组认为第1I组实验装置(图II)中在A、C处添加加热装置就可以验证:乙醇在加热条件下能否被氧化铁氧化,且验证主要产物.
(5)C处的加热方法是
查看习题详情和答案>>
I.第一个研究性学习小组用如图I所示的装置进行镁与二氧化硫反应的实验.
(1)实验室制取二氧化硫类似于制取二氧化碳,在下列物质中选择合适的试剂制取二氧化硫:
BE
BE
.A.10%的硫酸 B.95%的硫酸 C.浓盐酸D.稀硝酸
E.亚硫酸钠固体 F.亚硫酸钙固体 G.饱和亚硫酸钠溶液
(2)反应后,发现B管壁有淡黄色固体粉末产生,取反应后B中固体溶于稀盐酸中,产生具有臭鸡蛋气味的气体,写出在B管中发生的有关化学反应方程式:
2Mg+SO2
2MgO+S,Mg+S
MgS
| ||
| ||
2Mg+SO2
2MgO+S,Mg+S
MgS
| ||
| ||
(3)提出该装置的不足之处并写出改进方法:
在A、B之间加一个干燥管
在A、B之间加一个干燥管
.
Ⅱ.第二个研究性学习小组利用I装置(图I)进行适当改进(图Ⅱ)来探究氨气的还原性.
(4)分别注明所用试剂:甲
浓氨水
浓氨水
,乙生石灰或氢氧化钠
生石灰或氢氧化钠
,M为氧化铜,C为水
水
.确认反应己发生的实验现象黑色氧化铜粉末变红色粉末,试管内壁有水珠
黑色氧化铜粉末变红色粉末,试管内壁有水珠
.Ⅲ. 第三个研究性学习小组认为第1I组实验装置(图II)中在A、C处添加加热装置就可以验证:乙醇在加热条件下能否被氧化铁氧化,且验证主要产物.
(5)C处的加热方法是
水浴加热烧杯
水浴加热烧杯
.分别注明试剂:甲为乙醇,M为氧化铁,C为银氨溶液
银氨溶液
,B中发生反应的化学方程式是3CH3CH2OH+Fe2O3
2Fe+3CH3CHO+3H2O
| △ |
3CH3CH2OH+Fe2O3
2Fe+3CH3CHO+3H2O
.| △ |
(2009?黄浦区二模)如图中A、B、C分别是某课外活动小组设计的制取氨气并进行喷泉实验的三组装置示意图,制取NH3选用试剂如图所示,回答下列问题:

(1)用A图所示的装置可制备干燥的NH3
①反应的化学方程式为:
②干燥管中干燥剂能否改用无水CaCl2
(2)用B图所示的装置可快速制取较大量NH3拟作喷泉实验.根据B图所示的装置及试剂回答下列问题:
①用化学方程式表示浓氨水滴入CaO中有大量NH3逸出的过程:
②检验NH3是否收集满的实验方法是:
(3)用C图所示的装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是
若测得C装置烧瓶中NH3的质量是相同状况下相同体积H2质量的10倍,则喷泉实验完毕后,烧瓶中水可上升至烧瓶容积的
(填“几分之几”).
查看习题详情和答案>>

(1)用A图所示的装置可制备干燥的NH3
①反应的化学方程式为:
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
.装置中收集NH3的试管口放置棉花团的作用是
| ||
防止空气对流,使NH3充满试管
防止空气对流,使NH3充满试管
.②干燥管中干燥剂能否改用无水CaCl2
不能
不能
,理由是CaCl2+8NH3=CaCl2?8NH3
CaCl2+8NH3=CaCl2?8NH3
.(2)用B图所示的装置可快速制取较大量NH3拟作喷泉实验.根据B图所示的装置及试剂回答下列问题:
①用化学方程式表示浓氨水滴入CaO中有大量NH3逸出的过程:
CaO+H2O=Ca(OH)2,反应放热,NH3?H2O
NH3↑+H2O
| ||
CaO+H2O=Ca(OH)2,反应放热,NH3?H2O
NH3↑+H2O
| ||
②检验NH3是否收集满的实验方法是:
用玻璃棒蘸取少许浓盐酸靠近收集NH3的试管口,若产生白烟,说明试管已收集满NH3,反之,则没有收集满.
或用湿润的红色石蕊试纸靠近收集NH3的试管口,若湿润的红色石蕊试纸变蓝,则说明NH3已收集满,反之,则没有收集满.
或用湿润的红色石蕊试纸靠近收集NH3的试管口,若湿润的红色石蕊试纸变蓝,则说明NH3已收集满,反之,则没有收集满.
用玻璃棒蘸取少许浓盐酸靠近收集NH3的试管口,若产生白烟,说明试管已收集满NH3,反之,则没有收集满.
或用湿润的红色石蕊试纸靠近收集NH3的试管口,若湿润的红色石蕊试纸变蓝,则说明NH3已收集满,反之,则没有收集满.
.或用湿润的红色石蕊试纸靠近收集NH3的试管口,若湿润的红色石蕊试纸变蓝,则说明NH3已收集满,反之,则没有收集满.
(3)用C图所示的装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是
打开止水夹挤出胶头滴管中的水
打开止水夹挤出胶头滴管中的水
,该实验的原理是:NH3极易溶解于水,致使烧瓶内压强迅速减小
NH3极易溶解于水,致使烧瓶内压强迅速减小
.若测得C装置烧瓶中NH3的质量是相同状况下相同体积H2质量的10倍,则喷泉实验完毕后,烧瓶中水可上升至烧瓶容积的
| 3 |
| 4 |
| 3 |
| 4 |
(2009?巢湖二模)某校化学兴趣小组为探究铜的常见化合物性质,提出了如下问题进行探究.请你协助该小组的同学完成下列探究活动.
提出问题①CuO能否被NH3还原?②如何安全的进行“钠投入CuSO4 溶液反应”的实验?
资料卡片Cu2O是红色粉末.Cu+在酸性溶液中能发生自身氧化还原反应生成Cu2+和Cu.
实验方案(1)为解决问题①,设计的实验装置如下(夹持及尾气处理装置未画出):
实验中观察到黑色CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体.
(2)为解决问题②,该小组做了以下两组实验:
I.分别取40mL2%的CuSO4 溶液三份,各加入质量不同的钠块,实验现象如下:
II.保持钠块大小相同(约为0.05g),分别加入到不同浓度的CuSO4 溶液中,实验现象如下:
实验结论
(1)CuO能被NH3还原,该反应的化学方程式为
(2)在40mL2%的CuSO4 溶液,加入约
问题讨论
(1)有同学认为:NH3与CuO反应生成的红色物质可能含有Cu2O.你认为他的看法是否正确?
(2)从“钠投入CuSO4 溶液反应”的实验结果来看,硫酸铜溶液的浓度越大,越容易发生爆炸.你认为可能的原因是什么?提出猜想,并设计实验检验你的猜想.猜想:
查看习题详情和答案>>
提出问题①CuO能否被NH3还原?②如何安全的进行“钠投入CuSO4 溶液反应”的实验?
资料卡片Cu2O是红色粉末.Cu+在酸性溶液中能发生自身氧化还原反应生成Cu2+和Cu.
实验方案(1)为解决问题①,设计的实验装置如下(夹持及尾气处理装置未画出):

实验中观察到黑色CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体.
(2)为解决问题②,该小组做了以下两组实验:
I.分别取40mL2%的CuSO4 溶液三份,各加入质量不同的钠块,实验现象如下:
| 钠块质量 | 实验现象 |
| 0.2g | 钠块剧烈燃烧,发出爆炸声,少量的钠溅出 |
| 0.1g | 钠块燃烧,发出爆炸声 |
| 0.05g | 钠块四处游动,偶有轻微的爆炸声,未见钠块燃烧 |
实验结论
(1)CuO能被NH3还原,该反应的化学方程式为
2NH3+3CuO
N2+3Cu+3H2O
| ||
2NH3+3CuO
N2+3Cu+3H2O
.
| ||
(2)在40mL2%的CuSO4 溶液,加入约
0.05
0.05
g的钠块是安全的.问题讨论
(1)有同学认为:NH3与CuO反应生成的红色物质可能含有Cu2O.你认为他的看法是否正确?
是
是
(填是或否),请你设计一个实验检验该红色物质中是否含有Cu2O.取少量样品,加入稀H2SO4,若溶液出现蓝色,说明红色物质中含有Cu2O,反之,则没有
取少量样品,加入稀H2SO4,若溶液出现蓝色,说明红色物质中含有Cu2O,反之,则没有
.(2)从“钠投入CuSO4 溶液反应”的实验结果来看,硫酸铜溶液的浓度越大,越容易发生爆炸.你认为可能的原因是什么?提出猜想,并设计实验检验你的猜想.猜想:
硫酸铜溶液浓度大,生成氢氧化铜絮状沉淀多,阻止了钠块的游动,使得热量积聚,从而引发爆炸
硫酸铜溶液浓度大,生成氢氧化铜絮状沉淀多,阻止了钠块的游动,使得热量积聚,从而引发爆炸
;检验方案用不同浓度的硫酸铜溶液加入一定浓度NaOH溶液生成絮状氢氧化铜沉淀后,立即加入0.1g钠块实验,观察现象
用不同浓度的硫酸铜溶液加入一定浓度NaOH溶液生成絮状氢氧化铜沉淀后,立即加入0.1g钠块实验,观察现象
.(2010?揭阳一模)硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,探索测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验可能用到的仪器如图所示:

[提出猜想]
Ⅰ.所得气体的成分可能只含
Ⅱ.所得气体的成分可能含有
Ⅲ.所得气体的成分可能含有
[实验探究]
实验操作过程(略).已知实验结束时,硫酸铜完全分解.请回答下列问题:
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:
(2)若实验结束,B中量筒没有收集到水,则证明猜想
(3)若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3?
请说明理由.答:
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不同,数据如下:
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学反应方程式:
一组:
二组:
(5)该实验设计中,由于实验操作的原因容易给测定带来最大误差的两个仪器是
查看习题详情和答案>>

[提出猜想]
Ⅰ.所得气体的成分可能只含
SO3
SO3
一种;Ⅱ.所得气体的成分可能含有
SO2、O2
SO2、O2
二种;Ⅲ.所得气体的成分可能含有
SO3、SO2、O2
SO3、SO2、O2
三种.[实验探究]
实验操作过程(略).已知实验结束时,硫酸铜完全分解.请回答下列问题:
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:
①⑨⑩⑥⑤③④⑧⑦②
①⑨⑩⑥⑤③④⑧⑦②
(填序号)(2)若实验结束,B中量筒没有收集到水,则证明猜想
Ⅰ
Ⅰ
正确.(3)若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3?
请说明理由.答:
不能,因为SO3与F中的饱和NaHSO3反应会生成等物质的量的SO2
不能,因为SO3与F中的饱和NaHSO3反应会生成等物质的量的SO2
.(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不同,数据如下:
| 实验小组 | 称取CuSO4 的质量(g) |
装置C增加 的质量(g) |
量筒中水的体积折算成标 准状况下气体的体积(mL) |
| 一 | 6.4 | 2.56 | 298.7 |
| 二 | 6.4 | 2.56 | 448 |
一组:
3CuSO4
3CuO+2SO2↑+SO3↑+O2↑
| ||
3CuSO4
3CuO+2SO2↑+SO3↑+O2↑
;
| ||
二组:
2CuSO4
2CuO+2SO2↑+O2↑
| ||
2CuSO4
2CuO+2SO2↑+O2↑
.
| ||
(5)该实验设计中,由于实验操作的原因容易给测定带来最大误差的两个仪器是
B
B
和E
E
(填代号).