摘要:13.在100ml混合酸的溶液中.硝酸的物质的量浓度为0.5mol/L.硫酸的物质的量浓度为0.15mol/L.向其中加入5.76g铜粉.微热.使其充分反应. (1)求溶液中Cu2+的物质的量浓度. (2)若要使5.76g铜粉完全溶解.且溶液中只存在一种盐.则原溶液中的硝酸和硫酸的物质的量浓度分别是多少? 14.65%HNO3(质量为M1)中加72%Mg(NO3)2溶液(质量为M2)后蒸馏.分别得到97.5%HNO3和60%Mg(NO3)2溶液(不含HNO3). (1)若蒸馏过程中HNO3.Mg(NO3)2.H2O均无损耗.求蒸馏前的投料比M1/M2的值. (2)蒸馏过程中.若H2O的损耗占总质量的5.0%.即有(M1+M2)×5.0%的H2O流失.则投料时.比值M1/M2应该 .
网址:http://m.1010jiajiao.com/timu_id_3781575[举报]
在100mL混合酸的溶液中,硝酸的物质的量浓度为0.4mol/L,硫酸的物质的量浓度为0.2mol/L,向其中加入6.4g铜粉,微热,使其充分反应,生成NO的物质的量
| A.0.1mol | B.0.03mol | C.0.02mol | D.0.04mol |
在100mL的混合酸溶液中,硝酸的物质的量浓度为0.5mol/L,硫酸的物质的量浓度为0.15mol/L,向其中加入5.76g铜粉,微热,使其充分反应.
(1)溶液中Cu2+的物质的量浓度是
(2)若要使5.76g铜粉恰好完全溶解,且溶液中只存在一种盐.则原溶液中硝酸的物质的量是
查看习题详情和答案>>
(1)溶液中Cu2+的物质的量浓度是
0.3mol/L
0.3mol/L
.(2)若要使5.76g铜粉恰好完全溶解,且溶液中只存在一种盐.则原溶液中硝酸的物质的量是
0.06mol
0.06mol
;硫酸的物质的量是0.09mol
0.09mol
.
在100mL的混合酸溶液中,硝酸的物质的量浓度为0.5mol/L,硫酸的物质的量浓度为0.15mol/L,向其中加入5.76g铜粉,微热,使其充分反应.
(1)溶液中Cu2+的物质的量浓度是______.
(2)若要使5.76g铜粉恰好完全溶解,且溶液中只存在一种盐.则原溶液中硝酸的物质的量是______;硫酸的物质的量是______.
查看习题详情和答案>>
(1)溶液中Cu2+的物质的量浓度是______.
(2)若要使5.76g铜粉恰好完全溶解,且溶液中只存在一种盐.则原溶液中硝酸的物质的量是______;硫酸的物质的量是______.
查看习题详情和答案>>
 硝酸与金属反应时,还原产物可能是NO2、NO、N2O、N2或NH
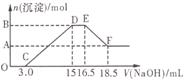
硝酸与金属反应时,还原产物可能是NO2、NO、N2O、N2或NH![]() 中的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图,则下列说法中不正确的是
中的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图,则下列说法中不正确的是
A.与HNO3反应后,Fe元素的化合价为+3
B.D→E段反应的离子方程式为:NH![]() +OH-=NH3·H2O
+OH-=NH3·H2O
C.纵坐标A点数值为0.008
D.纵坐标B点数值为0.012
查看习题详情和答案>>硝酸与金属反应时,还原产物可能是NO2、NO、N2O、N2或NH 中的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图,则下列说法中不正确的是
中的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图,则下列说法中不正确的是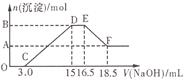
| A.与HNO3反应后,Fe元素的化合价为+3 |
B.D→E段反应的离子方程式为:NH +OH-=NH3·H2O +OH-=NH3·H2O |
| C.纵坐标A点数值为0.008 |
| D.纵坐标B点数值为0.012 |