摘要:11.(1)40 (2)2CaSO4·H2O(或CaSO4·H2O) 因为在加热过程中生石膏CaSO4·2H2O转化为相对稳定的2CaSO4·H2O.所以出现了图象中的ab段.
网址:http://m.1010jiajiao.com/timu_id_3779264[举报]
(2013?闵行区一模)碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2?yCuCO3.孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2?CuCO3.某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50mol/L Cu(NO3)2溶液、2.0mL 0.50mol/L NaOH溶液和0.25mol/L Na2CO3溶液按表Ⅰ所示体积混合.
实验2:将合适比例的混合物在表Ⅱ所示温度下反应.
实验记录如下:
表一:
表二:
(1)实验室制取少许孔雀石,应该采用的最佳反应条件:①Cu(NO3)2溶液与Na2CO3溶液的体积比为
(2)80℃时,所制得的孔雀石有少量褐色物质的原因是

步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K1、K2,关闭K3,鼓入空气,一段时间后关闭活塞K1、K2,打开K3,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
步骤4:
步骤5:称量相关装置的质量.
(3)装置A的作用是
(4)某同学在实验过程中采集了如下数据:
a.反应前玻璃管与样品的质量163.8g
b.反应后玻璃管中残留固体质量56.0g
c.装置C实验后增重9.0g
d.装置D实验后增重8.8g
为测定x/y的比值,你认为可以选用上述所采集数据中的
(5)根据你的计算结果,写出该样品组成的化学式
查看习题详情和答案>>
实验1:将2.0mL 0.50mol/L Cu(NO3)2溶液、2.0mL 0.50mol/L NaOH溶液和0.25mol/L Na2CO3溶液按表Ⅰ所示体积混合.
实验2:将合适比例的混合物在表Ⅱ所示温度下反应.
实验记录如下:
表一:
| 编号 | V (Na2CO3)/mL | 沉淀情况 |
| 1 | 2.8 | 多、蓝色 |
| 2 | 2.4 | 多、蓝色 |
| 3 | 2.0 | 较多、绿色 |
| 4 | 1.6 | 较少、绿色 |
| 编号 | 反应温度/℃ | 沉淀情况 |
| 1 | 40 | 多、蓝色 |
| 2 | 60 | 少、浅绿色 |
| 3 | 75 | 较多、绿色 |
| 4 | 80 | 较多、绿色(少量褐色) |
1:1
1:1
;②反应温度是75℃
75℃
.(2)80℃时,所制得的孔雀石有少量褐色物质的原因是
Cu(OH)2受热分解为CuO
Cu(OH)2受热分解为CuO
.实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K1、K2,关闭K3,鼓入空气,一段时间后关闭活塞K1、K2,打开K3,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
步骤4:
打开K1,继续通一段时间空气至装置冷却
打开K1,继续通一段时间空气至装置冷却
.步骤5:称量相关装置的质量.
(3)装置A的作用是
除去空气中的CO2和H2O
除去空气中的CO2和H2O
;若无装置E,则实验测定的x/y的比值将偏小
偏小
(选填“偏大”、“偏小”或“无影响”).(4)某同学在实验过程中采集了如下数据:
a.反应前玻璃管与样品的质量163.8g
b.反应后玻璃管中残留固体质量56.0g
c.装置C实验后增重9.0g
d.装置D实验后增重8.8g
为测定x/y的比值,你认为可以选用上述所采集数据中的
bc、bd、cd
bc、bd、cd
(写出所有组合的字母代号)一组即可进行计算.(5)根据你的计算结果,写出该样品组成的化学式
5Cu(OH)2?2CuCO3
5Cu(OH)2?2CuCO3
.用已知物质的量浓度的酸(或碱)来滴定未知物质的量浓度的碱(或酸)的方法叫酸碱中和滴定.中和滴定实验是以指示剂的变色来表示反应终点的到达.
(1)某学生中和滴定实验的过程如下:
①取一支碱式滴定管;
②用蒸馏水洗净;
③加入待测的NaOH溶液;
④调节起始读数,准确读取读数并记录;
⑤用酸式滴定管精确放出一定量标准酸液;
⑥置于未经标准酸液润洗的洁净锥形瓶中;
⑦加入2滴酚酞试液;
⑧开始滴定,边滴边摇荡;
⑨边注视滴定管内液面变化;
⑩当小心滴到溶液由无色变成粉红色时,即停止滴定;
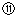 记录液面刻度的读数;
记录液面刻度的读数;
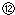 根据滴定管的两次读数得出NaOH溶液的体积为22mL
根据滴定管的两次读数得出NaOH溶液的体积为22mL
指出上述实验过程中的错误之处(填序号) .
(2)现以0.1000mol?L-1 NaOH溶液滴定20.00mL 0.1000mol?L-1HCl溶液为例,讨论强碱滴定强酸的情况,通过计算完成下表(已知:lg2=0.3,lg5=0.7.溶液混合时的体积变化忽略不计):
(3)请利用表的数据绘制滴定曲线.
(4)中和滴定过程中有好多技术问题要学会处理,如:读数时要平视.如果初读数和末读数如图所示,滴定液的用量为 mL.
查看习题详情和答案>>
(1)某学生中和滴定实验的过程如下:
①取一支碱式滴定管;
②用蒸馏水洗净;
③加入待测的NaOH溶液;
④调节起始读数,准确读取读数并记录;
⑤用酸式滴定管精确放出一定量标准酸液;
⑥置于未经标准酸液润洗的洁净锥形瓶中;
⑦加入2滴酚酞试液;
⑧开始滴定,边滴边摇荡;
⑨边注视滴定管内液面变化;
⑩当小心滴到溶液由无色变成粉红色时,即停止滴定;
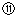 记录液面刻度的读数;
记录液面刻度的读数;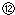 根据滴定管的两次读数得出NaOH溶液的体积为22mL
根据滴定管的两次读数得出NaOH溶液的体积为22mL指出上述实验过程中的错误之处(填序号)
(2)现以0.1000mol?L-1 NaOH溶液滴定20.00mL 0.1000mol?L-1HCl溶液为例,讨论强碱滴定强酸的情况,通过计算完成下表(已知:lg2=0.3,lg5=0.7.溶液混合时的体积变化忽略不计):
| 加入NaOH溶液的体积V/mL | 0.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 | 40.00 |
| 剩余盐酸溶液的体积V/mL | 20.00 | 2.00 | 0.20 | 0.02 | 0.00 | / | / | / | / |
| 过量NaOH溶液的体积V/mL | / | / | / | / | / | 0.02 | 0.20 | 2.00 | 20.00 |
| pH | 1.00 | 2.28 | 3.30 | 7.00 | 9.70 | 11.70 | 12.50 |

(4)中和滴定过程中有好多技术问题要学会处理,如:读数时要平视.如果初读数和末读数如图所示,滴定液的用量为
(2010?普陀区二模)反应①Fe(s)+CO2(g)?FeO(s)+CO(g)+akJ;
反应②CO(g)+
O2(g)?CO2(g)+bkJ.
测得在不同温度下,反应①的平衡常数K值随温度的变化如表所示:
(1)反应①的化学平衡常数表达式为
,a
(2)700℃反应①达到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有
A.缩小反应器体积 B.通入CO2 C.升高温度到900℃D.使用合适的催化剂
(3)图象符合反应①的是

(4)由反应①和②可求得,反应2Fe(s)+O2(g)?2FeO(s)+Q 的Q=
查看习题详情和答案>>
反应②CO(g)+
| 1 |
| 2 |
测得在不同温度下,反应①的平衡常数K值随温度的变化如表所示:
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
| c(CO) |
| c(CO2) |
| c(CO) |
| c(CO2) |
大于
大于
0(填“大于”、“小于”或“等于”). 在500℃2L密闭容器中进行反应①,CO2起始量为4mol,其转化率为50%,则CO的平衡浓度为1mol/L
1mol/L
.(2)700℃反应①达到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有
BC
BC
(填序号).A.缩小反应器体积 B.通入CO2 C.升高温度到900℃D.使用合适的催化剂
(3)图象符合反应①的是
A
A
(填序号)(图中v是速率、φ为混合物中CO含量,T为温度且T1>T2).
(4)由反应①和②可求得,反应2Fe(s)+O2(g)?2FeO(s)+Q 的Q=
2(a+b)KJ
2(a+b)KJ
.市场上有各种品牌的抗胃酸药,如复方氢氧化铝、盐酸雷尼替丁等.某研究性学习小组为了探究它们的差别及效果进行如下实验:
实验仪器:研钵、250mL烧杯、100mL量筒、电子天平
实验药品:复方氢氧化铝、盐酸雷尼替丁、0.05mol/L盐酸、蒸馏水
实验过程:
实验一:
①称量1.000g研磨后的复方氢氧化铝放入烧杯中,加入75mL蒸馏水搅拌使药品溶解;
②向溶液中缓慢滴入0.05mol/L盐酸,不断搅拌并测量溶液的pH;
③至测量的pH在3.00时,且30s内基本不变停止滴加,记录读数,重复滴定两次;
④将药品换成1.000g盐酸雷尼替丁重复上述步骤.
实验数据如下:
实验二:
①在烧杯中加入0.05mol/L盐酸50mL;
②在溶液中加入1.000g复方氢氧化铝粉末,不断搅拌,计时并同时记录pH读数的变化;
③将复方氢氧化铝粉末换成盐酸雷尼替丁重复上述步骤.
实验数据如下:
试回答下列问题:
(1)完成上述实验还缺少的仪器有 、 .
(2)用盐酸雷尼替丁进行实验二时,0~1.5min内pH减小的原因是: ;实验二不能反映药品发生反应时的实际环境,且实验时间较长,你认为应该如何控制该实验的条件 .
(3)请你根据上述实验,得出合理的实验结论:
① ;② .
查看习题详情和答案>>
实验仪器:研钵、250mL烧杯、100mL量筒、电子天平
实验药品:复方氢氧化铝、盐酸雷尼替丁、0.05mol/L盐酸、蒸馏水
实验过程:
实验一:
①称量1.000g研磨后的复方氢氧化铝放入烧杯中,加入75mL蒸馏水搅拌使药品溶解;
②向溶液中缓慢滴入0.05mol/L盐酸,不断搅拌并测量溶液的pH;
③至测量的pH在3.00时,且30s内基本不变停止滴加,记录读数,重复滴定两次;
④将药品换成1.000g盐酸雷尼替丁重复上述步骤.
实验数据如下:
| 复方氢氧化铝 | 盐酸雷尼替丁 | |||
| 滴定前 | 滴定后 | 滴定前 | 滴定后 | |
| 1 | 0.01 | 79.8 | 0.02 | 18.6 |
| 2 | 0.00 | 79.5 | 0.03 | 19.0 |
| 3 | 0.03 | 80.5 | 0.00 | 18.7 |
①在烧杯中加入0.05mol/L盐酸50mL;
②在溶液中加入1.000g复方氢氧化铝粉末,不断搅拌,计时并同时记录pH读数的变化;
③将复方氢氧化铝粉末换成盐酸雷尼替丁重复上述步骤.
实验数据如下:
| 时间(min) | 0 | 0.5 | 1 | 1.5 | 2 | 2.5 | 3 | 3.5 | 4 | 5 |
| 复方氢氧化铝 | 3.53 | 3.62 | 3.70 | 3.75 | 3.79 | 3.84 | 3.88 | 3.89 | 3.90 | 3.92 |
| 盐酸雷尼替丁 | 1.72 | 1.65 | 1.60 | 1.55 | 1.74 | 1.80 | 1.84 | 1.87 | 1.87 | 1.88 |
| 时间(min) | 10 | 15 | 20 | 25 | 30 | 35 | 40 | |||
| 复方氢氧化铝 | 3.97 | 4.01 | 4.12 | 4.13 | 4.14 | 4.15 | 4.15 | |||
| 盐酸雷尼替丁 | 1.88 | 1.87 | 1.88 |
(1)完成上述实验还缺少的仪器有
(2)用盐酸雷尼替丁进行实验二时,0~1.5min内pH减小的原因是:
(3)请你根据上述实验,得出合理的实验结论:
①
(2011?西安模拟)一定温度下,在一个带有活塞的容积可变的密闭容器中(活塞的一端与大气相通),发生如下反应:X(g)+3Y(g)
=2Z(g)△H<0若反应开始时充入2molX和8molY,达到平衡后,测得平衡时混合气体的总物质的量为8.4mol,X的体积分数为w%.
(1)写出该反应平衡常数的表达式
(2)若增大压强,该反应的化学反应速率将
(3)保持上述反应温度不变,设a、b、c分别代表初始加入的X、Y、Z的物质的量,若反应达平衡后,混合气体中x的体积分数仍为w%,那么:
若a=1,c=2,则b=
(4)保持上述反应温度不变,若按下列四种配比作为起始物质,达平衡后X的体积分数大于w%的是
A.4molZ B.2.5molX、4.5molY和 1molZ
C.3molX和 6molY D.1molX和 4molZ.
查看习题详情和答案>>
| ||
(1)写出该反应平衡常数的表达式
K=
| c2(Z) |
| c(X)?c3(Y) |
K=
,并计算平衡时X的转化率| c2(Z) |
| c(X)?c3(Y) |
40%
40%
.(2)若增大压强,该反应的化学反应速率将
增大
增大
,该反应的K值将不变
不变
(均填“增大”“减小”或“不变”).(3)保持上述反应温度不变,设a、b、c分别代表初始加入的X、Y、Z的物质的量,若反应达平衡后,混合气体中x的体积分数仍为w%,那么:
若a=1,c=2,则b=
5
5
,在此情况下反应起始时将向逆反应
逆反应
方向进行.(4)保持上述反应温度不变,若按下列四种配比作为起始物质,达平衡后X的体积分数大于w%的是
ABCD
ABCD
.(填序号)A.4molZ B.2.5molX、4.5molY和 1molZ
C.3molX和 6molY D.1molX和 4molZ.