摘要: (1)试管底部与烧杯底部接触 (2)冷凝回流 粉红,粘稠(6)乙醇 (7)
网址:http://m.1010jiajiao.com/timu_id_3779032[举报]
 如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸入2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题:
如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸入2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题:(1)教材中是用与制O2相同的制备装置来加热制取NH3的,该反应的化学方程式为:
2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2
| ||
2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2
.
| ||
(2)下面是部分同学对于能用图1制取NH3的原因分析,有道理的是
①②③④
①②③④
.①在NH3?H2O中有平衡 NH3+H2O=NH3?H2O=NH4++OH-,NaOH使平衡向左移动; ②在NH3?H2O中有平衡阳NH3+H2O=NH3?H2O=NH4++OH-,NH4Cl 使平衡向左移动; ③NaOH 溶于水时放热,使体系的温度升高,NH3的溶解度减小;④NH4Cl与NaOH在此情况下可反应生成NH3,即NH4++OH-
| ||
(3)判断图1中烧瓶己收满NH3的现象
烧杯内的溶液变红
烧杯内的溶液变红
.(4)图2中胶头漓管中的水挤入烧瓶后,观察到的现象是
气球逐渐变大
气球逐渐变大
它说明了NH3极易溶于水
极易溶于水
.(2011?湖北模拟)利用图进行浓硫酸与铜反应,并验证二氧化硫的性质.
实验操作如下:连接仪器和安放药品,用酒精灯加热1分钟后撤去酒精灯,将铜丝伸入液面以下,一段时间后拉起铜丝.
请回答下列问题:
(1)将反应后的试管充分静置,观察到试管底部有白色固体出现,中间层是浅黄色液体(浓硫酸),上层是蓝色溶液.白色固体的化学式为
①酸性 ②强氧化性 ③吸水性 ④脱水性
(2)直玻璃管中依次观察到的现象是:
(3)某次实验中小烧杯中澄清石灰水始终未观察到浑浊,你猜想可能的原因是
(4)某学生发现,常温下将铜片长时间放入浓硫酸的试管中并密封,最终生成黑色物质(Cu2S)和蓝色溶液,无气体生成,写出此条件下铜片与浓硫酸反应的化学方程式:
查看习题详情和答案>>

实验操作如下:连接仪器和安放药品,用酒精灯加热1分钟后撤去酒精灯,将铜丝伸入液面以下,一段时间后拉起铜丝.
请回答下列问题:
(1)将反应后的试管充分静置,观察到试管底部有白色固体出现,中间层是浅黄色液体(浓硫酸),上层是蓝色溶液.白色固体的化学式为
CuSO4
CuSO4
,上述现象中体现了浓硫酸的性质有①②③
①②③
(填序号)①酸性 ②强氧化性 ③吸水性 ④脱水性
(2)直玻璃管中依次观察到的现象是:
蓝色石蕊试纸变为红色
蓝色石蕊试纸变为红色
;红色滤纸变为白色
红色滤纸变为白色
;紫红色滤纸变为白色
紫红色滤纸变为白色
.(3)某次实验中小烧杯中澄清石灰水始终未观察到浑浊,你猜想可能的原因是
SO2易溶于水,大量SO2与Ca(OH)2生成易溶于水的Ca(HSO3)2而不产生CaSO3浑浊
SO2易溶于水,大量SO2与Ca(OH)2生成易溶于水的Ca(HSO3)2而不产生CaSO3浑浊
,请设计实验证明它.取小烧杯中溶液少许于另一支试管中,加入足量NaOH溶液,若有白色沉淀生成,则证明猜想合理
取小烧杯中溶液少许于另一支试管中,加入足量NaOH溶液,若有白色沉淀生成,则证明猜想合理
.(4)某学生发现,常温下将铜片长时间放入浓硫酸的试管中并密封,最终生成黑色物质(Cu2S)和蓝色溶液,无气体生成,写出此条件下铜片与浓硫酸反应的化学方程式:
5Cu+4H2SO4(浓)=Cu2S+3CuSO4+4H2O
5Cu+4H2SO4(浓)=Cu2S+3CuSO4+4H2O
. 实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55℃~60℃反应,已知苯与硝基苯的基本物理性质如下表所示:
实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55℃~60℃反应,已知苯与硝基苯的基本物理性质如下表所示:| 熔点 | 沸点 | 状态 | |
| 苯 | 5.51℃ | 80.1℃ | 液体 |
| 硝基苯 | 5.7℃ | 210.9℃ | 液体 |
将浓H2SO4沿烧杯内壁缓缓注入浓HNO3中,并用玻璃棒不断搅拌
将浓H2SO4沿烧杯内壁缓缓注入浓HNO3中,并用玻璃棒不断搅拌
.(2)分离硝基苯和水的混合物的方法是
分液
分液
;分离硝基苯和苯的方法是蒸馏
蒸馏
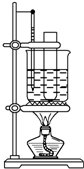
.(3)某同学用如图装置制取硝基苯:
①用水浴加热的优点是
使反应体系受热均匀,容易控制温度
使反应体系受热均匀,容易控制温度
;②指出该装置的两处缺陷
试管底部不能与烧杯底部接触
试管底部不能与烧杯底部接触
;缺少一个带有长直玻璃导管的橡皮塞
缺少一个带有长直玻璃导管的橡皮塞
.(2009?深圳二模)已知某白色混合物粉末中含有 Al2 (SO4)3、Na2SO4、NH4HCO3、NH4Cl、KCl五种物质中的两种.请完成下述探究混合物组成的实验
限选仪器、用品与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、酒精灯、火柴、试管夹;紫色石蕊试纸;1mol?L-1硝酸、1mol?L-1盐酸、1mol?L-1NaOH溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水.
I、初步探究
取适量混合物于烧杯中,用蒸馏水完全溶解,得到无色透明溶液A;取少量A于试管中,滴加稀硝酸,有无色气泡产生,继续滴加稀硝酸至溶液中不再产生气泡,得到无色透明溶液B.
(1)上述实验证明:该混合物中肯定含有
II、进一步探究
(2)为了进一步确定该混合固体的组成,需要进行实验1或实验1、2,完成下表:
查看习题详情和答案>>
限选仪器、用品与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、酒精灯、火柴、试管夹;紫色石蕊试纸;1mol?L-1硝酸、1mol?L-1盐酸、1mol?L-1NaOH溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水.
I、初步探究
取适量混合物于烧杯中,用蒸馏水完全溶解,得到无色透明溶液A;取少量A于试管中,滴加稀硝酸,有无色气泡产生,继续滴加稀硝酸至溶液中不再产生气泡,得到无色透明溶液B.
(1)上述实验证明:该混合物中肯定含有
碳酸氢铵
碳酸氢铵
(名称),肯定不含有Al2(SO4)3
Al2(SO4)3
(化学式)II、进一步探究
(2)为了进一步确定该混合固体的组成,需要进行实验1或实验1、2,完成下表:
| 实验操作 | 预期现象和结论 |
| 实验1:取少量溶液B于试管中,加入少量 Ba(NO3)2溶液,振荡,静置观察. | 如果产生白色沉淀,说明原固体混合物含有Na2SO4,该混合物组成为NH4HCO3和Na2SO4;若没有白色沉淀生成,说明原固体混合物中不含Na2SO4;含有KCl和NH4Cl 如果产生白色沉淀,说明原固体混合物含有Na2SO4,该混合物组成为NH4HCO3和Na2SO4;若没有白色沉淀生成,说明原固体混合物中不含Na2SO4;含有KCl和NH4Cl |
| 实验2: 若固体混合物不含Na2SO4;取少量原固体混合物放于试管中,将试管套入试管夹,用火柴点燃酒精灯充分加热 若固体混合物不含Na2SO4;取少量原固体混合物放于试管中,将试管套入试管夹,用火柴点燃酒精灯充分加热 |
如果试管底部有固体剩余说明混合物中含有KCl,该混合物的组成为KCl和NH4HCO3,如试管底部无固体残留,说明固体中含有NH4Cl,该混合物的组成为NH4Cl和NH4HCO3; 如果试管底部有固体剩余说明混合物中含有KCl,该混合物的组成为KCl和NH4HCO3,如试管底部无固体残留,说明固体中含有NH4Cl,该混合物的组成为NH4Cl和NH4HCO3; |
 此题分A、B题,任选一题答题,两题都做分数以A题为准,B题较容易.
此题分A、B题,任选一题答题,两题都做分数以A题为准,B题较容易.A题:在盛有少量无水乙醇的试管中,加入一小块新切的、擦干表面煤油的金属钠,迅速用配有导管的单孔塞塞住试管口,用一小试管收集并验纯气体后,点燃,并把干燥的小烧杯罩在火焰上,片刻,迅速倒转烧杯,向烧杯中加入少量澄清石灰水.观察现象,完成下表.
(1)
| 乙醇与钠反应的现象 | 气体燃烧的现象 | 检验产物 |
| ① Na沉到试管底部 Na沉到试管底部 ② 反应有气泡产生 反应有气泡产生 ③ 反应时放出热量 反应时放出热量 |
蓝色 蓝色 有水珠(或有水雾) 有水珠(或有水雾) 不变浑浊 不变浑浊 |
H2 H2 |
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
B题:如图,某气体X可能由H2、CO、CH4中的一种组成.将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶.试回答下列问题:
(1)若A洗气瓶的质量增加,B洗气瓶的质量不变,则气体X是
H2
H2
.(2)若A洗气瓶的质量不变,B洗气瓶的质量增加,则气体X是
CO
CO
.(3)若A、B两个洗气瓶的质量都增加,则气体X可能是
CH4;H2、CO;CH4、H2;CH4、CO、CH4、H2、CO
CH4;H2、CO;CH4、H2;CH4、CO、CH4、H2、CO
.