摘要:10.下列物质久置与空气中发生颜色改变的是 ①绿矾 ②氢氧化亚铁 ③碘化钾 ④苯酚 ⑤过氧化钠 A.①③ B.③④ C.①②⑤ D.①②③④⑤ (本题考查了部分重要物质与氧气的反应以及颜色的变化)
网址:http://m.1010jiajiao.com/timu_id_3778770[举报]
| |||||||||||||||||||||||||||||||||
敌草胺是一种除草剂.它的合成路线如下:

回答下列问题:
(1)在空气中久置,A易被空气中O2氧化而由无色转变为棕色,这与下列物质中的________(填序号)的性质类似.
A.
B.
C.
D.
(2)C分子中有2个含氧官能团,分别为________和________(填官能团名称).
(3)由B与CH3CHClCOOH转化成C时,从结构上看,还有另一种无机物生成,则该无机物是________.
(4)若C不经提纯,产物敌草胺中将混有少量副产物E,E是一种由B和C生成的酯(变化过程中碳原子数未变),推断E的分子式为________.
(5)已知:![]() ,若以苯酚和乙酸为原料制备
,若以苯酚和乙酸为原料制备 ,其合成路线中应分为________步变化.
,其合成路线中应分为________步变化.
 把在空气中久置的铝片5.0g投入盛有500mL0,5mol?L-1盐酸溶液的烧杯中该铝片与盐酸反应产生氢气的速率与反应时间可用如图所示的坐标曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL0,5mol?L-1盐酸溶液的烧杯中该铝片与盐酸反应产生氢气的速率与反应时间可用如图所示的坐标曲线来表示,回答下列问题:(1)曲线由0→a段不产生氢气的原因,用化学方程式为
Al2O3+6HCl=2AlCl3+3H2O
Al2O3+6HCl=2AlCl3+3H2O
;(2)曲线由b→c段产生氢气的速率增加较快的主要原因
反应放热,溶液温度升高,反应速率加快
反应放热,溶液温度升高,反应速率加快
;(3)向溶液中加入下列物质,能加快上述化学反应速率的是
BDE
BDE
.A.蒸馏水 B.改用铝粉 C.饱和氯化钠溶液 D.浓盐酸 E.少量硫酸铜溶液.
下表是周期表中的一部分,请回答下列问题:

(1)A是④的最高价含氧酸,其化学式为
(2)将③对应的单质投入A的稀溶液中,发生的反应属于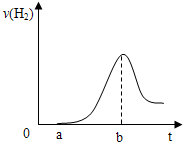
(3)把在空气中久置的③的单质投入A的稀溶液中,产生氢气的速率与反应时间的关系可用如图曲线表示:
曲线0→a段不产生氢气的原因是
曲线由b以后产生氢气速率逐渐减小的主要原因是
(4)①和②对应的单质在一个固定体积的密闭容器中发生可逆反应,该反应达到平衡的标志是
查看习题详情和答案>>

(1)A是④的最高价含氧酸,其化学式为
H2SO4
H2SO4
,A中所含的化学键类型为共价键
共价键
.(2)将③对应的单质投入A的稀溶液中,发生的反应属于
放热
放热
反应(填“吸热”或“放热”),该反应中反应物的总能量大于
大于
生成物的总能量(填“大于”或“小于”);若将③对应的单质和铁用导线连接后投入A的稀溶液中,组成的装置中能量转化形式主要是化学能转化为电能
化学能转化为电能
,该装置正极材料是Fe
Fe
.
(3)把在空气中久置的③的单质投入A的稀溶液中,产生氢气的速率与反应时间的关系可用如图曲线表示:
曲线0→a段不产生氢气的原因是
铝表面被O2氧化为致密的氧化膜,限制了铝与H2SO4的反应
铝表面被O2氧化为致密的氧化膜,限制了铝与H2SO4的反应
,曲线a→b段产生氢气速率逐渐增大的主要原因是反应放热,温度升高是影响反应速率的主要因素,使反应速率增大
反应放热,温度升高是影响反应速率的主要因素,使反应速率增大
,曲线由b以后产生氢气速率逐渐减小的主要原因是
随反应c(H+)减小,该因素变为影响化学反应速率的主要因素,化学反应速率开始下降
随反应c(H+)减小,该因素变为影响化学反应速率的主要因素,化学反应速率开始下降
.(4)①和②对应的单质在一个固定体积的密闭容器中发生可逆反应,该反应达到平衡的标志是
各成分的浓度(或质量、物质的量、压强等)不再变化
各成分的浓度(或质量、物质的量、压强等)不再变化
(请列举一项).(2011?武胜县一模)A、B、C、D、E均为可溶于水的固体,它们的离子可能有:Na+、Ca2+、Ba2+、C1O-、HSO4-、CO32-、C1-.
分别取他们的溶液进行实验,主要操作及现象如下:
①向A的溶液中通入二氧化碳,再加入品红溶液,红色褪去.
②将B和C的溶液混合,生成白色沉淀,该沉淀可溶于E溶液.
③将B和D的溶液混合,生成白色沉淀,继续加入过量的E溶液,有气泡产生的同时还有白色沉淀存在.
④A和E溶液的焰色反应都呈黄色.
(1)写出下列物质的化学式:A
(2)写出E溶液与铝发生反应的实验现象为
(3)向B的溶液中,缓慢滴入少量稀的E溶液后,其主要的溶质成分为
(4)D在空气中长期久置会失效.其化学方程式为
查看习题详情和答案>>
分别取他们的溶液进行实验,主要操作及现象如下:
①向A的溶液中通入二氧化碳,再加入品红溶液,红色褪去.
②将B和C的溶液混合,生成白色沉淀,该沉淀可溶于E溶液.
③将B和D的溶液混合,生成白色沉淀,继续加入过量的E溶液,有气泡产生的同时还有白色沉淀存在.
④A和E溶液的焰色反应都呈黄色.
(1)写出下列物质的化学式:A
NaC1O
NaC1O
、BNa2CO3
Na2CO3
、CCaC12或Ca(C1O)2
CaC12或Ca(C1O)2
、ENaHSO4
NaHSO4
.(2)写出E溶液与铝发生反应的实验现象为
有气体产生
有气体产生
.(3)向B的溶液中,缓慢滴入少量稀的E溶液后,其主要的溶质成分为
NaHCO3或Na2SO4
NaHCO3或Na2SO4
.(填化学式)(4)D在空气中长期久置会失效.其化学方程式为
Ba(ClO)2+CO2+H2O═BaCl2+2HClO、2HClO
2HCl+O2↑
| ||
Ba(ClO)2+CO2+H2O═BaCl2+2HClO、2HClO
2HCl+O2↑
.
| ||





 ,其合成路线中应分为________步变化.
,其合成路线中应分为________步变化.