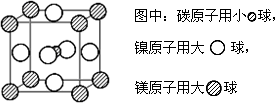
摘要:1.无机物的相互反应 (1)无机物间能否反应.主要决定于反应物的性质及反应时的客观条件.上图示左边的无机物间的相互反应指其主要性质而言.至于各个具体物质间能否反应.还有一些具体条件要加以考虑. (2)对于氧化物要注意以下问题:①氧化物不一定能直接与水作用生成对应的酸或碱,②金属氧化物有可能是碱性氧化物也有可能是酸性氧化物或两性氧化物.一般有“高价酸.低价碱 的说法.即高价的是酸性氧化物.而低价的是碱性氧化物.如Mn2O7是酸性氧化物.而MnO则是碱性氧化物,③酸性氧化物也叫酸酐.但酸酐不一定是氧化物.如有机酸酸酐就不是氧化物. (3)还有一些特殊的反应比较重要.应结合具体物质的性质.加以理解记忆.如: ①C12+H2O- ②C12+NaOH- ③Mg+CO2- ④Al+NaOH+H2O- ⑤Al+Fe2O3- ⑥SiO2+C- ⑦NO2+H2O- ⑧Na2O2+H2O (CO2)- ⑨弱酸的正盐与弱酸反应.生成相应酸式盐: Na2CO3+CO2+H2O- ⑩弱酸的酸式盐与强碱反应.生成正盐: NaHCO3+NaOH-
网址:http://m.1010jiajiao.com/timu_id_3778479[举报]
 碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.(1)C60分子能与F2发生加成反应,其加成产物为
C60F60
C60F60
,C60分子的晶体中,在晶胞的顶点和面心均含有一个C60分子,则一个C60晶胞的质量为| 2880 |
| NA |
| 2880 |
| NA |
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是
ac
ac
.a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有
ae
ae
.a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C;
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力;
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
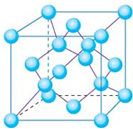
(4)金刚石晶胞结构如图,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为
正四面体
正四面体
,B原子与N原子之间共价键与配位键的数目比为3:1
3:1
,一个晶胞中N原子数目为4
4
.(5)C与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为
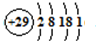
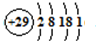
12
12
.已知Cu单质的晶体密度为ρg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的原子半径为
| ||
| 4 |
| 3 |
| ||
| ||
| 4 |
| 3 |
| ||
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
(1)C60分子能与F2发生加成反应,其加成产物为______,C60分子的晶体中,在晶胞的顶点和面心均含有一个C60分子,则一个C60晶胞的质量为______.
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是______.
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有______.
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C;
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力;
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
(4)金刚石晶胞结构如图,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为______,B原子与N原子之间共价键与配位键的数目比为______,一个晶胞中N原子数目为______.
(5)C与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为______,金属铜采用面心立方最密堆积(在晶胞的顶点和面心均含有一个Cu原子),则Cu的晶体中Cu原子的配位数为______.已知Cu单质的晶体密度为ρg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的原子半径为______.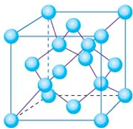
查看习题详情和答案>>
(1)C60分子能与F2发生加成反应,其加成产物为______,C60分子的晶体中,在晶胞的顶点和面心均含有一个C60分子,则一个C60晶胞的质量为______.
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是______.
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有______.
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C;
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力;
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
(4)金刚石晶胞结构如图,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为______,B原子与N原子之间共价键与配位键的数目比为______,一个晶胞中N原子数目为______.
(5)C与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为______,金属铜采用面心立方最密堆积(在晶胞的顶点和面心均含有一个Cu原子),则Cu的晶体中Cu原子的配位数为______.已知Cu单质的晶体密度为ρg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的原子半径为______.

碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
(1)C60分子能与F2发生加成反应,其加成产物为______,C60分子的晶体中,在晶胞的顶点和面心均含有一个C60分子,则一个C60晶胞的质量为______.
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是______.
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有______.
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C;
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力;
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
(4)金刚石晶胞结构如图,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为______,B原子与N原子之间共价键与配位键的数目比为______,一个晶胞中N原子数目为______.
(5)C与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为______,金属铜采用面心立方最密堆积(在晶胞的顶点和面心均含有一个Cu原子),则Cu的晶体中Cu原子的配位数为______.已知Cu单质的晶体密度为ρg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的原子半径为______
 查看习题详情和答案>>
查看习题详情和答案>>
(1)C60分子能与F2发生加成反应,其加成产物为______,C60分子的晶体中,在晶胞的顶点和面心均含有一个C60分子,则一个C60晶胞的质量为______.
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是______.
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有______.
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C;
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力;
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
(4)金刚石晶胞结构如图,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为______,B原子与N原子之间共价键与配位键的数目比为______,一个晶胞中N原子数目为______.
(5)C与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为______,金属铜采用面心立方最密堆积(在晶胞的顶点和面心均含有一个Cu原子),则Cu的晶体中Cu原子的配位数为______.已知Cu单质的晶体密度为ρg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的原子半径为______
 查看习题详情和答案>>
查看习题详情和答案>>
Ⅰ、
氯化铬酰(CrO2Cl2)在有机合成中可作(1)写出铬原子的基态电子排布式________,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有________(填元素符号),其中一种金属的晶胞结构如下图所示,该晶胞中含有金属原子的数目为________.
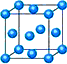
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是________(填“极性”或“非极性”)分子.
(3)在①苯
②CH3OH
③HCHO
④CS2
⑤CCl4
⑥CH3Cl
⑦HCOOH七种有机物质中,碳原子采取sp2杂化的分子有________(填序号),CS2![]() 分子的空间构型是________.
分子的空间构型是________.
Ⅱ、不锈钢是由铁、铬、镍、碳及众多不同元素所组![]() 成的合金.
成的合金.
(1)基![]() 态碳(C)原子的价电子排布式为________.
态碳(C)原子的价电子排布式为________.
(2)[Cr(H2O)4Cl2]Cl·2H2O中Cr3+的配位数为________;[Cr(H2O)4Cl2]Cl中含有的化学键为________.
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型.423 K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测:四羰基镍的晶体类型是________,Ni(CO)4易溶于________(填序号).
A.水
B.四氯化碳
C.苯
D.硫酸镍溶液
(4)据报道,只含镁、镍和碳三![]() 种元素的晶体竟然具有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式________.晶体中
种元素的晶体竟然具有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式________.晶体中![]() 每个镁原子周围距离最近的镍原子有________个.
每个镁原子周围距离最近的镍原子有________个.