摘要:2..H2(氢) (2)3Mg+N2 Mg3N2 (3)O2+2NO = 2NO2 讲析:解本题的突破口.可以尝试从棕色气体I着手.若考虑它是NO2.则H和A就应考虑分别是NO和O2.这样C应为N2.B的首选当然是Mg(因为Mg分别与O2和N2反应时.其化学计量关系均满足题中条件).再根据题中C与D反应生成E的计量关系.可判断D为H2.这样可以将图中每种物质都确定下来.它们是:A为O2.B为Mg.C为N2.D为H2.E为NH3.F为Mg3N2.G为MgO.H为NO.I为NO2.J为H2O.再进行有关反应的化学计量关系的检验.都符合题意.故以上答案正确无误.
网址:http://m.1010jiajiao.com/timu_id_3778470[举报]
海水是镁的重要来源,从海水中提镁须经过以下流程:
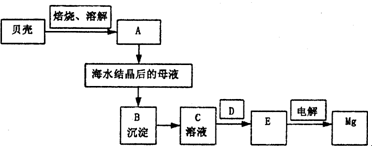
(1)分别写出A、B、C、D、E是什么物质.
A B C D E
(2)回答为什么不选择电解MgO制备金属镁. .
(3)用电解法制备碱金属、碱土金属时,常常加入CaC12,为什么? .
(4)海水结晶后的母液中加入生石灰,请计算溶液中pH=11时,溶液中Mg2+浓度为 mol/L.[K sp[Mg(OH)2]=5.6×10-12]
(5)我国从20世纪70年代开始采用硅热法炼镁,现年产量已达35.4万吨左右.根据下列条件,完成填空:
Mg(s)+O2(g)=2MgO(s)△H=-601.83kJ/mol
Mg(s)=Mg(g)△H=+150kJ/mol
Si(s)+O2(g)=SiO2(s)△H=-859.4kJ/mol
2MgO(s)+Si(s)=SiO2(s)+2Mg(g)△H= .
查看习题详情和答案>>

(1)分别写出A、B、C、D、E是什么物质.
A
(2)回答为什么不选择电解MgO制备金属镁.
(3)用电解法制备碱金属、碱土金属时,常常加入CaC12,为什么?
(4)海水结晶后的母液中加入生石灰,请计算溶液中pH=11时,溶液中Mg2+浓度为
(5)我国从20世纪70年代开始采用硅热法炼镁,现年产量已达35.4万吨左右.根据下列条件,完成填空:
Mg(s)+O2(g)=2MgO(s)△H=-601.83kJ/mol
Mg(s)=Mg(g)△H=+150kJ/mol
Si(s)+O2(g)=SiO2(s)△H=-859.4kJ/mol
2MgO(s)+Si(s)=SiO2(s)+2Mg(g)△H=
金属镁可用于制造合计、储氢材料、镁电池等.
已知:C(s)+
O2(g)=CO(g)△H=-110.5kJ?mol-1
Mg(g)+
O2(g)=MgO(s)△H=-732.7kJ?mol-1
(1)一种制备镁的反应为:MgO(s)+C(s)=Mg(g)+CO(g),该反应的△H= .
(2)一种用水氯镁石(主要成分为MgCl2?6H2O)制备金属镁工艺的关键流程如下:

①为探究MgCl2?6H2O“一段脱水”的合理温度范围,某科研小组将MgCl2?6H2O在不同温度下分解,测得残留固体物质的X-射线衍射谱图如图所示(X-射线衍射可用于判断某晶态物质是否存在).

测得E中Mg元素质量分数为60.0%,则E的化学式为 .“一段脱水”的目的是制备MgCl2?2H2O,温度不高于180℃的原因是 .
②若电解时电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低点解效率,生成MgO的化学方程式为 .
③该工艺,可以循环使用的物质有 .
(3)Mg2Ni是一中储氢材料,2.14g Mg2Ni在一定条件下能吸收0.896L H2(标准状况下)生成X,X的化学式为 .“镁-次氯酸盐”燃料电池的装置如图,该电池反应的总反应方程式为 .

查看习题详情和答案>>
已知:C(s)+
| 1 |
| 2 |
Mg(g)+
| 1 |
| 2 |
(1)一种制备镁的反应为:MgO(s)+C(s)=Mg(g)+CO(g),该反应的△H=
(2)一种用水氯镁石(主要成分为MgCl2?6H2O)制备金属镁工艺的关键流程如下:

①为探究MgCl2?6H2O“一段脱水”的合理温度范围,某科研小组将MgCl2?6H2O在不同温度下分解,测得残留固体物质的X-射线衍射谱图如图所示(X-射线衍射可用于判断某晶态物质是否存在).

测得E中Mg元素质量分数为60.0%,则E的化学式为
②若电解时电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低点解效率,生成MgO的化学方程式为
③该工艺,可以循环使用的物质有
(3)Mg2Ni是一中储氢材料,2.14g Mg2Ni在一定条件下能吸收0.896L H2(标准状况下)生成X,X的化学式为

下表为元素周期表的一部分,a、b、c…为部分元素.回答下列问题:
(1)请写出h元素的价电子排布图
 ;
;
(2)ya3分子的电子式是
 ,其分子的空间构型是
,其分子的空间构型是
(3)请写出上述元素d3+的核外电子排布式
(4)请比较b、e、j三种元素的第一电离能由大到小的顺序
查看习题详情和答案>>
| a | |||||||||||||||||
| f | y | h | i | ||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | l | ||||||||||||||


(2)ya3分子的电子式是


三角锥形
三角锥形
,分子中y原子的杂化轨道类型是sp3杂化
sp3杂化
,g2+可以与ya3 以配位
配位
键形成[g(ya3)4]2+离子;(3)请写出上述元素d3+的核外电子排布式
ls22s22p63s23p63d5
ls22s22p63s23p63d5
,实验室常用形成一种红色配离子的方法检验该离子,该反应的离子方程式为Fe3++3SCN-=Fe(SCN)3
Fe3++3SCN-=Fe(SCN)3
.(4)请比较b、e、j三种元素的第一电离能由大到小的顺序
Cl>Mg>Al
Cl>Mg>Al
(写元素符号),其原因是同一周期,随着原子序数的增加,元素的第一电离能呈现增大的趋势.但镁元素的最外层电子达到全充满的稳定结构,其第一电离能大于铝元素
同一周期,随着原子序数的增加,元素的第一电离能呈现增大的趋势.但镁元素的最外层电子达到全充满的稳定结构,其第一电离能大于铝元素
.(2000?上海)铜镁合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mL的N2O4气体(都已折成标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为( )
(Cu、Mg、O、H的相对原子质量分别为:64、24、16、1)
(Cu、Mg、O、H的相对原子质量分别为:64、24、16、1)
查看习题详情和答案>>
由菱镁矿(主要成分为MgCO3)制阻燃型氢氧化镁的工艺流程如下:
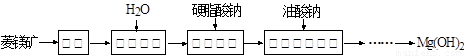
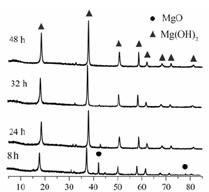
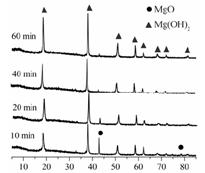


(1)从图可以得出的结论为 、 。
(2)水化反应MgO+H2O = Mg(OH)2能自发进行的原因是 。
(3)结合元素周期律和表1可知,金属氢氧化物受热分解的规律有 。(写一条即可)
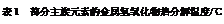
|
LiOH |
NaOH |
KOH |
Al(OH)3 |
Mg(OH)2 |
Ca(OH)2 |
Ba(OH)2 |
|
924 |
不分解 |
不分解 |
140 |
258 |
390 |
700 |
(4)已知热化学方程式:Mg(OH)2 (s) =" MgO" (s)+H2O (g) ΔH =" 81.5" kJ·mol-1
①Mg(OH)2起阻燃作用的主要原因是 。
②与常用卤系(如四溴乙烷)和有机磷系(磷酸三苯酯)阻燃剂相比,Mg(OH)2阻燃剂的优点是 。
查看习题详情和答案>>