摘要:4.(1)①,③,③,④ Cu2(OH)2CO3 2CuO+H2O+CO2↑ C+2CuO 2Cu+CO2↑ (2)②Fe2O3+3CO 2Fe+3CO2↑. WO3+3H2 W+3H2O, ③3MnO2+4Al 3Mn+2 Al2O3 ④2NaCl 2Na + C12↑ 讲析: 4种方法有一个共同点.都是从金属化合物 里把金属还原出来.焦炭.氢气.一氧化碳是常使用的还原剂.方法①.②一般冶炼不活泼或较活泼的金属.如铜.铁等.活泼金属置换法.一般在水溶液中进行.也可以是粉末状.在工业上利用铝热反应.用铝作还原剂冶炼难溶的金属.如钒.铬.锰等.活泼的金属一般采用电解的方法.电解熔融的氯化钠.氯化镁.氧化铝制取钠.镁.铝. (Ⅰ)孔雀石的主要成分是Cu2(OH)2CO3.加热分解: Cu2(OH)2CO3 2CuO+H2O+CO2↑ 火烧时.使用的树木变为木炭.CuO再与木炭反应.产生铜.属于焦炭法. C+2CuO 2Cu+CO2↑ 符合① (Ⅱ)湿法炼铜是我国西汉时期用铁从某些含铜化合物的溶液中置换出铜.属活泼金属置换法. Fe+CuSO4=Fe SO4+Cu 适合于③ (Ⅲ)是使铝粉和Cr2O3的混合物在高温下反应.置换出铬.反应产生的热量使铬熔化而分离. 2Al+ Cr2O3 Al2O3 +2Cr 适合于③ (Ⅳ)从光卤石(KCl·MgCl2·6H2O)中可得到六水合氯化镁晶体.再采用通电分解熔融的氯化镁的方法制取镁. MgCl2 Mg + C12↑ 符合④ 新活题网站
网址:http://m.1010jiajiao.com/timu_id_3778403[举报]
 (2012?江苏三模)卤素性质活泼,能形成卤化物、多卤化物等多种类型的化合物.
(2012?江苏三模)卤素性质活泼,能形成卤化物、多卤化物等多种类型的化合物.(1)卤化氢中,HF的沸点高于HCl,原因是
HF分子间形成氢键
HF分子间形成氢键
.(2)如图所示为F-与Mg2+、K+形成的某种离子晶体的晶胞,其中“O”表示的离子是
F-
F-
(填离子符号).(3)多卤化物Rb[ICl2]分解时生成晶格能相对较大的铷(Rb)的卤化物,则该卤化物的化学式为
RbCl
RbCl
.(4)BF3与NH3,能发生反应生成X(H3BNF3),X的结构式为


sp3
sp3
.(5)有一类物质的性质与卤素类似,称为“拟卤素”[如(SCN)2、(CN)2等].(CN)2的结构式为N≡C-C≡N,该分子中σ键和π键数目之比为
3:4
3:4
.现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子.
请回答下列问题(题中的字母只代表元素代号,与实际元素符号无关):
(1)A~F六种元素原子,原子半径最大的是
(2)A、C、D三种元素组成的一种常见化合物,是重要的工业产品,该化合物电子式为: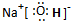
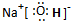 .
.
(3)B与F两种元素形成的一种化合物分子,各原子均达八电子结构,其中B显负价,F显正价,则该化合物水解的主要产物是:
(4)A、C、E三种元素形成的一种常见化合物,其浓溶液在加热条件下可与铜反应,该反应的化学方程式为
查看习题详情和答案>>
请回答下列问题(题中的字母只代表元素代号,与实际元素符号无关):
(1)A~F六种元素原子,原子半径最大的是
D
D
(填序号).(2)A、C、D三种元素组成的一种常见化合物,是重要的工业产品,该化合物电子式为:
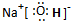
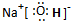
(3)B与F两种元素形成的一种化合物分子,各原子均达八电子结构,其中B显负价,F显正价,则该化合物水解的主要产物是:
HClO和NH3(NH3?H2O)
HClO和NH3(NH3?H2O)
.(4)A、C、E三种元素形成的一种常见化合物,其浓溶液在加热条件下可与铜反应,该反应的化学方程式为
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
 如图表示在没有通风橱的条件下制备氯气时设计的装置,图中a、b是可控制的弹簧铁夹.(氯气在饱和氯化钠溶液中的溶解度较小.)
如图表示在没有通风橱的条件下制备氯气时设计的装置,图中a、b是可控制的弹簧铁夹.(氯气在饱和氯化钠溶液中的溶解度较小.)(1)仪器A的名称是
分液漏斗
分液漏斗
;水槽中应盛放的是饱和食盐水
饱和食盐水
;烧杯中盛放的是氢氧化钠溶液
氢氧化钠溶液
;烧瓶中反应的化学方程式MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
;
| ||
(2)在收集氯气时,应
关闭b,打开a
关闭b,打开a
.当氯气收集完毕时应关闭a,打开b
关闭a,打开b
.(填如何控制a、b)(2012?江苏三模)合理地固定和利用CO2能有效减少空气中的温室气体,产物还能造福人类.
(1)11km深海底的无脊椎动物依靠化学自养菌,以海底热泉喷出液中的H2S和CO2合成(C6H10O5)n和一种淡黄色固体,该反应的化学方程式为
(2)CO2可用于合成二甲醚(CH3OCH3),有关反应的热化学方程式为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1
2CH3OH(g)?H3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1
①反应2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)的△H=
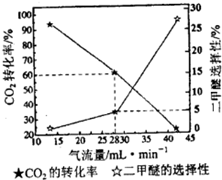
②一定条件下用CO2和H2合成二甲醚,反应物气流量对CO2的转化率、二甲醚选择性的影响结果如下图所示.控制气流量为28mL?min-1,生产0.3mol二甲醚需通入CO2的物质的量为
③反应2CH3OH(g)?CH3OCH3(g)+H2O(g)在T℃时的平衡常数为400.该温度下,在密闭容器中加入CH3OH,t时刻时,测得c(CH3OH)=0.03mol?L -1,c(CH3OCH3)=0.6mol?L -1,此时v正
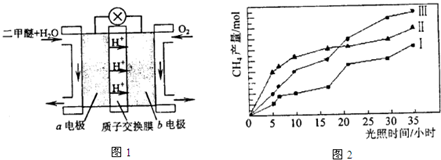
④二甲醚燃料电池的工作原理如图1所示.该电池工作时,a电极的反应式为
(3)一种“碳捕捉”技术为:将含CO2的工业尾气通过NaOH溶液,在所得溶液中加CaO,充分反应后过滤,滤渣高温分解得到的高浓度CO2可用于制备甲醇等.该技术电可以循环使用的物质为
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,等量的CO2和H2O(g)在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图2所示.在0~30小时内,CH4的半均生成速率v(Ⅰ)、v(Ⅱ)、和v(Ⅲ)、从大到小的顺序为
查看习题详情和答案>>
(1)11km深海底的无脊椎动物依靠化学自养菌,以海底热泉喷出液中的H2S和CO2合成(C6H10O5)n和一种淡黄色固体,该反应的化学方程式为
12nH2S+6nCO2=C6H10O5)n+12nS↓+7nH2O
12nH2S+6nCO2=C6H10O5)n+12nS↓+7nH2O
.(2)CO2可用于合成二甲醚(CH3OCH3),有关反应的热化学方程式为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1
2CH3OH(g)?H3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1
①反应2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)的△H=
-121.5kJ/mol
-121.5kJ/mol
.②一定条件下用CO2和H2合成二甲醚,反应物气流量对CO2的转化率、二甲醚选择性的影响结果如下图所示.控制气流量为28mL?min-1,生产0.3mol二甲醚需通入CO2的物质的量为
20mol
20mol
.
③反应2CH3OH(g)?CH3OCH3(g)+H2O(g)在T℃时的平衡常数为400.该温度下,在密闭容器中加入CH3OH,t时刻时,测得c(CH3OH)=0.03mol?L -1,c(CH3OCH3)=0.6mol?L -1,此时v正
=
=
v逆(填“>”、“<”或“等于”)④二甲醚燃料电池的工作原理如图1所示.该电池工作时,a电极的反应式为
CH3OCH3+3H2O-12e-=2CO2+12H+
CH3OCH3+3H2O-12e-=2CO2+12H+
.(3)一种“碳捕捉”技术为:将含CO2的工业尾气通过NaOH溶液,在所得溶液中加CaO,充分反应后过滤,滤渣高温分解得到的高浓度CO2可用于制备甲醇等.该技术电可以循环使用的物质为
氧化钙和氢氧化钠
氧化钙和氢氧化钠
.(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,等量的CO2和H2O(g)在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图2所示.在0~30小时内,CH4的半均生成速率v(Ⅰ)、v(Ⅱ)、和v(Ⅲ)、从大到小的顺序为
v(Ⅲ)>v(Ⅱ)>v(Ⅰ)
v(Ⅲ)>v(Ⅱ)>v(Ⅰ)
.