网址:http://m.1010jiajiao.com/timu_id_3778380[举报]
某同学在学习硝酸与硫酸时,对两种酸与铜的反应情况进行研究,试完成下列各题。
(1)在甲、乙两个烧杯中,分别装入40mL浓度均为2mol·L-1的稀硫酸和稀硝酸,并向其中各加入 4g束状铜丝,观察现象,试完成下列实验报告:

(2)充分反应后,将甲、乙烧杯混合,再使之充分反应,最终所得溶液溶质为____ ,剩余固体总质量为 g
(3)若甲中硫酸溶液体积V(V>40mL)可变,其余数据不变,则:
①当甲、乙烧杯混合充分反应后,溶液中只有一种溶质时,V=____ mL,若要将溶液中的Cu2+沉淀完全,应加NaOH使溶液的pH至少为____
。已知KsP[Cu(OH)2]=2.2×l0-20,1g  =0.7)
=0.7)
②能否通过硫酸溶液体积的改变,使铜丝在甲、乙烧杯混合充分反应后完全溶解? 试写出推理过程________ 。
查看习题详情和答案>>
小明等同学为了探究酸、碱、盐溶液的导电性,设计了如下实验:
1.在5只250mL烧杯分别加入浓度均为0.1mol·L-1的盐酸、CH3COOH溶液、NaOH溶液、NaCl溶液、氨水各150mL。
2.在5种溶液中分别放入相同规格的石墨电极,按下图连接好。

3.接通电源,仔细观察现象。
现象1:五个灯泡都亮起来。
结论: 。
现象2:盐酸、氯化钠、氢氧化钠溶液对应的灯泡较亮,醋酸、氨水对应的灯泡较暗。
结论: 。
思考:
1.酸、碱、盐溶液导电与金属导电的原理是否相同,为什么?
2.同学们为了探究不同电解质之间电离能力的差异,设计了上述实验,通过观察灯泡的明亮程度,判断电解质的电离能力大小,为此必须控制其他能影响灯泡亮度的一些因素,使之保持一致,从而不影响灯泡的明亮程度。在本实验中,采取了哪些主要措施来控制其他因素对灯泡亮度的影响?(写出三条即可) 。
3.小明同学根据现象2得出一个结论:氯化氢、氯化钠、氢氧化钠是强电解质,醋酸、一水合氨是弱电解质。你同意他这个观点吗?为什么?
。
4.为了进一步探究氯化氢等化合物是强电解质,小红同学在老师的帮助下测定了0.1mol·L-1的盐酸中的氢离子浓度,通过对结果的分析,即可得出结论。说明氯化氢是强电解质的理由是:测得溶液中的氢离子浓度 0.1mol·L-1(选填>、<、=)。
5.同学们在实验的基础上,进一步查阅资料得知:一般来说, 是强电解质, 是弱电解质。根据以上结论推测:如果将上述实验中的醋酸和氨水混匀,然后分别盛放在原来的烧杯中。接通电源,可以观察到的现象是:
A.与混合前无任何区别。
B.5只灯泡都亮起来,亮度完全相同。
C.只有盐酸、氯化钠、氢氧化钠溶液对应的灯泡亮起来,另外两只不亮。
D.5个灯泡都亮起来,盐酸、氯化钠、氢氧化钠溶液对应的灯泡较亮,另外两只略暗,但明显比混合前明亮。
查看习题详情和答案>>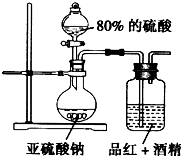 某研究性学习小组的同学决定通过实验探究SO2的漂白性是SO2本身具有的还是SO2与水作用的产物具有的,他们查阅资料知品红能溶解在酒精中形成红色溶液.
某研究性学习小组的同学决定通过实验探究SO2的漂白性是SO2本身具有的还是SO2与水作用的产物具有的,他们查阅资料知品红能溶解在酒精中形成红色溶液.(1)甲同学设计了如图所示的装置,并认为由广口瓶中溶液颜色的变化可以达到实验目的,甲作出此判断的依据是
(2)乙同学通过分析指出甲同学的装置图有两处不合理,并进行了修改,修改的内容:
按修改后的装置,实验中控制SO2以大约每分钟200个气泡的速率通过品红的酒精溶液,20分钟后溶液仍不褪色,由此知,品红的褪色不是
假设一:是HSO
- 3 |
假设二:是SO
2- 3 |
假设三:
(3)为验证自己的假设,乙同学进行了如下实验:取2mL相同浓度的品红的酒精溶液置于两支试管中,再向试管中分别加入少量Na2SO3、NaHSO3固体,振荡静置后发现试管中的液体均褪色,对此他们得出使品红褪色的粒子是HSO
- 3 |
2- 3 |
(4)为了进一步进行探究,丙同学又做了如下实验:取相同浓度的品红的酒精溶液各10mL分别置于两个小烧杯中,向两个烧杯中同时一次陛性地加久10mL 0.1mol/L Na2SO3、10mL 0.1mol/LNaHSO3溶液,发现加入Na2SO3溶液的褪色较快.对此他可以得出的结论是
A、B、C三种强电解质,它们在水中电离出的离子为Na+ 、Ag+ 、NO3- 、SO42- 、 Cl-,在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了10.8克。常温下各烧杯中溶液的pH与电解时间t的关系如图所示。据此回答下列问题:

(1)M为电源的_______极(填写“正”或“负”),甲、乙两个烧杯中的电解质分别为_______、_______(填写化学式)。
(2)计算电极f上生成的气体为_______mol。
(3)写出乙烧杯中的电解反应方程式: ________________________________。
(4)若电解后甲溶液的体积为10L,则该溶液的pH为___________ 。
(5)要使丙恢复到原来的状态,应加入适量的 (填写化学式)。
查看习题详情和答案>>
A、B、C三种强电解质,它们在水中电离出的离子为Na+、Ag+、NO、SO、Cl-,在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了10.8克。常温下各烧杯中溶液的pH与电解时间t的关系如图所示。据此回答下列问题:

(1)M为电源的 极(填写“正”或“负”),甲、乙两个烧杯中的电解质分别为 、 (填写化学式)。
(2)计算电极f上生成的气体为 mol。
(3)写出乙烧杯中的电解反应方程式: 。
(4)若电解后甲溶液的体积为10L,则该溶液的pH为 。
(5)要使丙恢复到原来的状态,应加入适量的 (填写化学式)。
查看习题详情和答案>>