网址:http://m.1010jiajiao.com/timu_id_3778133[举报]
| 实验序号 | 实验内容 | 实验结果 |
| ① | 加足量NaOH溶液并加热 | 收集到气体2.24L(已折算成标准状况下的体积) |
| ② | 加足量BaC12溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后过滤、洗涤、干燥、称量 | 第一次称量读数为12.54g,第二次称量读数为4.66g |
(1)该混合物中一定不存在的离子是
(2)试写出实验①发生反应的离子方程式
| ||
| ||
(3)溶液中一定存在的阴离子及其物质的量浓度(可不填满):
| 阴离子符号 | 物质的量浓度(mol?L-1) |
SO42- SO42- |
0.1 0.1 |
CO32- CO32- |
0.2 0.2 |
无 无 |
无 无 |
某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A==H++HA- HA- H++A2- 完成以下问题:
H++A2- 完成以下问题:
(1)Na2A溶液显______(填“酸性”“中性”或“碱性”),理由是________________(用离子方程式表示)。
(2)已知0.1 mol·L-1的NaHA溶液pH=2,则0.1 mol·L-1的H2A溶液中氢离子的物质的量浓度_______0.11 mol·L-1(填“>”“=”或“<”)。
(3)锅炉水垢中的CaSO4,可用Na2CO3溶液处理,转化为CaCO3,而后用酸除去。过程中发生:CaSO4(1)+
CO32- CaCO3(1)+ SO42-,已知298K时,Ksp[CaCO3]=2.80×10-9,Ksp[CaSO4]=4.90×10-5,求此温度下该反应的平衡常数K= (计算结果保留三位有效数字)
CaCO3(1)+ SO42-,已知298K时,Ksp[CaCO3]=2.80×10-9,Ksp[CaSO4]=4.90×10-5,求此温度下该反应的平衡常数K= (计算结果保留三位有效数字)
查看习题详情和答案>>
某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A==H++HA- HA- H++A2- 完成以下问题:
H++A2- 完成以下问题:
(1)Na2A溶液显______(填“酸性”“中性”或“碱性”),理由是________________(用离子方程式表示)。
(2)已知0.1 mol·L-1的NaHA溶液pH=2,则0.1 mol·L-1的H2A溶液中氢离子的物质的量浓度_______0.11 mol·L-1(填“>”“=”或“<”)。
(3)锅炉水垢中的CaSO4,可用Na2CO3溶液处理,转化为CaCO3,而后用酸除去。过程中发生:CaSO4(1)+ CO32- CaCO3(1)+ SO42-,已知298K时,Ksp[CaCO3]=2.80×10-9,Ksp[CaSO4]=4.90×10-5,求此温度下该反应的平衡常数K= (计算结果保留三位有效数字)
CaCO3(1)+ SO42-,已知298K时,Ksp[CaCO3]=2.80×10-9,Ksp[CaSO4]=4.90×10-5,求此温度下该反应的平衡常数K= (计算结果保留三位有效数字)
(1)某同学通过分析,认为无需检验就可判断其中必有的两种物质是
(2)为了确定X,现将(1)中的两种物质记为A和B,含X的物质记C,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时也产生红褐色沉淀,向该沉淀中滴入稀硝酸沉淀部分溶解,最后留有白色沉淀不再溶解.则X为
A.SO32-B.SO42-C.CH3COO-D.SiO32-
(3)B的水溶液显
(4)将0.02molA与0.01molC同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的物质的量为
(5)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.则物质D一定含有上述离子中的
(6)利用上述已经确定的物质,可以检验出D、E中的阳离子.请简述实验操作步骤、现象及结论
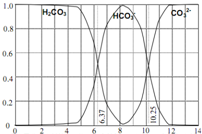 如图是一水溶液在pH从0至14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成百分率,下列叙述正确的是( )
如图是一水溶液在pH从0至14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成百分率,下列叙述正确的是( )