摘要:16.17.5 mol·L-1 讲析:溶液稀释到500 mL.再加入足量锌粉.收集到标准状况下气体2.24 L.这是H2.参加反应的硫酸为0.1 mol.用于产生H2的Zn为0.1 mol.固体质量减轻了6.5 g.还有1g的质量差是因为Zn与硫酸铜溶液发生了置换反应.由Zn→Cu.利用差量法可求得这一不参加反应的Zn为1 mol.生成的Cu为1 mol.即与浓硫酸反应的Cu为1 mol.参加反应的硫酸为2 mol.这样硫酸共2.1 mol.则原硫酸的物质的量浓度为17.5 mol·L-1.
网址:http://m.1010jiajiao.com/timu_id_3777821[举报]
 下列物质 ①Cu ②液态SO2 ③纯醋酸 ④NaHCO3 ⑤Ba(OH)2溶液
下列物质 ①Cu ②液态SO2 ③纯醋酸 ④NaHCO3 ⑤Ba(OH)2溶液I、属于非电解质的是
②
②
;(填序号)Ⅱ、(1)NaHCO3是一种
强
强
(填“强”或“弱”)电解质;(2)写出HCO3-水解的离子方程式:
HCO3-+H2O?H2CO3+OH-
HCO3-+H2O?H2CO3+OH-
;(3)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH- 五种微粒的浓度由大到小的顺序为:
c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-)
c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-)
.(4)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol?L-1.若忽略水的电离及H2CO3的第二级电离,则H2CO3?HCO3-+H+的平衡常数K1=
4.17×10-7(mol?L-1)
4.17×10-7(mol?L-1)
.(已知:10-5.60=2.5×10-6)Ⅲ、Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液.
(1)该Ba(OH)2溶液的物质的量浓度为
0.05mol?L-1
0.05mol?L-1
;(2)溶液中由水电离出c(OH-)=
10-13mol?L-1
10-13mol?L-1
;(3)与某浓度盐酸溶液按体积比(碱与酸之比)1:9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=
2
2
.Ⅳ、醋酸是一种弱电解质.某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如右图所示.则图
Ⅱ
Ⅱ
(填“I”或“Ⅱ”)为醋酸稀释的图象.利用染化厂的废料铁泥(主要成分是Fe2O3、FeO和铁)制备可用于隐形飞机涂层的纳米四氧化三铁的生产流程为图1:
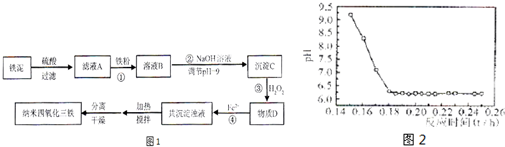
请回答:
(1)过程①主要反应的离子方程式为
(2)已知氢氧化亚铁的Ksp=4.87×10-17,氢氧化铁的Ksp=2.6×10-39.当溶液中某离子浓度不高于1×10-5 mol?L-1时,可以认为该离子已经完全沉淀.通过计算所得数据说明过程②调节pH=9的原因是
(3)物质D的主要产物中铁、氢、氧三种元素的质量比为56:1:32,则过程③主要反应的化学方程式为
(4)已知Fe2+在弱碱性溶液中还原性较强,图2是研究过程④的实验所得,则该反应所需的时间控制在
(5)某工厂处理废铁泥(测得铁元素含量为16.8%)的能力为10吨/小时,生产纳米四氧化三铁的产量为4.64吨/小时.如不考虑过程④以后生产中Fe2+的氧化,则该工厂每小时消耗铁粉的质量为
查看习题详情和答案>>

请回答:
(1)过程①主要反应的离子方程式为
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.(2)已知氢氧化亚铁的Ksp=4.87×10-17,氢氧化铁的Ksp=2.6×10-39.当溶液中某离子浓度不高于1×10-5 mol?L-1时,可以认为该离子已经完全沉淀.通过计算所得数据说明过程②调节pH=9的原因是
当pH=9时,Fe2+的浓度为5×10-5mol?L-1,已完全沉淀
当pH=9时,Fe2+的浓度为5×10-5mol?L-1,已完全沉淀
.(3)物质D的主要产物中铁、氢、氧三种元素的质量比为56:1:32,则过程③主要反应的化学方程式为
2Fe(OH)2+H2O2=2FeO(OH)+2H2O
2Fe(OH)2+H2O2=2FeO(OH)+2H2O
.(4)已知Fe2+在弱碱性溶液中还原性较强,图2是研究过程④的实验所得,则该反应所需的时间控制在
0.16
0.16
小时左右,较为适宜.(5)某工厂处理废铁泥(测得铁元素含量为16.8%)的能力为10吨/小时,生产纳米四氧化三铁的产量为4.64吨/小时.如不考虑过程④以后生产中Fe2+的氧化,则该工厂每小时消耗铁粉的质量为
560
560
千克.3g镁铝合金与100mL 稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到无水硫酸盐17.4g,则原硫酸的物质的量浓度为( )
| A、1 mol?L-1 | B、1.5 mol?L-1 | C、2 mol?L-1 | D、2.5 mol?L-1 |
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是
A.蔗糖 B.熔融硫酸钾 C.高锰酸钾溶液 D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为
mol/L.(只要求用原始数据写表达式,不需要化简与计算)
(3)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、托盘天平、
(4)使用容量瓶前必须进行的一步操作是
(5)在溶液配制过程中,下列操作对配制结果会产生什么影响(请填“偏高”或“偏低”或“无影响”)
A.定容时仰视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
查看习题详情和答案>>
| 成分 | 质量(g) | 摩尔质量(g?mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.25 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.25 | 158 |
| 硝酸银 | 0.02 | 170 |
A
A
.A.蔗糖 B.熔融硫酸钾 C.高锰酸钾溶液 D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为
| ||||
| 0.5 |
| ||||
| 0.5 |
(3)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、托盘天平、
胶头滴管
胶头滴管
、500mL容量瓶
500mL容量瓶
.(在横线上填写所缺仪器的名称)(4)使用容量瓶前必须进行的一步操作是
检查容量瓶是否漏水
检查容量瓶是否漏水
.(5)在溶液配制过程中,下列操作对配制结果会产生什么影响(请填“偏高”或“偏低”或“无影响”)
A.定容时仰视容量瓶刻度线
偏低
偏低
B.容量瓶在使用前未干燥,里面有少量蒸馏水
无影响
无影响
C.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
偏低
偏低
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
无影响
无影响
. (2011?惠州模拟)铁、铜都是人类最早使用的金属,它们的单质及化合物应用非常广泛.
(2011?惠州模拟)铁、铜都是人类最早使用的金属,它们的单质及化合物应用非常广泛.(1)钢铁“发蓝,,是将钢铁制品浸到某些氧化性溶液中,使其表面形成一层四氧化三铁的过程.其中有一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热至1300C,反应过程为:
I.3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
II.6Na2FeO2+NaNO2+5H2O=3Na2Fe2O4+NH3↑十+7NaOH
Ⅲ.Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH
①反应II中的氧化剂是
NaNO2
NaNO2
.②上述过程产生了大量NH3,有关NH3处理方案合理的是
ac
ac
a.用H2SO4吸收制氮肥 b. 高空排放 C.用于制备HNO3
(2)工业上常用氯化铁溶液腐蚀铜制电路板.
①请根据金属活动顺序及反应原理,判断Cu2+、Fe3+、Fe2+的氧化性强弱顺序:
Fe3+>Cu2++>Fe2+
Fe3+>Cu2++>Fe2+
.②请设计实验验证Cu2+、Fe3+氧化性强弱的结论.实验方案及现象为:
将铜棒与碳棒用导线连接(带电流表),再插入氯化铁溶液,发现有电流产生
将铜棒与碳棒用导线连接(带电流表),再插入氯化铁溶液,发现有电流产生
.(3)如图横坐标为溶液pH,纵坐标为金属离子物质的量浓度的对数值(当溶液中金属离子浓度≤10-5 mol?L-1时,可认为沉淀完全),试回答:
①腐蚀铜板后的溶液中,若Cu2+、Fe3+和Fe2+浓度均为0.1mol?L-1,今向混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为
Cu2+、Fe2+
Cu2+、Fe2+
.②从图中数据计算可得Fe(OH)2的溶度积Ksp[Fe(OH)2]=
1.0×10-17(mol?L-1)3
1.0×10-17(mol?L-1)3
.