摘要:3.浓盐酸具有强挥发性.产生的HCl在空气中形成白雾.浓盐酸中滴入浓硫酸时.因浓硫酸具有吸水性而使盐酸浓度增加.同时浓硫酸吸水放热.促进了HCl的挥发.4.运用差量法解题比较简捷. 5.煤燃烧产生大量的C02.排放到空气中会产生温室效应. 6.消除污染的方法是采取无污染的生产工艺. 7.少用煤作燃料.燃料脱硫.开发新能源可以减少SO2的产生.从而减少酸雨的产生. 8.C02无毒不过会产生温室效应而已. 9.浓硫酸与胆矾晶体混合振荡.晶体颜色变浅.说明浓硫酸具有吸水性,常温下.浓硫酸可以用铝质容器贮存.不是铝与浓硫酸不反应而是产生钝化现象.反应停止而已. 10.O3 在高空可吸收紫外光.而在低空因具有强氧化性具有危害. 11.光化学烟雾由氮的氧化物和烃类引起的. 12.溶液的pH=7.溶液中只有Na2SO4.A正确,若无H2SO4.沉淀只有Cu(OH)2.其物质的量为a/2mol.B正确.
网址:http://m.1010jiajiao.com/timu_id_3777817[举报]
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.Ⅰ(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
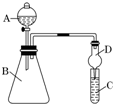
Ⅱ.利用图装置可验证同主族元素非金属性的变化规律
(3)仪器B的名称为
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液
(2009?安徽模拟)某化学研究性学习小组为探究元素性质的变化规律,设计了如下实验:
(1)甲同学根据同周期元素原子结构的变化规律,预测出同一周期,从左至右元素的金属性逐渐减弱.请你根据实验室常用试剂和仪器帮助甲同学设计实验,简述实验步骤和现象(以第三周期元素为例):
(2)乙同学欲比较N、C、Si的非金属性强弱,设计了图1所示的实验装置,其能否达到实验目的
(3)丙同学从资料中获悉:元素周期表中处于象硼与硅这样“对角线”位置的某些元素性质相似.预测金属铍应该具有与
(4)丁同学设计了如图2装置验证元素性质递变规律.A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.丁同学可能观察到的现象有

查看习题详情和答案>>
(1)甲同学根据同周期元素原子结构的变化规律,预测出同一周期,从左至右元素的金属性逐渐减弱.请你根据实验室常用试剂和仪器帮助甲同学设计实验,简述实验步骤和现象(以第三周期元素为例):
分别取钠、镁、铝小粒分别与冷水反应,钠剧烈反应,镁和铝无明显现象;另取镁、铝小粒分别与等浓度的盐酸反应,镁比铝反应剧烈
分别取钠、镁、铝小粒分别与冷水反应,钠剧烈反应,镁和铝无明显现象;另取镁、铝小粒分别与等浓度的盐酸反应,镁比铝反应剧烈
.(2)乙同学欲比较N、C、Si的非金属性强弱,设计了图1所示的实验装置,其能否达到实验目的
能
能
(填“能”或“不能”),设计的理论依据是元素的非金属性越强,其最高价氧化物的水合物酸性越强
元素的非金属性越强,其最高价氧化物的水合物酸性越强
. 但也有同学根据硝酸具有挥发性,认为乙同学的实验装置存在不足,请你帮助该同学提出修改意见在两导管之间连接一个装有饱和碳酸钠的洗气瓶
在两导管之间连接一个装有饱和碳酸钠的洗气瓶
.(3)丙同学从资料中获悉:元素周期表中处于象硼与硅这样“对角线”位置的某些元素性质相似.预测金属铍应该具有与
铝
铝
相似的性质,能证明其预测的实验方案是铍单质分别与酸和强碱反应,看反应现象
铍单质分别与酸和强碱反应,看反应现象
.(4)丁同学设计了如图2装置验证元素性质递变规律.A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.丁同学可能观察到的现象有
A:白色变成黄色或橙黄色;B:变蓝色;C:红纸褪色
A:白色变成黄色或橙黄色;B:变蓝色;C:红纸褪色
. 从环保角度考虑,该装置有明显不足,请指出并提出改进建议尾气排入空气污染环境,应在试管口处放一团浸有氢氧化钠溶液的棉花
尾气排入空气污染环境,应在试管口处放一团浸有氢氧化钠溶液的棉花
.
已知气体的相对分子质量越小,扩散速度越快。浓硫酸没有挥发性,浓氨水和浓盐酸都具有很强的挥发性,浓氨水会挥发出氨气,浓盐酸会挥发出氯化氢。下图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的是 ( )。
| A.甲是浓氨水,乙是浓硫酸 |
| B.甲是浓盐酸,乙是浓氨水 |
| C.甲是浓氨水,乙是浓盐酸 |
| D.甲是浓硫酸,乙是浓氨水 |
