摘要:C;2.C; 3.B; 4.B.C; 5.C; 6.D; 7.C 讲析:1.臭氧氧化有机色素.不是吸附作用.2.减压蒸馏可防止过氧化氢分解.3.随着核电荷数的递增.元素的非金属性逐渐减弱.而不是增强. 4.由同素异形体的定义进行辨析.5.根据元素周期表的有关知识可知:.116号元素应为第7周期ⅥA族.再由氧族元素的递变性进行分析.6.5种物质全有漂白作用.但原理不全部一样.Cl2.Na2O2.Ca(ClO)2因氧化而漂白.活性炭具有吸附作用而SO2是与有色物质化合.7.A.D选项体现SO2的还原性.B选项是SO2与碱性溶液作用是溶液碱性减弱而褪色.
网址:http://m.1010jiajiao.com/timu_id_3777755[举报]
A、B、C、D、E是原子序数依次增大的五种短周期元素,A的某种核素不含中子,B、E同主族,且E的L层电子数是K层和M层电子数之和,C是所有短周期元素中半径最大的元素、C、D、E三种元素的最高价氧化物对应水化物两两之间均可反应.试解答下列问题:
(1)B元素的简单离子的结构示意简图为
 .
.
(2)A、D、E元素的名称分别为
(3)E元素在周期表中的位置是第
(4)五种元素的简单离子半径从大到小的顺序是
(5)五种元素中,得电子能力最强的是
查看习题详情和答案>>
(1)B元素的简单离子的结构示意简图为


(2)A、D、E元素的名称分别为
氢
氢
、硫
硫
、铝
铝
.(3)E元素在周期表中的位置是第
三
三
周期ⅥA
ⅥA
族.(4)五种元素的简单离子半径从大到小的顺序是
S2->O2->Na+>Al3+>H+
S2->O2->Na+>Al3+>H+
(用元素离子符号填写).(5)五种元素中,得电子能力最强的是
O
O
,失电子能力最强的是Na
Na
(填元素符号).A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中A、D及C、F分别是同主族元素.A、F两元素的原子核中质子数之和比C、D两元素的原子核中质子数之和少2.F元素的最外层电子数是其次外层电子数的
.又知B元素的最外层电子数是内层电子数的2倍.E元素的最外层电子数等于其电子层数.请回答:
(1)写出元素A和B形成的直线型非极性分子的电子式:
 .
.
(2)已知:泡沫灭火器的工作原理是含有A、B、C、D四种元素形成的化合物X和含有C、E、F三种元素形成的Y的水溶液间的反应,写出该反应的离子方程式:
(3)工业上制备单质E,是通过电解C和E形成的化合物;写出阴极上的电极反应式:
(4)1mol由E、F两种元素组成的化合物跟由A、C、D三种元素组成的化合物的溶液恰好完全反应,则消耗后者化合物的物质的量为
(5)含有溶质为DAB2C4的水溶液显酸性的原因是
(6)若G是周期表中第四周期第Ⅷ族的金属元素,其最高价氧化物与单质E反应的化学方程式是
查看习题详情和答案>>
| 3 |
| 4 |
(1)写出元素A和B形成的直线型非极性分子的电子式:


(2)已知:泡沫灭火器的工作原理是含有A、B、C、D四种元素形成的化合物X和含有C、E、F三种元素形成的Y的水溶液间的反应,写出该反应的离子方程式:
3HCO3-+Al3+═3CO2↑+Al(OH)3↓
3HCO3-+Al3+═3CO2↑+Al(OH)3↓
.(3)工业上制备单质E,是通过电解C和E形成的化合物;写出阴极上的电极反应式:
Al3++3e-═Al
Al3++3e-═Al
.(4)1mol由E、F两种元素组成的化合物跟由A、C、D三种元素组成的化合物的溶液恰好完全反应,则消耗后者化合物的物质的量为
8
8
mol.(5)含有溶质为DAB2C4的水溶液显酸性的原因是
HC2O4-的电离大于水解
HC2O4-的电离大于水解
.(6)若G是周期表中第四周期第Ⅷ族的金属元素,其最高价氧化物与单质E反应的化学方程式是
2Al+Fe2O3
Al2O3+2Fe
| ||
2Al+Fe2O3
Al2O3+2Fe
.
| ||
A、B、C、D、E、F六种元素,其中A、B、C、D、E为短周期主族元素.它们之间的关系如下:
Ⅰ.原子半径:A<C<B<E<D
Ⅱ.原子的最外层电子数:A=D C=E A+B=C
Ⅲ.原子的核外电子层数:B=C=2A
Ⅳ.B元素的主要化合价:最高正价+最低负价=2
请回答:
(1)甲为由A、B两种元素组成的常见气体,写出其电子式
 ;乙为由B元素组成的单质,写出该单质的一种用途
;乙为由B元素组成的单质,写出该单质的一种用途
(2)写出某黑色含F的磁性氧化物在E的最高价氧化物对应水化物的稀溶液中反应的离子方程式:
(3)向A、B、C三种元素组成的某盐溶液中滴加AgNO3溶液生成白色沉淀,该反应的化学方程式为
(4)写出C和D形成的化合物与EC2发生氧化还原反应的化学方程式,并标出电子转移的方向和数目:
 .
.
(5)上述元素中的五种元素可形成一种常见复盐,经检测该复盐中三种离子的个数比为2:1:2.则该复盐的化学式为
查看习题详情和答案>>
Ⅰ.原子半径:A<C<B<E<D
Ⅱ.原子的最外层电子数:A=D C=E A+B=C
Ⅲ.原子的核外电子层数:B=C=2A
Ⅳ.B元素的主要化合价:最高正价+最低负价=2
请回答:
(1)甲为由A、B两种元素组成的常见气体,写出其电子式


作保护气
作保护气
.(2)写出某黑色含F的磁性氧化物在E的最高价氧化物对应水化物的稀溶液中反应的离子方程式:
Fe3O4+8H+═2Fe3++Fe2++4H2O
Fe3O4+8H+═2Fe3++Fe2++4H2O
(3)向A、B、C三种元素组成的某盐溶液中滴加AgNO3溶液生成白色沉淀,该反应的化学方程式为
NH4NO2+AgNO3═AgNO2↓+NH4NO3
NH4NO2+AgNO3═AgNO2↓+NH4NO3
,已知该盐溶液常温下呈酸性,则0.1mol/L该盐溶液中离子浓度的大小顺序为C(NO2->C(NH4+)>C(H+)>C(OH-)
C(NO2->C(NH4+)>C(H+)>C(OH-)
(4)写出C和D形成的化合物与EC2发生氧化还原反应的化学方程式,并标出电子转移的方向和数目:


(5)上述元素中的五种元素可形成一种常见复盐,经检测该复盐中三种离子的个数比为2:1:2.则该复盐的化学式为
(NH4)2Fe(SO4)2
(NH4)2Fe(SO4)2
.为探究该复盐中的某种离子,取少量该复盐于试管中并加水溶解,滴加铁氰化钾溶液(K3[Fe(CN)6]),则现象和结论为出现蓝色沉淀,证明有Fe2+
出现蓝色沉淀,证明有Fe2+
.A、B、C、D、E、F、G全为短周期元素,它们在中学常见化合物中显示的部分化合价及原子、离子半径从大到小的序号如下:(注:半径按①、②、③…的顺序依次减小)
(1)用电子式表示BA2的形成过程
 .
.
(2)写出F的最高价氧化物对应的水化物和G的最高价氧化物对应的水化物反应的离子方程式
(3)请设计实验比较B、F的活动性强弱.
查看习题详情和答案>>
| 元素 性质 |
A | B | C | D | E | F | G |
| 化合价 | +1、+5、+7 | 只有+2 | +4 | -3、+2、+4、+5 | 只有-1 | 只有+3 | 只有+1 |
| 原子半径 | ⑤ | ② | ④ | ⑥ | ⑦ | ③ | ① |
| 离子半径 | ① | ⑤ | 无离子 | ② | ③ | ⑥ | ④ |


(2)写出F的最高价氧化物对应的水化物和G的最高价氧化物对应的水化物反应的离子方程式
Al(OH)3+OH-═AlO2-+2H2O.
Al(OH)3+OH-═AlO2-+2H2O.
.(3)请设计实验比较B、F的活动性强弱.
| 元素 | 实验设计 | 现象 | 结论 |
| B | 活动性:B F (填“>”、“<”或“=”) | ||
| F |
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,Y的用量最大.相关物质间的关系如图所示.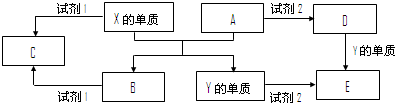
(1)X的单质与A反应的化学方程式是
(2)若试剂1是NaOH溶液,①X的单质与试剂1反应的离子方程式是
②4.5克X的单质参加反应转移的电子数
(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是:
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)
③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是:
查看习题详情和答案>>

(1)X的单质与A反应的化学方程式是
Fe2O3+2Al
Al2O3+2Fe
| ||
Fe2O3+2Al
Al2O3+2Fe
.
| ||
(2)若试剂1是NaOH溶液,①X的单质与试剂1反应的离子方程式是
2Al+2H2O+2OH-═2AlO2-+3H2↑
2Al+2H2O+2OH-═2AlO2-+3H2↑
.②4.5克X的单质参加反应转移的电子数
3.01×1023
3.01×1023
.(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是:
取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+
取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+
.②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是:
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
.