摘要:11. (3)35.5 讲析:(1)标出化合价.碳由+2→+4被氧化. (2)根据化合价升降法配平. (3)20L废水中含KCN 0.2mol.由电子守恒知需Cl2 0.5mol. 光 == 12.(1)2XeF2+2H2O=2Xe↑+4HF+O2↑,XeF2,氧. (2)XeF2+2KOH+KBrO3=KBr04+Xe↑+2KF+2H2O.(3)升高. 讲析:前两问用化合价升降法配平.第(3)问由信息进行分析可知:把HBrO3换成含KOH的KBrO3水溶液就得到了很纯的KBr04晶体.说明在碱性条件下易生成BrO4-. 13.(1)氯气与水反应:Cl2+H2O HCl+HClO.HClO有强氧化性起杀菌.消毒作用,氯气还能将Fe2+氧化:Cl2+2Fe2+=2 Fe3+.Fe3+水解:Fe3++3H2O Fe(OH)33胶体能吸附水中的悬浮杂质.使之净化. (2)向含有Cl2的自来水中加入少量液氨.发生反应: NH3+HClO H20+NH2Cl.使不稳定的HClO转化为稳定的NH2Cl.随着消毒时HClO浓度的下降.平衡左移.HClO得以补充.从而延长液氯杀菌时间. 讲析:回答(1)从消毒.净化两方面入手.起作用的到底是什么?又为什么能生成这些物质?而(2)要从题给的平衡以及两物质的稳定性来考虑.
网址:http://m.1010jiajiao.com/timu_id_3777711[举报]
(2009?淮安二模)现有A、B两种饱和链状饱和一元醇的混合物0.3mol,其质量为13.8g.已知A和B分子中碳原子数均不大于4,且A分子中的碳原子数小于B.则下列说法正确的是( )
查看习题详情和答案>>
下列说法正确的是( )
| A、分子组成上相差1个或若干个CH2原子团的有机物互为同系物 | B、医院里可以用25%的乙醇溶液杀菌消毒 | C、苯分子中不存在C-C和C=C的事实是分子中六个碳碳键的键长、键角、键能都相等,邻二氯苯没有同分异构体,苯不能被酸性高锰酸钾氧化,苯不与溴水加成 | D、H2O 和H2O2 互为同素异形体 |
2010年的上海世博会是第41届综合性世博会,其内运用多处科技创新.图1为PEMFC(质子交换膜燃料电池),以全氟磺酸型固体聚合物为电解质,铂/碳或铂一钌为电极,氢或净化重整气为燃料,空气或纯氧为氧化剂.图2为光伏并网发电装置,通过并网,上海市将使用半导体照明(LED).发出白光的LED是由GaN芯片和钇铝石榴石(YAG,化学式:Y3Al5O12)芯片封装在一起做成的.
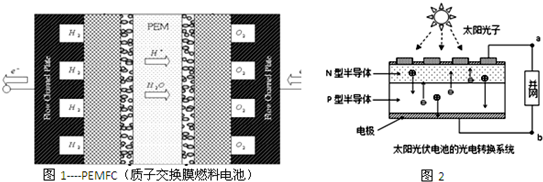
下列有关说法中正确的是( )

下列有关说法中正确的是( )
查看习题详情和答案>>
现有A、B两种链状饱和一元醇的混合物0.3mol,其质量为13.8g.已知A和B分子中碳原子数均不大于4,且A分子中的碳原子数小于B.则下列说法正确的是( )
| A、B的分子式是CH4O | B、若n (A)=n (B),A、B分子组合只有1种情况 | C、若n (A)≠n (B),A、B分子组合有3种情况 | D、n (A):n (B)=1:1或2:1 |