摘要:B; 2.B.C. 讲析:1.溶液中存在Cl-.Br-.I‑三种离子.通入Cl2后先与I‑反应.原来三者物质的量之比是1:2:3.后来变成3:2:1.说明I‑没有完全反应.I‑少了两份.通的Cl2为一份.故Cl2与I‑物质的量之比是1: 3. 2.IBr分子中两非金属原子之间以共价键结合.它属于分子晶体.又因碘元素呈+1价IBr可以作为氧化剂.A.D选项说法正确.IBr与水反应生成HIO和HBr元素化合价无变化且无I‑.
网址:http://m.1010jiajiao.com/timu_id_3777705[举报]
下列溶液中微粒的物质的量浓度关系正确的是
- A.Ca(ClO)2溶液中:c(Ca2+)>c(ClO-)>c(OH-)>c(H+)
- B.等体积、等物质的量浓度的NaX和弱酸HX混合:c(Na+)=c(X-)>c(OH-)=c(H+)
- C.常温下,将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中:c(Cl-)>c(NH4+)> c(NH3·H2O)>c(OH-)>c(H+)
- D.将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中:c(S2-)+2c(OH-)=2c(H+)+c(HS-)+3c(H2S)
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一.漂白粉是常用的消毒剂.根据所学知识,回答下列问题:
(1)工业上将氯气通入石灰乳制取漂白粉,化学反应方程式为
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
(3)制取漂白粉的氯气可通过电解饱和食盐水得到.在电解食盐水之前,需要提纯食盐水.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸 ④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
A、①④②⑤③B、④①②⑤③C、②⑤④①③D、⑤②④③①
查看习题详情和答案>>
(1)工业上将氯气通入石灰乳制取漂白粉,化学反应方程式为
2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O
2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O
.(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
.(3)制取漂白粉的氯气可通过电解饱和食盐水得到.在电解食盐水之前,需要提纯食盐水.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是
C
C
.①过滤 ②加过量的NaOH溶液 ③加适量的盐酸 ④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
A、①④②⑤③B、④①②⑤③C、②⑤④①③D、⑤②④③①
 A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:
A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:(1)若A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液,E溶于NaOH溶液的离子方程式是
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
;工业上冶炼A的化学反应方程式是2NaCl(熔融)
2Na+Cl2↑
| ||
2NaCl(熔融)
2Na+Cl2↑
.
| ||
(2)若C是既含有极性键又含有非极性键的四原子分子,则实验室制取C的化学方程式是
CaC2+2H2O→C2H2↑+Ca(OH)2
CaC2+2H2O→C2H2↑+Ca(OH)2
;1mol C完全燃烧生成液态水时放热1300kJ,则C完全燃烧的热化学方程式是2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2600kJ?mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2600kJ?mol-1
.A与盐B的溶液反应时只生成气体C、碳酸钙沉淀和水,则B的化学式是Ca(HCO3)2
Ca(HCO3)2
.(2009?静安区一模)某学习小组利用下图所示装置进行“铁与水气反应”和其他实验(略去了夹持仪器).
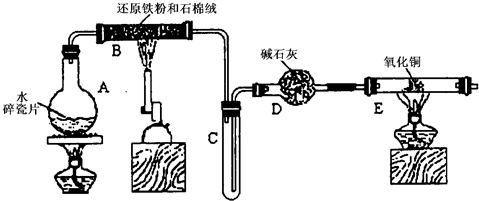
(1)仪器B的名称是
(2)B中发生反应的化学方程式是
(3)加热E以前要对装置中的气体验纯,方法是:收集一试管气体,然后
(4)已知有反应:Cu20+2H+→Cu+Cu2++H20,则可用来检验反应后E中的红色固体中除Cu外是否含Cu20,可用的试剂是
a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硫酸
(5)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成或铜的相对原子质量.若反应前盛有药品的E、F的质量分别是bg、cg,反应后分别是dg、eg.
①水中元素的物质的量之比可表示为n(H):n(0)=
②若空的E管的质量为ag,加热后CuO完全还原为Cu,则铜的相对原子质量可表示为
.
查看习题详情和答案>>

(1)仪器B的名称是
石英管或硬质玻璃管
石英管或硬质玻璃管
,石棉绒的作用是增大铁与水蒸气接触面积,防止加热时固体喷入导管
增大铁与水蒸气接触面积,防止加热时固体喷入导管
.(2)B中发生反应的化学方程式是
3Fe+4H2O(g)
Fe3O4+H2
| ||
3Fe+4H2O(g)
Fe3O4+H2
.
| ||
(3)加热E以前要对装置中的气体验纯,方法是:收集一试管气体,然后
将试管口靠近酒精灯火焰,弱发出噗的声音,说明气体纯净;若发生尖锐爆鸣声,说明气体不纯
将试管口靠近酒精灯火焰,弱发出噗的声音,说明气体纯净;若发生尖锐爆鸣声,说明气体不纯
.(4)已知有反应:Cu20+2H+→Cu+Cu2++H20,则可用来检验反应后E中的红色固体中除Cu外是否含Cu20,可用的试剂是
bc
bc
(填序号)a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硫酸
(5)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成或铜的相对原子质量.若反应前盛有药品的E、F的质量分别是bg、cg,反应后分别是dg、eg.
①水中元素的物质的量之比可表示为n(H):n(0)=
e-c-(b-d):
| b-d |
| 16 |
e-c-(b-d):
;若反应后E中除Cu外还含有另种还原产物Cu20,则该比值将| b-d |
| 16 |
无影响
无影响
(选填“偏大”“偏小”或“无影响”).②若空的E管的质量为ag,加热后CuO完全还原为Cu,则铜的相对原子质量可表示为
| 16(d-a) |
| b-d |
| 16(d-a) |
| b-d |
A、B、C、D、E、F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示:
请回答下列问题:
(1)写出A与E形成的化合物的电子式
 .
.
(2)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是
(3)F的盐酸盐水溶液呈酸性,原因是
(4)化合物M是一种元素C的+6含氧酸钾盐,常用作净水剂与消毒剂.由元素C稳定的氢氧化物与次氯酸钾、氢氧化钾溶液反应制取化合物M,则制备M的离子反应方程式是
查看习题详情和答案>>
| 元素 | 原子结构或性质 | ||
| A | 原子最外层电子数是内层电子总数的
| ||
| B | 形成化合物种类最多的元素,其单质为固体 | ||
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 | ||
| D | 地壳中含量最多的元素 | ||
| E | 与D同主族 | ||
| F | 与E同周期,且最外层电子数等于电子层数 |
(1)写出A与E形成的化合物的电子式


(2)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是
C+H2O
CO+H2
| ||
C+H2O
CO+H2
| ||
(3)F的盐酸盐水溶液呈酸性,原因是
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
(用离子方程式表示);F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
| ||
(4)化合物M是一种元素C的+6含氧酸钾盐,常用作净水剂与消毒剂.由元素C稳定的氢氧化物与次氯酸钾、氢氧化钾溶液反应制取化合物M,则制备M的离子反应方程式是
2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O
2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O
.