摘要:(1)CuCl2水解,Cu2++2H2OCu(OH)2+2H+.使溶液呈酸性.(2)电解时.Cu2+可在阴极放电析出Cu.随c(Cu2+)降低.Cu2+的水解平衡左移.导致溶液中c(H+)下降.溶液的升高.(3)溶液的PH降低 因阳极上产生Cl2.一部分Cl2溶于水后发生反应:Cl2 +H2OH++Cl-+HClO.故使溶液中c(H+)增大.即溶液PH降低.
网址:http://m.1010jiajiao.com/timu_id_3777439[举报]
工业上制氯化铜无水物时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁和SiO2),充分搅拌后使之溶解,制取流程如下:
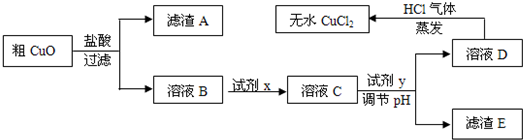
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38.试回答:
(1)根据常温时Fe(OH)3的Ksp计算,当溶液中的Fe3+完全沉淀(此时溶液中的Fe3+物质的量的浓度=10-5mol/L),溶液的pH=
(2)溶液D制取无水CuCl2时,需在HCl气体中蒸干,原因是
(3)粗CuO溶于过量盐酸后,得到的溶液B中加入试剂x将Fe2+氧化为Fe3+,试剂x可以是
A.KMnO4溶液 B.氯水 C.NaClO溶液 D.O3
若用H2O2溶液,则反应的离子方程式为
(4)溶液C加入试剂y,要调整溶液的pH至3-4,试剂y不能是
A.NaOH溶液 B.Cu(OH)2固体 C.Cu2(OH)2CO3固体 D.CuO固体
(5)将ag粗CuO经过以上一系列操作之后,最终得到bg无水CuCl2(不考虑实验过程中操作引起的损耗),下列说法正确的是
A.粗CuO中Cu2+数目小于
B.粗CuO中CuO物质的量小于
mol
C.粗CuO中所含的铜元素的质量分数为
x100%
D.粗CuO中关于CuO的量无法确定.
查看习题详情和答案>>

已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38.试回答:
(1)根据常温时Fe(OH)3的Ksp计算,当溶液中的Fe3+完全沉淀(此时溶液中的Fe3+物质的量的浓度=10-5mol/L),溶液的pH=
3
3
.(2)溶液D制取无水CuCl2时,需在HCl气体中蒸干,原因是
HCl抑制CuCl2水解
HCl抑制CuCl2水解
.(3)粗CuO溶于过量盐酸后,得到的溶液B中加入试剂x将Fe2+氧化为Fe3+,试剂x可以是
BD
BD
(填以下选项序号).A.KMnO4溶液 B.氯水 C.NaClO溶液 D.O3
若用H2O2溶液,则反应的离子方程式为
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
.(4)溶液C加入试剂y,要调整溶液的pH至3-4,试剂y不能是
A
A
(填以下选项序号),原因是将引入新杂质NaCl
将引入新杂质NaCl
.A.NaOH溶液 B.Cu(OH)2固体 C.Cu2(OH)2CO3固体 D.CuO固体
(5)将ag粗CuO经过以上一系列操作之后,最终得到bg无水CuCl2(不考虑实验过程中操作引起的损耗),下列说法正确的是
ABD
ABD
.(NA表示阿伏伽德罗常数)A.粗CuO中Cu2+数目小于
| aNA |
| 80 |
| b |
| 135 |
C.粗CuO中所含的铜元素的质量分数为
| 64b |
| 135a |
D.粗CuO中关于CuO的量无法确定.
氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色.已知pH为5时,+2价铜已开始以碱式盐的形式沉淀.某兴趣小组去一家回收含铜电缆废料的工厂做社会调查,技术人员向他们展示了处理废料的综合利用方案:

(1)加入的A是
(2)反应②的离子方程式是
(3)保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如图二所示.则溶液温度控制在
查看习题详情和答案>>

(1)加入的A是
稀硫酸
稀硫酸
,通入的B是空气
空气
.(2)反应②的离子方程式是
2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO4-+2H+
2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO4-+2H+
.为提高Cu2Cl2的产率,常在反应②的溶液中加适量稀碱溶液,控制pH为3.5.这样做的目的是OH-中和了反应生成的H+,有利于反应向右进行,提高Cu2Cl2的产率
但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
OH-中和了反应生成的H+,有利于反应向右进行,提高Cu2Cl2的产率
但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
.但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
(3)保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如图二所示.则溶液温度控制在
53℃~55℃
53℃~55℃
时,Cu2Cl2的产率已达到94%,当温度高于65℃时,Cu2Cl2产率会下降,其原因可能是温度过高,促进了CuCl2的水解
温度过高,促进了CuCl2的水解
.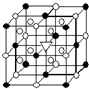 A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子
A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子AlF6-
AlF6-
、Na+
Na+
;大立方体的体心处▽所代表的是AlF6-
AlF6-
.冰晶石在化工生产中的用途电解炼铝的助熔剂
电解炼铝的助熔剂
.(2)H2S和H2O2的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
H2O2分子间存在氢键,与水分子可形成氢键
H2O2分子间存在氢键,与水分子可形成氢键
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体.写出铜原子价电子层的电子排布式
3d104s1
3d104s1
,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有Cr
Cr
(填元素符号).实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有共价键和配位键
共价键和配位键
.实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4?H2O晶体.实验中所加C2H5OH的作用是降低Cu(NH3)4SO4?H2O的溶解度
降低Cu(NH3)4SO4?H2O的溶解度
.B.用含少量铁的氧化铜制取氯化铜晶体(CuCl2?xH2O).有如下操作:
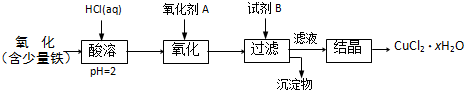
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解.
(1)加热酸溶过程中发生反应的离子方程式有:
Fe+2H+=Fe2++H2↑、CuO+2H+=Cu2++H2O
Fe+2H+=Fe2++H2↑、CuO+2H+=Cu2++H2O
(2)氧化剂A可选用
①
①
(填编号,下同)①Cl2 ②KMnO4 ③HNO3
(3)要得到较纯的产品,试剂B可选用
③
③
①NaOH ②FeO ③CuO
(4)试剂B的作用是
①③
①③
①提高溶液的pH ②降低溶液的pH ③使Fe3+完全沉淀 ④使Cu2+完全沉淀
(5)从滤液经过结晶得到氯化铜晶体的方法是
②④①
②④①
(按实验先后顺序填编号)①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(6)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止、冷却、称量所得无水CuCl2的质量为n g.
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g.
试评价上述两种实验方案,其中正确的方案是
二
二
,据此计算得x=| 80m-135n |
| 18n |
| 80m-135n |
| 18n |
 关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:观点一是:“理论派”认为电解氯化铜溶液后溶液的pH升高.观点二是:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时pH的变化如图曲线的关系.?请回答下列问题:
关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:观点一是:“理论派”认为电解氯化铜溶液后溶液的pH升高.观点二是:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时pH的变化如图曲线的关系.?请回答下列问题:(1)电解前氯化铜溶液的pH处在A点位置的原因是
Cu2++2H2O
Cu(OH)2+2H+
| 水解 |
Cu2++2H2O
Cu(OH)2+2H+
(用离子方程式说明).| 水解 |
(2)“理论派”所持观点的理论依据是
因为Cu2++2e-═Cu,使Cu2+水解平衡向左移动,c(H+)减少,pH上升.
因为Cu2++2e-═Cu,使Cu2+水解平衡向左移动,c(H+)减少,pH上升.
.(3)你持何种观点?
实验派
实验派
(填“理论派”或“实验派”)理由是CuCl2
Cu+Cl2↑,Cl2+H2O═HCl+HClO,使溶液酸性增强,pH降低.
| ||
CuCl2
Cu+Cl2↑,Cl2+H2O═HCl+HClO,使溶液酸性增强,pH降低.
(从化学原理加以简述).
| ||
硫酸亚铁铵(NH4)2SO4?FeSO4?6H2O是一种重要化学试剂,可以用除去锌镀层的铁片来制取硫酸亚铁铵,流程如下:

请回答下列问题:
(1)确定锌镀层被除去的标志是
(2)操作Ⅱ是
(3)A物质可以为
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
B物质的成分为
(4)加少量硫酸调节pH为 1~2的目的是
(5)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是
查看习题详情和答案>>

请回答下列问题:
(1)确定锌镀层被除去的标志是
反应速率突然减小
反应速率突然减小
;(2)操作Ⅱ是
过滤
过滤
.(3)A物质可以为
b、d
b、d
(填编号).a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
B物质的成分为
Fe和Cu
Fe和Cu
.(4)加少量硫酸调节pH为 1~2的目的是
抑制Fe2+、NH4+水解
抑制Fe2+、NH4+水解
.(5)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是
避免加热过程中晶体受热分解(或被氧化)
避免加热过程中晶体受热分解(或被氧化)
.