网址:http://m.1010jiajiao.com/timu_id_3777349[举报]
| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应的水化物,能按1:1电离出电子数相等的阴、阳离子 |
| E | 其单质有多种同素异形体,一种为自然界中硬度最大 |


(2)写出D的最高价氧化物的水化物电离出的阴离子的电子式


(3)D2ZX3的溶液与Y的单质可能发生反应,其反应的离子方程式为
(4)用化学符号表示D2EX3的水溶液中各离子的浓度关系(列等式)
(5)已知ZX2与X2可发生反应:2ZX2(g)+X2(g)?2ZX3(g)△H<0;
当反应达到平衡时不断改变条件(不改变ZX2、X2、ZX3的量),反应速率随时间的变化如图:

其中表示平衡混合物中ZX3含量最高的一段时间是
(填“大于”、“等于”或“小于”).

(1)用等式表示Na2CO3溶液中所有阳离子和阴离子浓度的关系:
(2)写出Na2CO3溶液中加入少量盐酸的离子方程式
(3)当混合液的pH=
(4)在20mL 0.1mol/LNa2CO3溶液中加入BaCl2粉末3.328×10-7 g时开始产生沉淀X,则KSP(X)=
①在A或D中滴入C,均有沉淀生成;②D和B反应生成的气体能被A吸收;③A和D反应生成的气体能被B吸收.
写出化学式:A
Ⅱ.已知下列信息:
(CH3)2C=CHCH3
| KMnO4 |
| H+ |
 -CH3+CH3COOH
-CH3+CH3COOHCH2=CH-CH=CH2+CH2=CH2
| 120℃ |

一种用途较广泛的有机玻璃树脂--聚丁烯酸甲酯结构简式为:
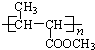
有一种合成这种高聚物的途径副产物污染少或无污染,原子利用率较高,符合“绿色化学挑战计划”的要求,其合成路线如下:

试回答下列问题:
(1)写出B、D的结构简式:B




(2)反应④属于
(3)在上述合成过程中,原子利用率最高的化学反应有
最近雾霾天气肆虐我国大部分地区。其中SO2是造成空气的污染的主要原因,利用钠碱循环法可除去SO2。
(1)钠碱循环法中,吸收液为Na2SO3溶液,该反应的离子方程式是________。
(2)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列微粒可以大量共存的是______(填序号)。
A.CO32- HSO3- B. HCO3- HSO3- C. SO32- HCO3- D. H2SO3 HCO3-
(3)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
①根据上表判断NaHSO3溶液显_______性,试解释原因__________________________;
②在NaHSO3溶液中离子浓度关系不正确的是_______(填序号)。
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
C.c(H2SO3)+ c(H+)=c(SO32-)+c(OH-)
D.c(Na+)+ c(H+)=2c(SO32-)+ c(HSO3-)+ c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽处理,直至得到pH>8的吸收液再循环利用,电解示意图如下:
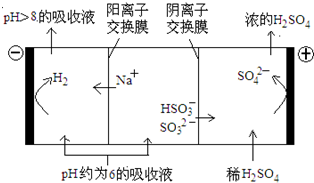
①写出阳极上发生的电极反应式____________;
②当电极上有1mol电子转移时阴极产物的质量为__________。 查看习题详情和答案>>
最近雾霾天气肆虐我国大部分地区。其中SO2是造成空气的污染的主要原因,利用钠碱循环法可除去SO2。
(1)钠碱循环法中,吸收液为Na2SO3溶液,该反应的离子方程式是________。
(2)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列微粒可以大量共存的是______(填序号)。
A.CO32- HSO3- B. HCO3- HSO3- C. SO32- HCO3- D. H2SO3 HCO3-
(3)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
|
n(SO32-):n(HSO3-) |
91:9 |
1:1 |
1:91 |
|
pH |
8.2 |
7.2 |
6.2 |
①根据上表判断NaHSO3溶液显_______性,试解释原因__________________________;
②在NaHSO3溶液中离子浓度关系不正确的是_______(填序号)。
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
C.c(H2SO3)+ c(H+)=c(SO32-)+c(OH-)
D.c(Na+)+ c(H+)=2c(SO32-)+ c(HSO3-)+ c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽处理,直至得到pH>8的吸收液再循环利用,电解示意图如下:
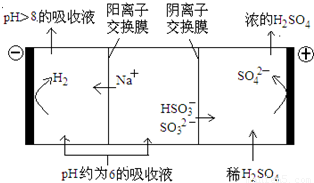
①写出阳极上发生的电极反应式____________;
②当电极上有1mol电子转移时阴极产物的质量为__________。
查看习题详情和答案>>