摘要: (1)AgCl饱和所需Ag+浓度[Ag+]1==1.8×10-7摩/升 Ag2CrO4饱和所需Ag+浓度[Ag+]2==4.36×10-5摩/升 [Ag+]1<[Ag+]2.Cl-先沉淀. (2) Ag2CrO4开始沉淀时c(Cl-)==4.13×10-6<10-5.所以能有效地分离.
网址:http://m.1010jiajiao.com/timu_id_3777291[举报]
下列根据实验操作和现象所得出的结论正确的是( )
|
查看习题详情和答案>>
 (2012?信阳二模)如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.
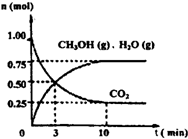
(2012?信阳二模)如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.(1)目前工业上有一种方法是用CO2来生产燃料甲醇.为探究该反应原理,进行如下实验:某温度下,在容积为2L的密闭容器中,充入1mol CO2和3.25mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间变化如右图所示:
①从反应开始到平衡,氢气的平均反应速率v(H2)=
0.1125mol/(L?min)
0.1125mol/(L?min)
.②下列措施中一定不能使CO2的转化率增大的是
ACD
ACD
.A.在原容器中再充入1mol CO2 B.在原容器中再充入1mol H2
C.在原容器中充入1mol氦气 D.使用更有效的催化剂
E.缩小容器的容积 F.将水蒸气从体系中分离
(2)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5mol/L.若忽略水的电离及H2CO3的第二级电离,则H2CO3?HCO3-+H+的电离平衡常数K=
4.2×10-7
4.2×10-7
.(已知:10-5.6=2.5×10-6).(3)标准状况下,将4.48L CO2通入200mL 1.5mol/L的NaOH溶液,所得溶液中离子浓度由大到小的顺序为
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
.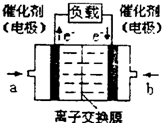
(4)如图是甲醇燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是
甲醇
甲醇
(填“甲醇”或“氧气”),其电极上发生的电极反应式为CH3OH+8OH--6e-═CO32-+6H2O
CH3OH+8OH--6e-═CO32-+6H2O
.(5)已知,常温下Ksp(AgCl)=2.0×10-10,Ksp(AgBr)=5.4×10-13.向AgNO3溶液中加入KBr和KCl,当两种沉淀共存时,溶液中c(Br-)和c(Cl-)的比值为
2.7×10-3
2.7×10-3
.25℃时,向AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀.已知有关物质的颜色和溶度积如下:
|
查看习题详情和答案>>
一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)×cn(Bm-),称为难溶电解质的离子积.在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀.已知有关物质的颜色和溶度积如下:
|
查看习题详情和答案>>
火柴头上通常含有氯酸钾、二氧化锰、硫等物质.某研究性学习小组进行火柴头中有关物质的实验探究.
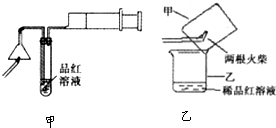
(1)检验火柴头中含有硫将两根火柴放在如图甲所示实验装置中漏斗下面,用一根燃着的火柴点燃它,慢慢拉动注射器活塞抽气,让火柴燃烧产生的气体通过稀品红溶液,观察到品红溶液褪色.
①燃烧产生的气体中一定含有 .
②可用于替代试管中品红溶液的试剂有 (填标号).
A.稀高锰酸钾酸性溶液 B.饱和石灰水
C.稀溴水 D.烧碱溶液
③某同学提出用图乙所示方法进行实验更为简便.他的操作是:
i.当图乙中所示火柴头燃烧完时,立即移出火柴;
ii. .
(2)证明火柴中的氯元素是以氯酸钾的形式存在,而不是以氯化钾的形式存在,请完成下列操作:
①取3~4根火柴,摘下火柴头,浸入水中,片刻后,取少量溶液于试管中,加入少量的硝酸银溶液,没有白色沉淀生成;
②再往上述溶液中加入稀硝酸和NaNO2溶液,观察到有白色沉淀生成.反应的离子方程式是 ;
③将燃尽的火柴头浸泡在少量水中,片刻后取少量溶液于试管中,滴加AgNO3和稀硝酸,可观察到白色沉淀产生,说明将燃尽的火柴头浸泡在少量水中,会有 物质被浸出,说明火柴头燃烧时其中含有的 转化为该物质.
(3)测定火柴头中KClO3的含量主要实验步骤如下:
(i)刮取火柴头,小心研碎,称得质量为2.45g;
(ii)用适量蒸馏水充分浸泡后过滤、洗涤残渣;
(iii)往装有滤液和洗涤液的烧杯中加入过量的NaNO2溶液、AgNO3溶液和稀硝酸,搅拌,充分反应后,过滤、洗涤沉淀;
(iv)干燥沉淀物,称得其质量为1.435g.
①反应中NaNO2、AgNO3均需要过量的原因是 ;
②实验测得火柴头中KClO3的质量分数为 ;
③如果第ii步中未洗涤沉淀残渣,测得KC1O3的质量分数将 (填“偏大”、“偏小”、或“无影响”,下同);如果第Ⅲ步中未洗涤AgCl沉淀,测得KClO3的质量分数将 .
查看习题详情和答案>>

(1)检验火柴头中含有硫将两根火柴放在如图甲所示实验装置中漏斗下面,用一根燃着的火柴点燃它,慢慢拉动注射器活塞抽气,让火柴燃烧产生的气体通过稀品红溶液,观察到品红溶液褪色.
①燃烧产生的气体中一定含有
②可用于替代试管中品红溶液的试剂有
A.稀高锰酸钾酸性溶液 B.饱和石灰水
C.稀溴水 D.烧碱溶液
③某同学提出用图乙所示方法进行实验更为简便.他的操作是:
i.当图乙中所示火柴头燃烧完时,立即移出火柴;
ii.
(2)证明火柴中的氯元素是以氯酸钾的形式存在,而不是以氯化钾的形式存在,请完成下列操作:
①取3~4根火柴,摘下火柴头,浸入水中,片刻后,取少量溶液于试管中,加入少量的硝酸银溶液,没有白色沉淀生成;
②再往上述溶液中加入稀硝酸和NaNO2溶液,观察到有白色沉淀生成.反应的离子方程式是
③将燃尽的火柴头浸泡在少量水中,片刻后取少量溶液于试管中,滴加AgNO3和稀硝酸,可观察到白色沉淀产生,说明将燃尽的火柴头浸泡在少量水中,会有
(3)测定火柴头中KClO3的含量主要实验步骤如下:
(i)刮取火柴头,小心研碎,称得质量为2.45g;
(ii)用适量蒸馏水充分浸泡后过滤、洗涤残渣;
(iii)往装有滤液和洗涤液的烧杯中加入过量的NaNO2溶液、AgNO3溶液和稀硝酸,搅拌,充分反应后,过滤、洗涤沉淀;
(iv)干燥沉淀物,称得其质量为1.435g.
①反应中NaNO2、AgNO3均需要过量的原因是
②实验测得火柴头中KClO3的质量分数为
③如果第ii步中未洗涤沉淀残渣,测得KC1O3的质量分数将