摘要:AD 2.B 3.B 讲析:1.中性溶液中. .AG=0,酸性溶液中..AG<1.AG<0.常温下0.1mol·L-1氢氧化钠溶液中..AG=-12,常温下0.1mol·L-1盐酸溶液中..AG=12. 2.纯水的pH值是由其[H+]决定的.[H+]对水的离子积Kw有关.而Kw在不同温度时数值不一样.常温时水的Kw=1×10-14.纯水中[H+]=[OH-]=10-7mol/L.因水的电离是吸热反应.温度升高到80℃.平衡向右移动.电离程度加大.Kw>1×10-14.[H+]=[OH-]>1×10-7mol/L.所以pH<7.由于是纯水[H+]=[OH-].纯水仍是中性.不是酸性.任何温度下纯水都是中性.答案:因水的电离是吸热反应.温度升高到80℃.平衡向右移动.电离程度加大.Kw>1×10-14.[H+]=[OH-]>1×10-7mol/L.所以pH<7 3.本题的特点是:由实验结果分析.酸和碱溶液混合后所得溶液呈酸性.原因有两种可能:一是这两种溶液恰好完全反应.但参与反应的是弱碱和强酸.生成强酸弱碱盐.易水解而显酸性,二是酸和碱并没有恰好完全反应.反应后酸有剩余.因而溶液显酸性.本题中的酸溶液[H+]=1×10-3mol/L.如此应是强酸.它是完全电离.可见它是一种稀溶液,如是弱酸.因它只有少部分电离.则弱酸的浓度可能较大.碱溶液[OH-]=1×10-3mol/L.当然也适于上述分析.即或是强碱的稀溶液.或是弱碱的较浓溶液.根据选项.依照题意.可确定(B)为正确选项.
网址:http://m.1010jiajiao.com/timu_id_3777274[举报]
 (2013?大连模拟)向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如右图,则原混合溶液中MgCl2与FeCl3的物质的量之比为( )
(2013?大连模拟)向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如右图,则原混合溶液中MgCl2与FeCl3的物质的量之比为( )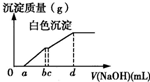 向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图所示,则原混合溶液中MgCl2与FeCl3的物质的量之比为( )
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图所示,则原混合溶液中MgCl2与FeCl3的物质的量之比为( )熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求。试回答下列问题:
(1)在仪器a.分液漏斗 b.试剂瓶 c.集气瓶 d.滴定管 e.容量瓶 f.量筒 g.托盘天平中,标有“0”刻度的是 (填序号)。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺,在下列仪器中,没有用到“磨砂”工艺处理的有 (填序号)。
a.试管 b.分液漏斗 c.带滴管的试剂瓶(滴瓶) d.集气瓶 e.酸式滴定管 f.碱式滴定管
(3)用装置甲、乙、丙和乳胶管组成一套装置(气密性已检查),可用于制取并收集NH3或HCl气体,可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。试回答下列问题:

①若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B均为无色液体,则试剂A为 ,制取该气体利用了B的性质有 、 。
通过丙中紫色石蕊溶液变红或变蓝,说明乙中气体已集满。若石蕊溶液变蓝,则烧瓶甲中应加入的固体试剂A为 。
②若在乙中收集氨气,气体流经装置的顺序是:a



 d(填接口代号)。
d(填接口代号)。
查看习题详情和答案>>