摘要:(1)3CO+Fe2O32Fe+3CO2 (2)⑤①②③⑥④ (3)①一氧化碳能燃烧.二氧化碳不能燃烧 ②一氧化碳能和氧化铁反应.二氧化碳不能 ③二氧化碳能使澄清的石灰水变浑浊.一氧化碳不能 2+CO2==CaCO3↓+H2O
网址:http://m.1010jiajiao.com/timu_id_3775082[举报]
请用化学用语表示:
(1)2个氢原子
(4)地壳中含量最多的金属元素
(5)碳酸钠中碳元素的化合价为+4
(6)过氧化氢溶液中加入二氧化锰:
(7)利用一氧化碳还原氧化铁来炼铁
(8)“湿法炼铜”的反应原理
查看习题详情和答案>>
(1)2个氢原子
2H
2H
;(2)3个氨气分子3NH3
3NH3
;(3)亚铁离子Fe2+
Fe2+
;(4)地壳中含量最多的金属元素
Al
Al
;(5)碳酸钠中碳元素的化合价为+4
Na2
O3
| +4 |
| C |
Na2
O3
;| +4 |
| C |
(6)过氧化氢溶液中加入二氧化锰:
2H2O
2H2O+O2↑
| ||
2H2O
2H2O+O2↑
;
| ||
(7)利用一氧化碳还原氧化铁来炼铁
3CO+Fe2O
2Fe+3CO2
| ||
3CO+Fe2O
2Fe+3CO2
;
| ||
(8)“湿法炼铜”的反应原理
Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
.常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉.
脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 (红褐色固体)
(1)Fe(OH)2读作
(2)某同学用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行两个实验:
实验Ⅰ:
请回答:
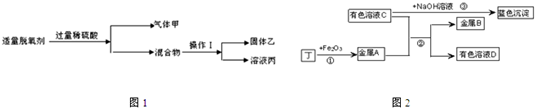
如图1,①操作Ⅰ的名称是
②溶液丙中含有的金属阳离子是
实验Ⅱ:将乙洗涤烘干后,二氧化碳通过灼热的乙生成丁.进行如图2实验,物质之间的转化关系如图(部分产物略去).
①金属A与B的活动性:A
②区别有色溶液C与有色溶液D的方法是
③反应①的化学方程式为:
④向溶液C中加入BaCl2溶液,有白色沉淀产生.其化学方程式为
查看习题详情和答案>>
脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 (红褐色固体)

(1)Fe(OH)2读作
氢氧化亚铁
氢氧化亚铁
.(2)某同学用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行两个实验:
实验Ⅰ:
请回答:
如图1,①操作Ⅰ的名称是
过滤
过滤
;②溶液丙中含有的金属阳离子是
Fe2+、Na+
Fe2+、Na+
(写微粒符号)实验Ⅱ:将乙洗涤烘干后,二氧化碳通过灼热的乙生成丁.进行如图2实验,物质之间的转化关系如图(部分产物略去).
①金属A与B的活动性:A
>
>
B(填“>”“<”或“﹦”);②区别有色溶液C与有色溶液D的方法是
观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液
观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液
;③反应①的化学方程式为:
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
;
| ||
④向溶液C中加入BaCl2溶液,有白色沉淀产生.其化学方程式为
CuSO4+BaCl2=BaSO4↓+CuCl2
CuSO4+BaCl2=BaSO4↓+CuCl2
.(2013?北京一模)人类的生产和生活都离不开金属.
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是
赤铁矿 孔雀石 铝土矿
(主要成分Fe2O3)〔主要成分Cu2(OH)2CO3〕(主要成分Al2O3)
(2)金属的回收和利用是保护金属资源的一种有效途径.
①废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为
②向含有AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是
A.固体中一定有Fe、Ag,可能有 Cu、Zn
B. 固体中一定有Fe、Zn,可能有 Cu、Ag
C.滤液中一定含Fe2+、Zn2+,不含Cu2+、Ag+
D.滤液中一定含Zn2+、Fe2+,可能含Cu2+
(3)某次实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放会造成水污染.于是几位同学利用课余时间处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下:

请回答:
①操作1的名称是
②若要检验向固体C中加入的稀硫酸是否足量的方法是
③若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量废液的质量、蒸发得到固体硫酸锌的质量和
查看习题详情和答案>>
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是
Al
Al
.金属以矿物形式存在,下列矿石的主要成分属于氧化物的是Fe2O3、Al2O3
Fe2O3、Al2O3
(填化学式).赤铁矿 孔雀石 铝土矿
(主要成分Fe2O3)〔主要成分Cu2(OH)2CO3〕(主要成分Al2O3)
(2)金属的回收和利用是保护金属资源的一种有效途径.
①废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
②向含有AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是
C
C
A.固体中一定有Fe、Ag,可能有 Cu、Zn
B. 固体中一定有Fe、Zn,可能有 Cu、Ag
C.滤液中一定含Fe2+、Zn2+,不含Cu2+、Ag+
D.滤液中一定含Zn2+、Fe2+,可能含Cu2+
(3)某次实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放会造成水污染.于是几位同学利用课余时间处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下:

请回答:
①操作1的名称是
过滤
过滤
;固体A的成分为Zn、Fe、Cu
Zn、Fe、Cu
.②若要检验向固体C中加入的稀硫酸是否足量的方法是
取少量铜,加适量稀硫酸,若无气泡产生,证明硫酸足量
取少量铜,加适量稀硫酸,若无气泡产生,证明硫酸足量
.③若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量废液的质量、蒸发得到固体硫酸锌的质量和
操作1中加入锌粉的质量
操作1中加入锌粉的质量
..(2005?西城区二模)研究小组为了解北京西山的地质情况,从实地选取两块样品D和J,进行如图所示的实验(其中部分反应产物被略去):
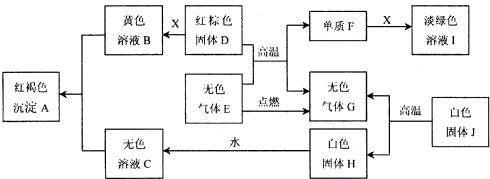
(1)样品D和J的主要成分分别是(用化学式表示)
(2)实验室用固体J制取气体G的化学方程式为
(3)上述实验中部分反应的化学方程式
J→H:
F+X→:
D+E→:
B+C→:
查看习题详情和答案>>

(1)样品D和J的主要成分分别是(用化学式表示)
Fe2O3
Fe2O3
、CaCO3
CaCO3
.(2)实验室用固体J制取气体G的化学方程式为
CaCO3+2HCl=CaCl2+CO2↑+H2O
CaCO3+2HCl=CaCl2+CO2↑+H2O
.(3)上述实验中部分反应的化学方程式
J→H:
CaCO3
CaO+CO2↑
| ||
CaCO3
CaO+CO2↑
;
| ||
F+X→:
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
;D+E→:
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
;
| ||
B+C→:
Fe2(SO4)3+3Ca(OH)2=2Fe(OH)3↓+3CaSO4
Fe2(SO4)3+3Ca(OH)2=2Fe(OH)3↓+3CaSO4
.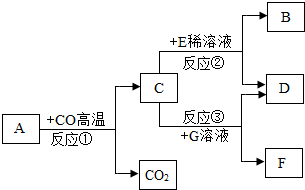 (2012?日照)现有A~G七种物质,已知A是赤铁矿的主要成分,E的浓溶液稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系:
(2012?日照)现有A~G七种物质,已知A是赤铁矿的主要成分,E的浓溶液稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系:(1)写出下列物质的化学式:D:
FeSO4
FeSO4
F:Cu
Cu
(2)在反应①②③中,属于置换反应的是
②③
②③
(填序号).(3)工业上常利用反应①的原理来炼铁,写出反应①的化学方程式
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
(4)写出物质A与E的稀溶液发生反应的化学方程式
Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
.