摘要:HA.HB.HC三种一元弱酸溶液的浓度都是0.1mol/L.在室温时.HA溶液中A‑的浓度是1.32×10-3mol/L.HB的电离度是1.15%.HC溶液的pH值等于3.这三种酸的酸性由强到弱的顺序是 .
网址:http://m.1010jiajiao.com/timu_id_3773262[举报]
(8分)现有HA、HB、HC三种一元弱酸,分析并回答下列问题:
①等PH值的三种酸,加水稀释的PH值变化如图比较三种酸的酸性强弱 〉
〉 三种酸的物质的量浓度由大到小的顺序 。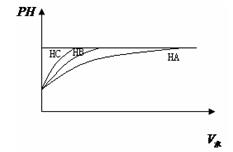
②同浓度的NaA, NaB, NaC,PH值的大小 〉 〉 。
③25℃时若已知NH4B的溶液显中性,则NH4A溶液的PH值 7,写出NH4C的水解的离子方程式 。
④PH=2的HA与PH=12的NaOH等体积混合后,溶液中离子浓度由大到小的顺序是 。
现有HA、HB、HC三种一元弱酸,分析并回答下列问题:
①等PH值的三种酸,加水稀释的PH值变化如图比较三种酸的酸性强弱________>________>________三种酸的物质的量浓度由大到小的顺序________.

②同浓度的NaA,NaB,NaC,PH值的大小________>________>________.
③25℃时若已知NH4B的溶液显中性,则NH4A溶液的PH值________7,写出NH4C的水解的离子方程式________.
④PH=2的HA与PH=12的NaOH等体积混合后,溶液中离子浓度由大到小的顺序是________.
有三种一元弱酸HA,HB,HC的钠盐分别为NaA,NaB,NaC,它们相同物质的量浓度的溶液的pH依次为12、8、10,则三种弱酸的酸性由大到小的顺序是
- A.HA>HB>HC
- B.HA>HC>HB
- C.HB>HC>HA
- D.HC>HB>HA