网址:http://m.1010jiajiao.com/timu_id_3770575[举报]
(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化,其反应式如下:
①CH4(g)+1/2O2 (g)=CO (g)+2H2(g)△H1=-35.6kJ?molˉ1
试判断常温下,上述反应能否自发进行 (填“能”或“否”),有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2 (g)=CO 2(g)+2H2O(g)△H2=-890.3kJ?molˉ1
③CH4(g)+CO2 (g)=2CO (g)+2H2(g)△H3=247.3kJ?molˉ1
试结合反应①,确定下面热化学反应方程式中的△H值
CH4(g)+H2O (g)=CO (g)+3H2(g)△H= kJ?molˉ1
(2)恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/ | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
(3)希腊亚里斯多德大学的Marmellos和Stoukides用一种特殊的电解方法合成氨.即在常压下把氢气和用氦气稀释的氮气,分别通入到570℃的电解池中,用高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯多晶薄膜做电极,转化率高达78%.其实验装置如右图.阴极的电极反应式 .
(4)用标准盐酸标定某氨水的浓度时应该选择下列哪种指示剂最好 .
A.甲基橙 B.石蕊 C.酚酞
(Ⅱ) pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10ˉ3mol?Lˉ1,则pC=-lg(1×10ˉ3)=3.某温度下,H2CO3溶液的pC-pH关系如图.

请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为 ;
(2)求此温度下H2CO3
 H++HCO3ˉ 的电离平衡常数 ;
H++HCO3ˉ 的电离平衡常数 ;(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?Lˉ1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3ˉ
 H++CO32ˉ移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液 .
H++CO32ˉ移动,溶液中H+浓度变化不大.根据上述信息,确定氨水和氯化铵的混和溶液能不能形成缓冲溶液 . 查看习题详情和答案>>
查看习题详情和答案>>
| 实验操作 | 实验现象 | |
| 步骤1 | 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,过滤,将滤液分为若干份. | 有少量气泡产生,溶液的黄绿色褪去. |
| 步骤2 | 将第一份滤液与稀盐酸混合. | 产生大量气泡. |
| 步骤3 | 将第二份滤液加热. | 溶液变浑浊,且有大量无色气体产生. |
(2)步骤2、步骤3的实验目的都是
(3)请你设计-个简单的实验方案,证明步骤1所得滤液中的HClO浓度比饱和氯水中HClO浓度大:
Ⅱ.摩尔盐[(NH4)2SO4?FeSO4?6H2O]在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组按以下步骤制取摩尔盐:
①用30%的NaOH溶液和废铁屑混合、煮沸、冷却、分离;
②用①处理过的铁屑和稀H2SO4反应制取FeSO4;
③将②制得的FeSO4溶液与[(NH4)2SO4溶液混合,结晶得到摩尔盐.
试回答下列问题:
(1)如何从溶液中分解出摩尔盐?
(2)如何设计一个简单的实验证明得到的产品中有Fe2+?
(3)为了确定产品中亚铁离子的含量,某研究小组用KMnO4酸性溶液进行滴定,请写出该反应的离子方程式:
(4)现有等浓度的①(NH4)2CO3 ②(NH4)2SO4 ③(NH4)2Fe(SO4)2溶液,其中c(NH4+)由大到小的顺序是:
(1)粗食盐常含有少量Ca2+、Mg2+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
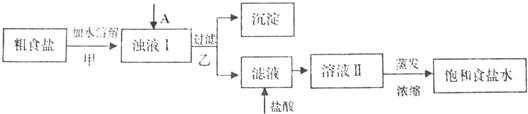
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液
(1)①欲除去浊液I中的Ca2+、Mg2+、SO42-离子,选出A所代表的试剂,按滴加顺序依次为
②加盐酸的目的是(用离子方程式表示)
③如果在实验室中完成下列过程,甲、乙两个过程均要用到玻璃棒,玻璃棒的作用分别是:
甲
(2)工业上用惰性电极电解饱和食盐水制取盐酸,写出电解饱和食盐水的化学方程式
| ||
| ||
(1)(4分)某无色透明溶液,跟金属铝反应放出H2 ,所得的溶液中可能存在下列离子:Cu2+、 Ba2+ 、H+、Ag+、SO42-、 SO32-、HCO3-、OH-、CO32- ,回答下列问题:
①所得溶液中含有Al3+时,该溶液中一定存在的其它离子是 ;
②所得溶液中含有AlO2―时,该溶液中一定存在的其它离子是___________。
(2)(18分)有5瓶白色固体试剂,分别是氯化钡、氢氧化钠、硫酸钠、硫酸铵、无水硫酸铜。现只提供蒸馏水,试管、试管夹和酒精灯,不能再使用其它仪器和药品,进行如下鉴别试验。
请填写下列空白:
①各取适量固体试剂分别装入5支试管中,加入适量蒸馏水,振荡试管。被检出的物质是(填化学式,下同)
②分别取少量未检出的溶液于试管中,往其中加入上述已检出的溶液,被检出的物质是 ,所发生反应的离子方程式是
③鉴别余下未检出物质的方法是_____ ________________,相应的离子方程式为 查看习题详情和答案>>工业生产的纯碱中常含有少量NaCl杂质。为测定某纯碱样品的纯度,化学课外活动小组设计了三种实验方案:
【方案一】取样品溶解后,加试剂使CO32-沉淀,测定沉淀的质量。
【方案二】用0.100 mol/L盐酸滴定。
【方案三】用稀酸将CO32-转化为CO2,测定CO2的质量。
解答31-34小题:
方案一的操作步骤有:①称量并溶解样品;②加入足量的BaCl2溶液;③过滤;④洗涤;⑤干燥;⑥称量并进行恒重操作。称量时所需定量实验仪器为____________________。判断是否达到恒重的标准是_____________________________________________________。
方案二的具体过程为:
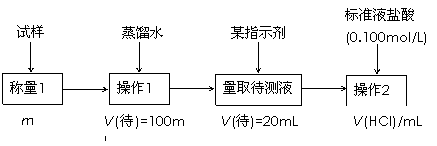 |
①操作1所需要的仪器有_____________________________________________。
②滴定时选择的指示剂为甲基橙。当溶液____________________________________时,说明达到了滴定终点。
③为减少偶然误差,通常的处理办法是_______________________________。
④滴定时若锥形瓶内有少量液体溅出,则测定结果_________。(选填“偏高”、“偏低”、“不影响”,下同),若盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗,测定结果_________。
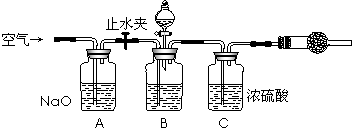 方案三的实验装置如下图:
方案三的实验装置如下图:
操作步骤有:①检查装置的气密性;②在干燥管内装满碱石灰,称量质量为W1 g;③称量W2 g样品装入广口瓶B中;④关闭止水夹;⑤缓慢加入稀H2SO4至不再产生气体为止;⑥ 打开止水夹;⑦缓缓鼓入空气数分钟,再称量干燥管,质量为W3 g。
该方案样品中纯碱的质量分数为__________________________(用代数式表示)。
上图中装置A的作用是_____________________。装置C的作用是_____________________。有同学认为空气中的水蒸气会进入干燥管导致测量结果_____________(填“偏大”、“偏小”或“无影响”)。改进措施可以是______________________________________________。
若用下图装置对样品进行分析,根据量瓶中收集到的液体的体积来计算样品中碳酸钠的含量。则下列装置中,最合理的是______。(选填序号)
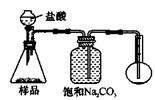
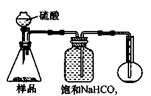
A B


C D
查看习题详情和答案>>