网址:http://m.1010jiajiao.com/timu_id_3769382[举报]
氨气作为一种重要的化工原料,主要用于生产氮肥、硝酸、纯碱、尿素等化工产品。下图是合成氨,并联合生产硝酸、纯碱、尿素的简要流程示意图:

反应体系中各组分的部分性质见下表:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210 | -253 | -78 |
| 沸点(℃) | -195 | -259 | -33 |
(1)设备A的名称是 ,副产物B的化学式是
(2)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度至少降低到 ℃(填具体温度),使 分离出来,循环使用的气体有 。
(3)已知尿素的结构简式为![]() 反应②的化学方程式是 。
反应②的化学方程式是 。
|
(5)已知:4NH3+3O2 ![]() 2N2 + 6H2O ,以此设计的氨燃料电池的负极电极反应式为_____________________________(电极材料均为惰性电极,KOH溶液作电解质溶液)。
2N2 + 6H2O ,以此设计的氨燃料电池的负极电极反应式为_____________________________(电极材料均为惰性电极,KOH溶液作电解质溶液)。
查看习题详情和答案>>
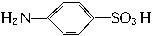
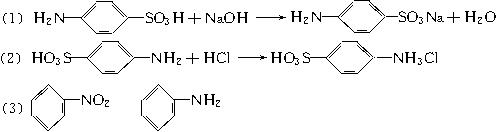 )是一种重要的化工原料,它具有两性,既能和氢氧化钠溶液反应,也可和盐酸反应。工业上常用苯为原料来合成对氨基苯磺酸。请回答下列问题:
)是一种重要的化工原料,它具有两性,既能和氢氧化钠溶液反应,也可和盐酸反应。工业上常用苯为原料来合成对氨基苯磺酸。请回答下列问题:(1)请写出对氨基苯磺酸和氢氧化钠溶液反应的化学方程式:_______________________。
(2)请写出对氨基苯磺酸和盐酸反应的化学方程式:_______________________________。
(3)已知下列(Ⅰ)—(Ⅳ)四个有机反应:
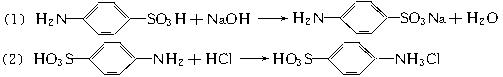
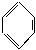
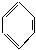
根据上述信息,试完成以下合成路线:
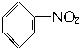
写出上述合成路线,A、B的结构简式A:____________,B:____________。
步骤(1)的反应条件是____________;上述(Ⅳ)反应是氧化反应还是还原反应?____________。
查看习题详情和答案>>氨气是一种重要的化工产品,是生产铵盐、尿素等的原料。工业合成氨的反应如下:N2(g) +3H2(g)  2NH3(g) △H=一92. 4 KJ·mol-1
2NH3(g) △H=一92. 4 KJ·mol-1
(1)2NH3(g)  N2(g) +3H2(g)在恒容密闭容器中达到平衡的标志有
N2(g) +3H2(g)在恒容密闭容器中达到平衡的标志有
①单位时间内生成3n mol H2:同时生成2n mol NH3②用NH3、N2、H2表示反应速率比为2∶1∶3 ③混合气体的密度不再改变 ④混合气体压强不再改变 ⑤混合气体平均相对分子质量不再改变
| A.①③④ | B.①②④⑤ | C.①④⑤ | D.②③④ |
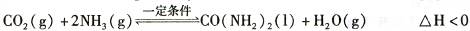
t℃时,向容积恒定为2L的密闭容器中加入0.10 molCO:和0. 40 molNH3 ,70 min开始达到平衡。反应中CO2 ( g)的物质的量随时间变化如下表所示:
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2) /mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
①20 min时,υ正(CO2 )_ 80 min时。υ逆(H2O)(填“>”、“=”或“<”)。
②在100 min时,保持其它条件不变,再向容器中充入0. 050 mo1CO2和0. 20 molNH3,重新建立平衡后CO2的转化率与原平衡相比将_ (填“增大”、“不变”或“减小”)。
③上述可逆反应的平衡常数为_ (保留二位小数)。
④根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图像;保持其它条件不变;则(t+10)℃下正确的图像可能是 (填图甲中的“A”或“B”)。
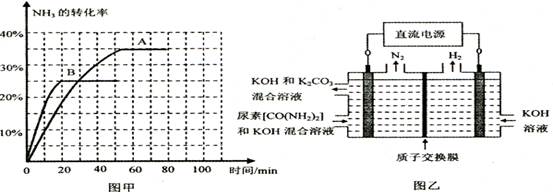
⑤图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素〔CO(NH2)2〕的碱性溶液制取氢气。该装置中阳极的电极反应式为 ,若两极共收集到气体22. 4L(标
况),则消耗的尿素为 g(忽略气体的溶解)。 查看习题详情和答案>>
(1)实验室制取氨气的化学方程式是
| ||
| ||
(2)①如图(1)是进行氨气喷泉实验的装置,引发喷泉的操作步骤是
②氨气使烧杯中溶液由无色变为红色,其原因是
(3)该小组同学设计了如图(2)所示的实验装置(部分夹持仪器未画出),探究氨气的还原性并检验产物.
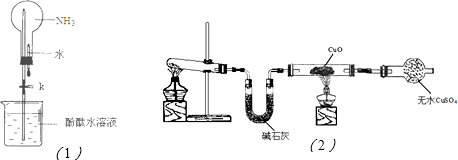
①实验现象为:黑色CuO变为红色;白色无水CuSO4粉末变为蓝色;同时生成一种无色气体,该气体无污染.请写出氨气与CuO反应的化学方程式
| ||
| ||
②碱石灰的作用是
③该装置存在明显缺陷,请指出存在的问题并提出改进意见
 ;
; ;
;(4)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O.已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+
| H+ |
(5)工业废气中的氮氧化物是主要的大气污染物之一.为了治理污染,工业上常用氨气与之发生反应:NOx+NH3→N2+H2O,使其转化为无毒的N2.现有NO2和NO的混合气体3.0L,跟3.4L(同温同压下)NH3反应,恰好使其全部转化为氮气,则原混合气体中,NO2与NO的体积比是