摘要:(三)在实际生产中.我国合成氨厂一般选用的压强在 之间. 合成氨如果采用较低温度.虽然有利于增大平衡混合气中氨的含量.但温度过低.反应速率太小.要很长时间才能使反应达到平衡状态.这对生产十分不利.加入催化剂是为了 .然而催化剂需要在一定的温度范围内才能表现出良好的催化活性.目前.合成氨工业普遍使用的是以 催化剂.这种催化剂又称为铁触媒.铁触媒在 的活性最大.
网址:http://m.1010jiajiao.com/timu_id_3767613[举报]
(2011?四川模拟)石油脱硫废气中含有硫化氢,为了有效防止污染,实现废物的综合利用,工业上采用下列工艺过程将硫化氢转化为硫酸和氢气等产品.
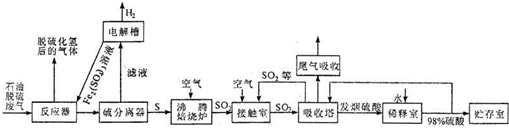
请回答下列问题:
(1)反应器中装有硫酸铁的酸性溶液,该溶液与硫化氢反应的离子方程式是
(2)滤液电解后,得到硫酸铁的酸性溶液,再将其返回到反应器中的目的是
(3)在实际生产中,二氧化硫转化为三氧化硫的适宜条件是:V2O5作催化剂、常压、400℃~500℃.如图是不同压强下该反应体系中温度与二氧化硫的平衡转化率变化曲线.
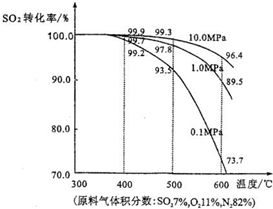
考虑工业生产效益并结合图示分析,选择400℃~500℃的原因是
选择常压的原因是
(4)工业上常用过量氨水吸收尾气中的二氧化硫,该反应的化学方程式是
(5)生产过程中,接触室生成的三氧化硫用98%的硫酸吸收,制得一种发烟硫酸(9H2SO4?SO3).某硫酸车间10小时消耗的硫为at,则平均每小时从吸收塔流出的该发烟硫酸为
t(在生产过程中硫的损失忽略不计).
查看习题详情和答案>>

请回答下列问题:
(1)反应器中装有硫酸铁的酸性溶液,该溶液与硫化氢反应的离子方程式是
2Fe3++H2S=2Fe2++2H++S↓
2Fe3++H2S=2Fe2++2H++S↓
.(2)滤液电解后,得到硫酸铁的酸性溶液,再将其返回到反应器中的目的是
使硫酸铁的酸性溶液循环使用
使硫酸铁的酸性溶液循环使用
.(3)在实际生产中,二氧化硫转化为三氧化硫的适宜条件是:V2O5作催化剂、常压、400℃~500℃.如图是不同压强下该反应体系中温度与二氧化硫的平衡转化率变化曲线.

考虑工业生产效益并结合图示分析,选择400℃~500℃的原因是
在此温度下,反应速率和平衡转化率都较高
在此温度下,反应速率和平衡转化率都较高
;选择常压的原因是
常压下,平衡转化率较高,且不会因加压造成设备造价和耗能增加
常压下,平衡转化率较高,且不会因加压造成设备造价和耗能增加
.(4)工业上常用过量氨水吸收尾气中的二氧化硫,该反应的化学方程式是
SO2+2NH3?H2O=(NH4)2SO3+H2O
SO2+2NH3?H2O=(NH4)2SO3+H2O
.(5)生产过程中,接触室生成的三氧化硫用98%的硫酸吸收,制得一种发烟硫酸(9H2SO4?SO3).某硫酸车间10小时消耗的硫为at,则平均每小时从吸收塔流出的该发烟硫酸为
| 481a |
| 304 |
| 481a |
| 304 |
(Ⅰ)多项选择题
下列关于化工生产的叙述正确的是 .
A.炼钢就是在高炉中用还原剂把铁从铁矿石中还原出来
B.离子交换膜法制碱工业中,氢氧化钠在电解槽的阴极区产生
C.工业制硫酸中,三氧化硫是在吸收塔内用98%的硫酸吸收
D.黏土是生产陶瓷、玻璃和水泥的共同原料
(Ⅱ)氨是重要的无机化工产品之一,在国民经济中占有重要地位.世界上的氨除少量从焦炉气中回收副产外,绝大部分是合成的氨.海南岛的南海北部湾莺歌海海域有着丰富的天然气气田,利用此资源在东方市八所港建有一家大型的合成氨化肥厂.
(1)写出该化肥厂生产H2的化学反应方程式 .
(2)在硫酸的工业生产中,往往会增大O2的比例来提高SO2的转化率,在合成氨生产中是否会采用相同的方法,请说明理由. .
(3)在制取原料气体的过程中,常混有一些杂质,在进入合成塔之前必须将杂质除去,原因是 .例如除去CO是先将其氧化成CO2,然后常用 吸收.
(4)下图是氨的产率与温度的关系,曲线1表示平衡时氨的产率,曲线2表示反应进行一段时间但还未达到平衡时氨的含量.请分析A点氨的含量小于B的原因 .在实际生产中,温度往往采用500℃而不用400℃的原因是 .
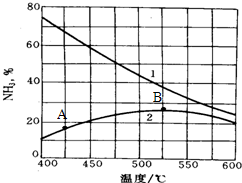
(5)在合成氨的生产过程中会产生大量CO2,该化肥厂与俄罗斯塔氏集团合作,利用这些CO2建设一个年产52万吨的小颗粒尿素加工厂,再进一步加工成氮磷钾复合肥,请写出该合成尿素反应的化学方程式 ,请写出该设计的优点 .
查看习题详情和答案>>
下列关于化工生产的叙述正确的是
A.炼钢就是在高炉中用还原剂把铁从铁矿石中还原出来
B.离子交换膜法制碱工业中,氢氧化钠在电解槽的阴极区产生
C.工业制硫酸中,三氧化硫是在吸收塔内用98%的硫酸吸收
D.黏土是生产陶瓷、玻璃和水泥的共同原料
(Ⅱ)氨是重要的无机化工产品之一,在国民经济中占有重要地位.世界上的氨除少量从焦炉气中回收副产外,绝大部分是合成的氨.海南岛的南海北部湾莺歌海海域有着丰富的天然气气田,利用此资源在东方市八所港建有一家大型的合成氨化肥厂.
(1)写出该化肥厂生产H2的化学反应方程式
(2)在硫酸的工业生产中,往往会增大O2的比例来提高SO2的转化率,在合成氨生产中是否会采用相同的方法,请说明理由.
(3)在制取原料气体的过程中,常混有一些杂质,在进入合成塔之前必须将杂质除去,原因是
(4)下图是氨的产率与温度的关系,曲线1表示平衡时氨的产率,曲线2表示反应进行一段时间但还未达到平衡时氨的含量.请分析A点氨的含量小于B的原因

(5)在合成氨的生产过程中会产生大量CO2,该化肥厂与俄罗斯塔氏集团合作,利用这些CO2建设一个年产52万吨的小颗粒尿素加工厂,再进一步加工成氮磷钾复合肥,请写出该合成尿素反应的化学方程式
(2011?江山市模拟)以黄铁矿为原料生产硫酸的主要设备是沸腾炉、(炉气精制)、接触室和吸收塔等.
(1)请写出炉气制造即沸腾炉中黄铁矿燃烧的化学方程式
 (2)炉气精制的作用是将含SO2进行除法和水洗.而精制炉气即SO2的催化氧化,在接触室中进行.
(2)炉气精制的作用是将含SO2进行除法和水洗.而精制炉气即SO2的催化氧化,在接触室中进行.
A、精制炉气(含SO2体积分数为7%、O2为11%、N2为82%)中SO2平衡转化率与温度及压强关系如图1所示.在实际生产中,SO2催化氧化反应的条件选择常压、450℃左右(对应图中A点),而没有选择SO2转化率更高的B或C点对应的反应条件,其原因分别是
B、接触室中2SO2(g)+O2(g)
2SO3(g),反应过程的能量变化如图2所示.
已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:
①图中C点表示
②反应达到平衡时,平衡常数表达式K=
,升高温度,K值
(3)从吸收塔出来的气体用一定量氨水吸收,得到的铵盐产品是(NH4)2SO3和NH4HSO3的混合物.取不同质量的铵盐,分别加入x mol/L的50.00mL NaOH溶液中,经沸水浴(此温度下铵盐自身不分解)加热使氨气全部逸出,干燥后用浓硫酸完全吸收.实验数据如下:
①该铵盐中(NH4)2SO3和NH4HSO3的物质的量之比为
②x的值为
查看习题详情和答案>>
(1)请写出炉气制造即沸腾炉中黄铁矿燃烧的化学方程式
4FeS2+11O2
2Fe2O3+4SO2
| ||
4FeS2+11O2
2Fe2O3+4SO2
.
| ||
 (2)炉气精制的作用是将含SO2进行除法和水洗.而精制炉气即SO2的催化氧化,在接触室中进行.
(2)炉气精制的作用是将含SO2进行除法和水洗.而精制炉气即SO2的催化氧化,在接触室中进行.A、精制炉气(含SO2体积分数为7%、O2为11%、N2为82%)中SO2平衡转化率与温度及压强关系如图1所示.在实际生产中,SO2催化氧化反应的条件选择常压、450℃左右(对应图中A点),而没有选择SO2转化率更高的B或C点对应的反应条件,其原因分别是
不选B点,因为压强越大对设备的投资大,消耗的动能大;SO2原料的转化率在1个大气压下的转化率已是97%左右,再提高压强,SO2的转化率提高的余地很小,所以采用1个大气压
不选B点,因为压强越大对设备的投资大,消耗的动能大;SO2原料的转化率在1个大气压下的转化率已是97%左右,再提高压强,SO2的转化率提高的余地很小,所以采用1个大气压
、不选择C点,因为温度越低,SO2转化率虽然更高,但催化剂的催化作用受影响,450℃时,催化剂的催化效率是高.故选择A点,不选C点.
不选择C点,因为温度越低,SO2转化率虽然更高,但催化剂的催化作用受影响,450℃时,催化剂的催化效率是高.故选择A点,不选C点.
.B、接触室中2SO2(g)+O2(g)
| ||
| △ |
已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:

①图中C点表示
生成物能量
生成物能量
,E的大小对该反应的反应热无
无
(填“有”或“无”) 影响.该反应通常用V2O5作催化剂,加V2O5会使图中B点降低
降低
(填“升高”或“降低”).②反应达到平衡时,平衡常数表达式K=
| c2(SO3) |
| c2(SO2)c(O2) |
| c2(SO3) |
| c2(SO2)c(O2) |
减小
减小
(填“增大”、“减小”或“不变”);图中△H=-198
-198
kJ?mol-1.(3)从吸收塔出来的气体用一定量氨水吸收,得到的铵盐产品是(NH4)2SO3和NH4HSO3的混合物.取不同质量的铵盐,分别加入x mol/L的50.00mL NaOH溶液中,经沸水浴(此温度下铵盐自身不分解)加热使氨气全部逸出,干燥后用浓硫酸完全吸收.实验数据如下:
| 实验次数 | 铵盐质量(g) | 浓硫酸增加的质量(g) |
| 第一次 | 1.570 | 0.340 |
| 第二次 | 3.140 | 0.680 |
| 第三次 | 4.710 | 0.510 |
| 第四次 | 6.280 | 0 |
2:1
2:1
.②x的值为
1.2
1.2
.