摘要:14.2008年初我国南方遭遇的冰雪灾害中.使用了一种融雪剂.其主要成分的化学式为XY2.X原子的结构示意图为 .X的阳离子与Y的阴离子的电子层结构相同.元素Z.W均为短周期元素.它们原子的最外层电子数均是其电子层数的2倍.Z与Y相邻且Z.W能形成一种WZ2型分子. (1)m= .该融雪剂的化学式为 . (2)Z.W元素的名称为 . . (3)下列说法正确的是 . A.XY2和WZ2都为离子化合物 B.XY2分子中仅含离子键.WZ2中仅含极性共价键 C.H2Z比HY的稳定性强 D.X的阳离子比Y的阴离子半径大 (4)下列化学用语表达正确的是 . A.XY2的电子式:X2+[ ?]2- B.WZ2的结构式:Z===W===Z C.Y元素的单质与H2Z水溶液反应的离子方程式为: Y2+Z2-===2Y-+Z↓ D.用电子式表示XY2的形成过程为: (5)冰雪的化学成分是H2O.水的沸点比H2Z的沸点高.其原因是 . 解析:(1)由X原子的结构示意图 可推知其为 .该元素为Ca.根据CaY2可知Y为-1价.又因为Y-与Ca2+的电子层结构相同.可知 Y为Cl. (2)Z.W原子的最外层电子数是其电子层数的2倍.则Z.W是C或S.Z与Y相邻则Z是S.W是C. (3)CaCl2是仅含离子键的离子化合物.CS2是仅含极性键的共价化合物.A错误.B正确,S的非金属性弱于Cl.则H2S的稳定性比HCl弱.C错误.Ca2+.Cl-具有相同的电子层结构.但Ca元素的核电荷数大.离子半径小.D错误. (4)XY2为CaCl2.其电子式为[? ?]-Ca2+[? ?]-.H2S的水溶液为弱酸.应写成分子式.即Cl2+H2S===2H++2Cl-+S↓.A.C错误. (5)氢键影响物质的熔沸点.使水的沸点升高. 答案:(1)20 CaCl2 B.D (5)水分子间存在氢键
网址:http://m.1010jiajiao.com/timu_id_3760704[举报]
2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图
X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=
(2)Z、W元素的名称为
(3)下列说法正确的是
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是
A.XY2的电子式:
B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-═2Y-+Z↓
D.用电子式表示XY2的形成过程为:
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是
查看习题详情和答案>>

X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=
20
20
,该融雪剂的化学式为CaCl2
CaCl2
.(2)Z、W元素的名称为
硫
硫
、碳
碳
.(3)下列说法正确的是
B
B
.A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是
BD
BD
.A.XY2的电子式:

B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-═2Y-+Z↓
D.用电子式表示XY2的形成过程为:

(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是
水分子中含有氢键
水分子中含有氢键
.2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图

X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=______,该融雪剂的化学式为______.
(2)Z、W元素的名称为______、______.
(3)下列说法正确的是______.
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是______.
A.XY2的电子式:

B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-═2Y-+Z↓
D.用电子式表示XY2的形成过程为:

(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是______.
查看习题详情和答案>>

X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=______,该融雪剂的化学式为______.
(2)Z、W元素的名称为______、______.
(3)下列说法正确的是______.
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是______.
A.XY2的电子式:

B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-═2Y-+Z↓
D.用电子式表示XY2的形成过程为:

(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是______.
2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图
X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=______,该融雪剂的化学式为______.
(2)Z、W元素的名称为______、______.
(3)下列说法正确的是______.
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是______.
A.XY2的电子式:
B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-═2Y-+Z↓
D.用电子式表示XY2的形成过程为:
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是______.
查看习题详情和答案>>

X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=______,该融雪剂的化学式为______.
(2)Z、W元素的名称为______、______.
(3)下列说法正确的是______.
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是______.
A.XY2的电子式:

B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-═2Y-+Z↓
D.用电子式表示XY2的形成过程为:

(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是______.
查看习题详情和答案>>
2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图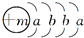
X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=______,该融雪剂的化学式为______.
(2)Z、W元素的名称为______、______.
(3)下列说法正确的是______.
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是______.
A.XY2的电子式:
B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-═2Y-+Z↓
D.用电子式表示XY2的形成过程为:
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是______.
查看习题详情和答案>>
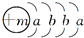
X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=______,该融雪剂的化学式为______.
(2)Z、W元素的名称为______、______.
(3)下列说法正确的是______.
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是______.
A.XY2的电子式:

B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-═2Y-+Z↓
D.用电子式表示XY2的形成过程为:

(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是______.
查看习题详情和答案>>
在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子.
(1)该融雪剂的化学式是
 .
.
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,D与E能形成一种对称分子,该分子的结构式为
(3)元素W与Y同周期,其氧化物可作为太阳能电子板的材料;元素Z的单质分子Z2中由3个共价键; W与Z能形成一种新型无机非金属材料,其化学式是
(4)W的氧化物是玻璃的主要成分,易与烧碱反应,该反应的化学方程式为
查看习题详情和答案>>
(1)该融雪剂的化学式是
CaCl2
CaCl2
;X的氢氧化物的电子式是

(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,D与E能形成一种对称分子,该分子的结构式为
S=C=S
S=C=S
. (3)元素W与Y同周期,其氧化物可作为太阳能电子板的材料;元素Z的单质分子Z2中由3个共价键; W与Z能形成一种新型无机非金属材料,其化学式是
Si3N4
Si3N4
. (4)W的氧化物是玻璃的主要成分,易与烧碱反应,该反应的化学方程式为
SiO2+2NaOH=Na2SiO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
.