摘要: > . > (2) < . >
网址:http://m.1010jiajiao.com/timu_id_3760385[举报]
用“>”、“<”或“=”填写下列空格:
(1)离子半径:Al3+
(2)酸性:H2SO4
(3)键的极性:H-F
(4)晶体的熔点:Si
(5)沸点:H2O
(6)原子的核外电子排布中,未成对电子数:24Cr
(7)元素的电子构型为ns2np3,B元素的电子构型为ns2np4,第一电离能:A
查看习题详情和答案>>
(1)离子半径:Al3+
<
<
Na+ (2)酸性:H2SO4
>
>
H2SeO4(3)键的极性:H-F
>
>
H-O (4)晶体的熔点:Si
<
<
SiC(5)沸点:H2O
>
>
H2S(6)原子的核外电子排布中,未成对电子数:24Cr
>
>
25Mn(7)元素的电子构型为ns2np3,B元素的电子构型为ns2np4,第一电离能:A
>
>
B.用“>”、“<”或“=”填空:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),光照和点燃条件的△H(化学计量数相同)分别为△H1、△H2,△H1
(2)相同条件下,2mol氢原子所具有的能量
(3)已知常温时红磷比白磷稳定,比较下列反应中△H的大小:△H1
①4P(白磷,s)+5O2(g)=2P2O5(s)△H1,
②4P(红磷,s)+5O2(g)=2P2O5(s)△H2;
(4)已知:101kPa时,2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1,则碳的燃烧热数值
(5)已知:稀溶液中,H+(aq)+OH (aq)=H2O(l)△H=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应生成1mol水,放出的热量
(6)可逆反应:aA(气)+bB(气)?cC(气)+dD(气);△H=Q,根据图回答:

①P1
查看习题详情和答案>>
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),光照和点燃条件的△H(化学计量数相同)分别为△H1、△H2,△H1
=
=
△H2;(2)相同条件下,2mol氢原子所具有的能量
>
>
1mol氢分子所具有的能量;(3)已知常温时红磷比白磷稳定,比较下列反应中△H的大小:△H1
<
<
△H2.①4P(白磷,s)+5O2(g)=2P2O5(s)△H1,
②4P(红磷,s)+5O2(g)=2P2O5(s)△H2;
(4)已知:101kPa时,2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1,则碳的燃烧热数值
>
>
110.5kJ?mol-1;(5)已知:稀溶液中,H+(aq)+OH (aq)=H2O(l)△H=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应生成1mol水,放出的热量
>
>
57.3kJ;(6)可逆反应:aA(气)+bB(气)?cC(气)+dD(气);△H=Q,根据图回答:

①P1
<
<
P2; ②(a+b)<
<
(c+d); ③t1℃>
>
t2℃.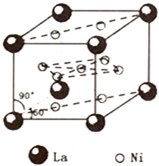 <化学--选修3:物质结构>
<化学--选修3:物质结构>镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用.
(1)Ni在元素周期表中的位置是
(2)镍易形成配合物,如:Ni(CO)4、[Ni(NH3)6]2+ 等.写出一种与配体CO互为等电子体的阴离子
(3)镍常见化合价为+2、+3,在水溶液中通常只以+2 价离子的形式存在.+3价的镍离子具有很强的氧化性,在水中会与水或酸根离子迅速发生氧化还原反应.Ni3+的电子排布式为
(4)镍和镧(
139 57 |