摘要:d (2)小于,醇分子可与水分子形成氢键.溴代烃分子不能与水分子形成氢键. (3)下层 c (6)平衡向生成溴乙烷的方向移动 解析:(1)在溴乙烷和1-溴丁烷的制备实验中.最不可能用到的是仪器d.即布氏漏斗.因其是用于过滤的仪器.即不可能用作反应容器.也不可能用于量取液体. (2)溴代烃的水溶性小于相应的醇.因为醇分子可与水分子形成氢键.溴代烃分子不能与水分子形成氢键. (3)根据题干表格数据:1-溴丁烷的密度大于水的密度.因此将1-溴丁烷的粗产品置于分液漏斗中加水.振荡后静置.产物即1-溴丁烷应在下层. (4)由于浓硫酸在稀释时放出大量的热且具有强氧化性.因此在制备操作过程中.加入的浓硫酸必须进行稀释.其目的是防止放热导致副产物烯或醚的生成并减小HBr的挥发.同时也减少Br2的生成 (5)除去溴代烷中少量杂质Br2反应可用c即NaHSO4.二者可以发生氧化还原反应而除去Br2.NaI能与Br2反应生成I2而引入新的杂质,NaOH不但能与Br2反应.同时也能与溴代烷反应,KCl都不反应.因此.a.b.d都不适合. (6)根据平衡移动原理.蒸出产物平衡向有利于生成溴乙烷的方向移动,在制备1-溴丁烷是不能采用此方法.原因是1-溴丁烷与正丁醇的沸点差较小.若边反应边蒸.会有较多的正丁醇被蒸出. 反馈“小练习
网址:http://m.1010jiajiao.com/timu_id_3757474[举报]
(2008?江苏模拟)为了除去NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理(反应方程式:3NO2+2NaOH→NaNO3+NaNO2+H2O;NO2+NO+2NaOH→2NaNO2+H2O).现有由amolNO、bmolNO2、cmolN2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为( )
(2008?江苏)工业上制备BaCl2的工艺流程图如下: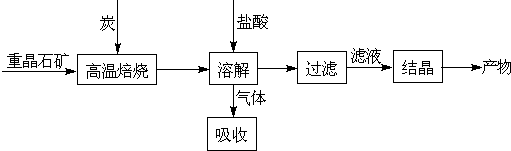
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验.查表得
BaSO4(s)+4C(s)
4CO(g)+BaS(s)△H1=571.2kJ?mol-1 ①
BaSO4(s)+2C(s)
2CO2(g)+BaS(s)△H2=226.2kJ?mol-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠.Na2S水解的离子方程式为
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
=
(3)反应C(s)+CO2(g)
2CO(g)的△H2=
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是
查看习题详情和答案>>

某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验.查表得
BaSO4(s)+4C(s)
| ||
BaSO4(s)+2C(s)
| ||
(1)气体用过量NaOH溶液吸收,得到硫化钠.Na2S水解的离子方程式为
S2-+H2O HS-+OH-;HS-+H2O
HS-+OH-;HS-+H2O H2S+OH-
H2S+OH-
S2-+H2O HS-+OH-;HS-+H2O
HS-+OH-;HS-+H2O H2S+OH-
H2S+OH-
;(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
| c(Br-) |
| c(Cl-) |
2.7×10-3
2.7×10-3
;[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10](3)反应C(s)+CO2(g)
| ||
172.5
172.5
kJ?mol-1;(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是
使BaSO4得到充分的还原(或提高BaS的产量),①②为吸热反应,炭和氧气反应放热维持反应所需高温.
使BaSO4得到充分的还原(或提高BaS的产量),①②为吸热反应,炭和氧气反应放热维持反应所需高温.
.(2008?江苏)将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2
2SO3(正反应放热).反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积).(计算结果保留一位小数)
请回答下列问题:
(1)判断该反应达到平衡状态的标志是
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)求该反应达到平衡时SO2的转化率(用百分数表示).
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?
查看习题详情和答案>>
| 催化剂 | △ |
请回答下列问题:
(1)判断该反应达到平衡状态的标志是
bc
bc
.(填字母)a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是
b
b
.(填字母)a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)求该反应达到平衡时SO2的转化率(用百分数表示).
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?