摘要:11.某同学设计了如图所示的方法.鉴定盐A的组成成分.由此分析.下列结论中正确的是 A.A中一定有Fe3+ B.C中一定有Fe3+ C.B为AgI沉淀 D.A一定为FeBr2溶液 12.可用如图装置制取.净化.收集的气体是 A.铜与稀硝酸制一氧化氮 B.二氧化锰与双氧水制氧气 C.锌和稀硫酸制氢气 D.硫化亚铁与稀硫酸制硫化氢
网址:http://m.1010jiajiao.com/timu_id_3756977[举报]
黄铜矿是工业炼铜的主要原料,主要成分为CuFeS2,含少量脉石.为测定该黄铜矿的纯度,某同学设计了如图所示实验:
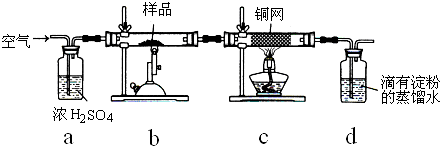
现用电子天平称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的
置于锥形瓶中,用0.05mol?L-1标准碘溶液进行滴定,消耗标准碘溶液20.00mL.请回答下列问题:
(1)将样品研细后再进行反应,其目的是 ;标准碘溶液应盛放在(填“碱式”或“酸式”) 滴定管中.
(2)装置a的作用是 .
A.除去空气中的二氧化碳
B.除去空气中的水蒸气
C.有利于气体混合
D.有利于观察、控制空气流速
(3)若去掉c装置,会使测定结果(填“偏低”、“偏高”或“无影响”) ,写出影响测定结果的化学方程式 .
(4)上述反应结束后,仍需通一段时间的空气,其目的是 .
(5)通过计算可知,该黄铜矿的纯度为 .
(6)假设实验操作均正确,测得的黄铜矿纯度仍然偏低,可能的原因主要有 .
查看习题详情和答案>>

现用电子天平称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的
| 1 | 10 |
(1)将样品研细后再进行反应,其目的是
(2)装置a的作用是
A.除去空气中的二氧化碳
B.除去空气中的水蒸气
C.有利于气体混合
D.有利于观察、控制空气流速
(3)若去掉c装置,会使测定结果(填“偏低”、“偏高”或“无影响”)
(4)上述反应结束后,仍需通一段时间的空气,其目的是
(5)通过计算可知,该黄铜矿的纯度为
(6)假设实验操作均正确,测得的黄铜矿纯度仍然偏低,可能的原因主要有
 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:(1)若A为水,B为过氧化钠,C中盛有盐酸酸化过的FeCl2溶液,旋开活塞E后,B中发生反应的化学方程式为
2Na2O2+2H2O=4NaOH+O2
2Na2O2+2H2O=4NaOH+O2
;C中现象为变黄或加深
变黄或加深
.(2)若A为硫酸,B为亚硫酸钠固体,C中盛有氢硫酸溶液,旋开活塞E后,B中发生反应的化学方程式的为
H2SO4+Na2SO3=Na2SO4+H2O+SO2
H2SO4+Na2SO3=Na2SO4+H2O+SO2
,C中发生反应的化学方程式的为2H2S+SO2=3S+2H2O
2H2S+SO2=3S+2H2O
.(3)利用上述装置还可以验证物质的性质,如设计证明氧化性:KClO3>Cl2>Br2,则A中加浓盐酸,B中加
KClO3
KClO3
,C中发生反应的离子方程式为2Br-+Cl2=2Cl-+Br2
2Br-+Cl2=2Cl-+Br2
. 国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:
国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:(1)该废液中可能大量存在的一种阴离子是
D
D
(选填序号)?A.SO42- B.CO32- C.Cl- D.NO3-
(2)经检测废液中铝元素的含量较高,需将其与其他三种离子分开,请选用合适的试剂,写出铝元素与该试剂反应时的离子方程式:
Al3++4OH-=AlO2-+2H2O
Al3++4OH-=AlO2-+2H2O
.(3)为了回收废液中的金属银,某同学设计了如图所示的方案.若依该方案获得金属银10.80g,为保证不污染环境和Cl2的循环利用,理论上应提供标准状况下的H2体积为
1.12
1.12
L.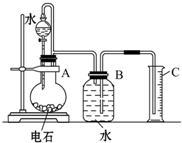 某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.
某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.(1)烧瓶中发生反应的化学方程式为
CaC2+2H2O→Ca(OH)2+C2H2↑
CaC2+2H2O→Ca(OH)2+C2H2↑
.装置B、C的作用是装置B用于贮水以便烧瓶中生成的C2H2气体进入B时排出与它等体积的水进入量筒C来测定生成乙炔的量;
装置B用于贮水以便烧瓶中生成的C2H2气体进入B时排出与它等体积的水进入量筒C来测定生成乙炔的量;
.(2)分液漏斗与烧瓶间用乳胶管连接的目的是
便于液体顺利滴下
便于液体顺利滴下
.(3)所用电石质量不能太大,否则
生成C2H2太多超过B的空间
生成C2H2太多超过B的空间
;也不能太小,否则无法测定其体积测定误差会更大
无法测定其体积测定误差会更大
;若容器B的容积为250mL,则所用电石的质量应在0.60
0.60
g左右(从后面数据中选填:0.03、0.60、1.00、1.50、2.00).(4)为了得到比较平稳的乙炔气流,实验室通常用
饱和食盐水
饱和食盐水
代替水进行实验.(5)实验中测得排入量筒中水的体积为VL、电石的质量为Wg.则电石中碳化钙的质量分数是
| 0.29V |
| W |
| 0.29V |
| W |
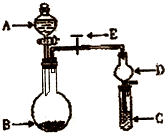 (2010?临沂一模)化学实验中一套装置往往可以完成多个实验,A某同学设计了如图所示装置(夹持仪器省略)进行系列实验.请回答:
(2010?临沂一模)化学实验中一套装置往往可以完成多个实验,A某同学设计了如图所示装置(夹持仪器省略)进行系列实验.请回答:(1)指出下列仪器的名称:
A
分液漏斗
分液漏斗
;D
干燥管
干燥管
.(2)若A中为浓氨水,B中为烧碱,C中为AICl3溶液,实验中可观测到B中有气体生成,C中有白色沉淀.则C中发生反应的离子方程式为
Al3++3NH3?H2O═Al(OH)3+3NH4+
Al3++3NH3?H2O═Al(OH)3+3NH4+
,仪器D的作用为防止倒吸
防止倒吸
.(3)若A中装有浓盐酸,B中装有固体KMn04,C中盛有KI淀粉溶液,实验中可观测到B中出现黄绿色气体,C中溶液变蓝.依据实验现象可以得到的结论为:
删除此空
删除此空
;氧化性由强到弱的顺序:
KMnO4>Cl2>I2
KMnO4>Cl2>I2
;但该装置的不足之处是:
缺少尾气吸收装置
缺少尾气吸收装置
.