网址:http://m.1010jiajiao.com/timu_id_3756574[举报]
已知反应①:CO(g)+CuO(s)??CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)  Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)  CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1=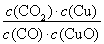
B.反应③的平衡常数K=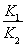
C.对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值
D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看习题详情和答案>>
已知反应①:CO(g)+CuO(s)??CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)  Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)  CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1= |
B.反应③的平衡常数K= |
| C.对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值 |
| D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小 |
 CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的是
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟利昂排放
c.多步行或乘公交车,少用私家车
d.将工业废气用碱液吸收后再排放
(2)有学者设想以如图所示装置用电化学原理将CO2、SO2转化为重要化工原料.
①若A为CO2,B为H2,C为CH3OH,则正极的电极反应式为
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为
当电路中有1mole-流过,正极区溶液中的H+的物质的量的变化量△n(H+)=
(3)在研究氮的氧化物的转化时,某小组查阅到以下数据:17℃、1.01×l05Pa时,2NO2(g)?N2O4(g)△H<0的平衡常数K=13.3.
①若该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol?L-1,则c(N2O4)=
②若改变上述体系的某一个条件,达到新的平衡后,测得混合气体中c(NO2)=0.04mol?L-1,c(N2O4)=0.007mol?L-1,则改变的条件为
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料.
①由CO和H2合成甲醇的方法是CO(g)+2H2(g)?CH3OH(g),己知该反应在300°C时的化学平衡常数为0.27,该温度下将2mol CO、3mol H2利2molCH3OH(g)充入容积为2L的密闭容器中,此时反应将
②己知:
a.用合成气(CO和H2)生产甲醇(CH3OH),合成1mol CH3OH(l)吸收热量131.9kJ
b.2H2(g)+CO(g)+
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
(16分)化工工业中常用乙苯脱氢的方法制备苯乙烯。
(1)已知某温度下:
反应①:CO2(g) +H2 (g)→CO(g) + H2O(g),ΔH= +41.2 kJ/mol
反应②: 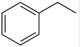 (g)→
(g)→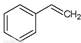 (g)+H2(g),ΔH=" +117.6" kJ/mol
(g)+H2(g),ΔH=" +117.6" kJ/mol
②的化学反应平衡常数分别为K1、K2。
请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式 。该反应的化学平衡常数K= (用K1、K2表示)。
(2)对于反应①,恒温恒容条件下,向密闭容器中加入2molCO2和2molH2,当反应达到平衡后,以下说法正确的是 。
| A.因为该反应是吸热反应,所以升高温度,正反应速率增大,逆反应速率减小; |
| B.若继续加入1molCO2、1mol H2,平衡向正反应方向移动; |
| C.若继续通入1mol CO2则平衡向正反应方向移动,CO2的转化率增大; |
| D.压缩体积,平衡不移动,反应物和产物的浓度都不变; |
(4)已知某温度下, Ag2SO4(M=312g/mol)的溶解度为0.624g/100g H2O,该温度下Ksp(Ag2SO4)= ;(两位有效数字)
(5)电解法制备高铁酸钠(Na2FeO4),总反应式为:Fe+2H2O+2OH- = FeO42-+3H2,电解质溶液选用NaOH溶液。该电解池阳极材料是 (写化学式) ;阳极的电极反应式为: 。 查看习题详情和答案>>
(12分)化学平衡原理在工农业生产中发挥着重要的指导作用。
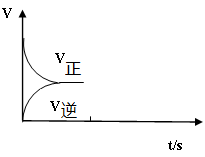
(1)反应C(s)+CO2(g)
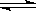 2CO(g)平衡常数K的表达式为
;
2CO(g)平衡常数K的表达式为
;
已知C(s) +
H2O(g)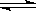 CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)
CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g) 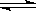 CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为
。
CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为
。
(2) 已知某温度下,反应2SO2+O2 2SO3,的平衡常数K=19
2SO3,的平衡常数K=19
在该温度下的体积固定的密闭容器中充入C(SO2)=1mol·L-1,C(O2)=1 mol·L-1,当反应在该温度下SO2转化率为80%时,该反应 (填“是”或“否”)达到化学平衡状态,若未达到,向 (填“正反应”或“逆反应”) 方向进行。
(3)对于可逆反应:aA(g) +bB(g) cC(g)+dD(g)
△H = a kJ·mol-1;
cC(g)+dD(g)
△H = a kJ·mol-1;
若a+b>c+d,增大压强平衡向_______(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则a_______0(填“>”或“<”)
查看习题详情和答案>>