摘要:现有一氯化钠样品中混有少量碳酸钠.现用下面两种方法进行提纯.方法一.取样品溶于蒸馏水.加稍过量的盐酸蒸干溶液.方法二.取样品溶于蒸馏水.加稍过量石灰水.过滤.向滤液中加稍过量的盐酸.蒸干溶液.试评价这两种方法.(物质提纯的过程要点:①加入的物质不能与成份物质发生反应,②不能引进新的杂质,③操作尽可能简单易行.) 答:从提纯的原则来看.方法一可行.而方法二最大的不足是在提纯过程中带进了新的杂质CaCl2.加过量Ca(OH)2.可使碳酸钠转变为氢氧化钠和碳酸钙.通过过滤除去碳酸钙.多出过量的氢氧化钙和氢氧化钠.加入稀盐酸后.能除去碳酸钠的同时又带进了新杂质氯化钙.方法二不可行.也不如方法一简便.
网址:http://m.1010jiajiao.com/timu_id_3755157[举报]
氯化钠和碳酸钠都是生活中常见的物质,实验室有一瓶混有少量碳酸钠杂质的氯化钠样品,为了除去其中的杂质,某兴趣小组最初设计了如下方案并进行试验.

(1)写出沉淀A的化学式
(2)加入CaCl2溶液后,分离除去沉淀A的实验操作方法是
(3)在实验过程中,兴趣小组的同学又发现了新问题:此方案很容易引入新的杂质,请写出固体物质B的成分 (用化学式表示)
(4)兴趣小组的同学讨论后提出新的方案:将混合物溶解,若滴加某溶液至不再产生气体为止,则既能除去Na2CO3杂质,又能有效的防止新杂质的引入.请写出有关反应的化学方程式:
(5)兴趣小组的同学利用新方案得到了纯净的氯化钠固体.现要配置1000g溶质质量分数为15%的氯化钠溶液,其正确的操作步骤是 (填序号)
A.溶解、过滤、结晶 B.计算、称量、溶解 C.称量、溶解、过滤、称量、计算. 查看习题详情和答案>>

(1)写出沉淀A的化学式
(2)加入CaCl2溶液后,分离除去沉淀A的实验操作方法是
(3)在实验过程中,兴趣小组的同学又发现了新问题:此方案很容易引入新的杂质,请写出固体物质B的成分 (用化学式表示)
(4)兴趣小组的同学讨论后提出新的方案:将混合物溶解,若滴加某溶液至不再产生气体为止,则既能除去Na2CO3杂质,又能有效的防止新杂质的引入.请写出有关反应的化学方程式:
(5)兴趣小组的同学利用新方案得到了纯净的氯化钠固体.现要配置1000g溶质质量分数为15%的氯化钠溶液,其正确的操作步骤是 (填序号)
A.溶解、过滤、结晶 B.计算、称量、溶解 C.称量、溶解、过滤、称量、计算. 查看习题详情和答案>>
某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下:①按图连接装置,并检查气密性;②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量为83.4g;③准确称得6g纯碱样品放入容器b中;④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6g.试回答:

(1)若④⑤两步的实验操作太快,则会导致测定结果 (填“偏大”或“偏小”);
(2)鼓入空气的目的是 ,装置A中试剂X应选用 ;
(3)若没有C装置,则会导致测定结果 (填“偏大”或“偏小”);
(4)E装置的作用是 ;
(5)根据实验中测得的有关数据,计算出纯碱样品Na2CO3的质量分数为 (计算结果保留一位小数).
查看习题详情和答案>>

(1)若④⑤两步的实验操作太快,则会导致测定结果
(2)鼓入空气的目的是
(3)若没有C装置,则会导致测定结果
(4)E装置的作用是
(5)根据实验中测得的有关数据,计算出纯碱样品Na2CO3的质量分数为
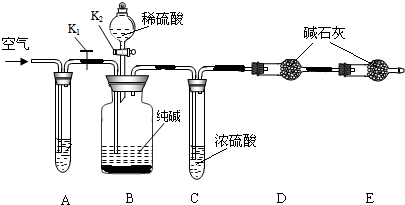
某纯碱样品中含有少量氯化钠杂质,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).

实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量为83.4g;
③准确称得6g纯碱样品并放入容器B中;
④关上K1,打开K2,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤关上K2,打开K1,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6g.
试回答:
(1)已知装置A中试剂为碱性溶液,其作用是 .
(2)实验步骤⑤鼓入空气的目的是 .
(3)C装置的作用是 ,若没有C装置,则会导致测定结果 (填“偏大”或“偏小”).
(4)E装置的作用是 .
(5)根据实验中测得的有关数据,计算出纯碱样品碳酸钠的质量分数为 %(计算结果保留一位小数).
(6)经精确测定,样品中碳酸钠的实际质量分数略小于上述所求数值,其原因可能是 .
查看习题详情和答案>>

实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量为83.4g;
③准确称得6g纯碱样品并放入容器B中;
④关上K1,打开K2,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤关上K2,打开K1,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6g.
试回答:
(1)已知装置A中试剂为碱性溶液,其作用是
(2)实验步骤⑤鼓入空气的目的是
(3)C装置的作用是
(4)E装置的作用是
(5)根据实验中测得的有关数据,计算出纯碱样品碳酸钠的质量分数为
(6)经精确测定,样品中碳酸钠的实际质量分数略小于上述所求数值,其原因可能是
碳酸钠,化学式Na2CO3,俗称纯碱.“纯碱中常常会混有少量的氯化钠”.某研究性学习小组以一包纯碱(若有杂质,只考虑为氯化钠)为研究对象,探究该纯碱样品中碳酸钠的含量.请你参与他们的活动.
【小组讨论】
观点Ⅰ:纯碱样品中只含有碳酸钠
观点Ⅱ:纯碱样品是由碳酸钠和少量氯化钠组成的混合物
【实验设计】
甲方案
Ⅰ设计思路:根据样品与石灰水反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ操作步骤:称取13.25g纯碱样品,加入过量的澄清石灰水,充分搅拌.过滤、洗涤、干燥,得到白色沉淀10.00g
Ⅲ数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数.
计算过程:
Ⅳ实验结论: .
乙方案
Ⅰ设计思路:根据样品(质量为a g)与稀硫酸完全反应生成二氧化碳的质量(质量为b g),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ实验结论:
(1)当a、b的质量关系满足 (填写含a、b字母的表达式,下同)时,纯碱样品中只含有碳酸钠,样品中碳酸钠的质量分数是100%.
(2)当a、b的质量关系满足 时,纯碱样品是由碳酸钠和少量氯化钠组成的混合物,样品中碳酸钠的质量分数是 .
【实验评价】
误差分析:(1)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小.
(2)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比 (填写“偏大”、“偏小”或“不变”).
【交流反思】
(1)实验过程中,需用玻璃棒不断搅拌,该操作的目的是 .
(2)甲方案实验操作中,对沉淀洗涤的目的是: .
(3)乙方案中,需用一定质量的19.6%的稀硫酸.现有一瓶98%的浓硫酸(密度为1.84g/cm3),配制乙方案中实验所用稀硫酸,至少需要浓硫酸的体积是 mL(填写含字母的表达式).浓硫酸稀释的正确操作是 .
查看习题详情和答案>>
【小组讨论】
观点Ⅰ:纯碱样品中只含有碳酸钠
观点Ⅱ:纯碱样品是由碳酸钠和少量氯化钠组成的混合物
【实验设计】
甲方案
Ⅰ设计思路:根据样品与石灰水反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ操作步骤:称取13.25g纯碱样品,加入过量的澄清石灰水,充分搅拌.过滤、洗涤、干燥,得到白色沉淀10.00g
Ⅲ数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数.
计算过程:
Ⅳ实验结论:
乙方案
Ⅰ设计思路:根据样品(质量为a g)与稀硫酸完全反应生成二氧化碳的质量(质量为b g),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ实验结论:
(1)当a、b的质量关系满足
(2)当a、b的质量关系满足
【实验评价】
误差分析:(1)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小.
(2)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比
【交流反思】
(1)实验过程中,需用玻璃棒不断搅拌,该操作的目的是
(2)甲方案实验操作中,对沉淀洗涤的目的是:
(3)乙方案中,需用一定质量的19.6%的稀硫酸.现有一瓶98%的浓硫酸(密度为1.84g/cm3),配制乙方案中实验所用稀硫酸,至少需要浓硫酸的体积是