摘要:22.某反应过程中的能量变化如图所示: (1)写出该反应的热化学方程式: . (2)在溶液中进行化学反应中的物质.其状态标为“aq .已知0.5 mol H2SO4在溶液中与足量氢氧化钠反应放出57.3 kJ的热量.用离子方程式写出该反应的热化学方程式: . (3)合成氨反应的热化学方程式: N2 ΔH=-92.2 kJ/mol 已知合成氨反应是一个反应物不能完全转化为生成物的反应.在某一定条件下.N2的转化率仅为10%.要想通过该反应得到92.2 kJ的热量.至少在反应混合物中要投放N2的物质的量为 mol. 解析:(1)由图可知.反应物总能量高于生成物总能量.可判断所给反应是一个放热反应.据图可写出反应的热化学方程式. (3)据热化学方程式可知.1 mol N2完全反应才能得到92.2 kJ的热量.而N2转化率为10%.则实际需要投入10 mol N2才能转化1 mol N2. 答案:+3D(l) ΔH=-432 kJ/mol ===H2O(l) ΔH=-57.3 kJ/mol (3)10
网址:http://m.1010jiajiao.com/timu_id_3753758[举报]
(1)某反应过程中的能量变化如图所示: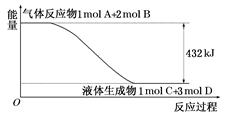
写出该反应的热化学方程式: 。
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ的热量,其热化学方程式为 。
(1)某反应过程中的能量变化如下图所示:

写出该反应的热化学方程式____________________________。
(2)在溶液中进行的化学反应的物质,其状态标为“aq”,已知含0.2 mol HCl的溶液与足量氢氧化钠溶液反应放出11.46 kJ的热量,用离子方程式写出中和热的热化学方程式________________________________。
查看习题详情和答案>>
(2)在溶液中进行的化学反应的物质,其状态标为“aq”,已知含0.2 mol HCl的溶液与足量氢氧化钠溶液反应放出11.46 kJ的热量,用离子方程式写出中和热的热化学方程式________________________________。
(1)某反应过程中的能量变化如下图所示:

写出该反应的热化学方程式_____________________________________________。
(2)在溶液中进行的化学反应的物质,其状态标为“aq”,已知含0.2 mol HCl的溶液与足量氢氧化钠溶液反应放出11.46 kJ的热量,用离子方程式写出中和热的热化学方程式____________________________________________________________________。
查看习题详情和答案>>(1)某反应过程中的能量变化如下图所示:

写出该反应的热化学方程式________.
(2)在溶液中进行的化学反应的物质,其状态标为“aq”,已知含0.2 mol HCl的溶液与足量氢氧化钠溶液反应放出11.46 kJ的热量,用离子方程式写出中和热的热化学方程式________.
某反应在反应过程中的能量变化如图所示(图中E1表示反应物总能量,E2表示生成物总能量)。下列有关叙述正确的是( )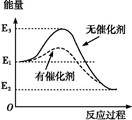
| A.该反应为吸热反应 |
| B.使用催化剂没有改变反应的反应热 |
| C.反应热等于E3-E2 |
| D.催化剂只对正反应有催化作用,对逆反应无催化作用 |