摘要:(2)在一定条件下.RO3 n―和I―发生反应的离子方程式为: RO3 n― + 6I― + 6H+ = R― + 3I2 + 3H2O RO3 n―中R元素的化合价是 , (3).(2003年广东省高考化学第7题)在一定条件下.RO3n-和氟气可发生如下反应: RO3n-+F2+2OH-=RO4-+2F-+H2O.从而可知在RO3n-中.元素R的化合价是 A.+4 B.+5 C.+6 D.+7
网址:http://m.1010jiajiao.com/timu_id_3749894[举报]
 (2013?朝阳区一模)燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放.
(2013?朝阳区一模)燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放.(1)用化学方程式表示NO形成硝酸型酸雨的反应
2NO+O2═2NO2、3NO2+H2O═2HNO3+NO
2NO+O2═2NO2、3NO2+H2O═2HNO3+NO
(2)能作脱除剂的物质很多,下列说法正确的是
ab
ab
a.用 H2O作脱除剂,不利于吸收含氮烟气中的NO
b.用 Na2SO3作脱除剂,O2会降低Na2SO3的利用率
c.用CO作脱除剂,会使烟气中NO2的浓度增加
(3)尿素[CO(NH2)2]在一定条件下能有效将NOx转化为N2.
Ⅰ.已知可通过下列方法合成尿素:
2NH3(g)+CO2(g)?H2NCOONH4(s)△H=-159.5kJ/mol
H2NCOONH4(s)?CO(NH2)2(s)+H2O(l)△H=+28.5kJ/mol
①尿素释放出NH3的热化学方程式是
CO(NH2)2(s)+H2O(l)?2NH3(g)+CO2(g)△H=+131kJ/mol
CO(NH2)2(s)+H2O(l)?2NH3(g)+CO2(g)△H=+131kJ/mol
②写出有利于尿素释放NH3的条件并说明理由
升高温度;升高温度有利于平衡向吸热反应方向进行,同时温度升高,氨气的溶解度降低,均有利于向释放氨气的方向进行
升高温度;升高温度有利于平衡向吸热反应方向进行,同时温度升高,氨气的溶解度降低,均有利于向释放氨气的方向进行
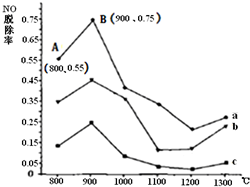
Ⅱ.CO(NH2)2与某种烟气(主要为N2、NO和O2)中的NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率随温度变化的曲线如图:
①曲线a 对应CO(NH2)2 与NO的物质的量比值是
3:1
3:1
.②曲线a、b、c中,800℃~900℃区间内发生主要反应的化学方程式是
4NH3+6NO═5N2+6H2O或2CO(NH2)2+6NO═2CO2+4H2O+5N2
4NH3+6NO═5N2+6H2O或2CO(NH2)2+6NO═2CO2+4H2O+5N2
.③900℃~1200℃区间内脱除率下降,NO浓度上升.发生的主要反应是
4NH3+5O2═4NO+6H2O
4NH3+5O2═4NO+6H2O
.④曲线a中,NO的起始浓度为6×10-4 mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为
1.5×10-4
1.5×10-4
mg/(m3?s).
(1)土壤的pH一般在4—9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因________________________________________。加入石膏(CaSO4·2H2O)可以使土壤碱性降低,有关反应的化学方程式为___________________。
(2)在一定条件下进行如下反应:
aX(g)+bY(g)![]() cZ(g)
cZ(g)
下图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系示意图。

①写出该反应的化学平衡常数表达式:K=___________。随着温度的升高,K值___________ (填“增大”“减小”或“不变”)。当反应物起始浓度相同时,平衡常数K值越大,表明__________(填序号)。
A.X的转化率越高 B.反应进行得越完全
C.达到平衡时X的浓度越大 D.化学反应速率越快
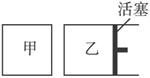
②如下图所示,相同温度下,在甲、乙两容器中各投入1 mol X、2 mol Y和适量催化剂,甲、乙两容器的初始体积均为
 香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如下:下列说法正确的是( )
香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如下:下列说法正确的是( )
