摘要:(一).氧化还原反应的基本概念 1.氧化还原反应中物质及变化关系: 反应物 表现性质 发生的变化 化合价的变化 生成物 氧化剂 氧化性 还原反应 降低 还原产物 还原剂 还原性 氧化反应 升高 氧化产物 常见的氧化剂 常见的还原剂 表达氧化还原关系的常用形式有 “双线桥 式和 “单线桥 式 形式 示例 箭头意义及指向 双线桥式 2Na2S+Na2SO3+3H2SO4==3S↓+3Na2SO4+3H2O 单线桥式 2Na2S+Na2SO3+3H2SO4==3S↓+3Na2SO4+3H2O 2.氧化性.还原性的比较 元素处于最高价.最低价和中间价态时的性质特点: 最高价只能表现氧化性.最低价只能表现还原性.中间价态既能表现氧化性又能表现还原性. 化合价降低时表现氧化性.化合价升高时表现还原性. 氧化性.还原性强弱的比较途径: (1)根据一个已知的氧化还原反应判断 氧化性: 氧化剂强于氧化产物 还原性: 还原剂强于还原产物 (2) 根据可变价金属被氧化的程度判断: 例:氯气和硫跟铁反应时.产物中铁的化合价分别为 +3.+2 可见Cl2的氧化性比S强. (3)根据反应条件判断: 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O MnO2+4HCl=MnCl2+Cl2+2H2O O2+4HCl=2Cl2+2H2O 比较KMnO4.O2.MnO2的氧化性强弱:KMnO4>MnO2>O2 (4)根据金属活动性顺序比较: 位置靠前的金属.单质还原性较强.其离子的氧化性性较弱 (5)根据元素所在周期表位置关系判断: 同主族从上到下.或同周期从左到右.其单质的性质递变和离子的性质递变规律:一般说来同主族从上到下单质的还原性越强.阳离子的氧化性性越弱,同周期从左到右单质的氧化性越强.阴离子的还原性性越弱, (6)根据原电池和电解池电极的极别或发生的反应判断: 原电池两金属电极,被腐蚀的一极是负极.该金属还原性较强,冒气体(H2)或质量增加的极是正极.该金属还原性较弱,电解反应中.阴极上先反应的阳离子氧化性较强.阳极上先反应的阴离子还原性较强. 注意:氧化性还原性的强弱只与原子得失电子的能力大小有关,而与得失电子的多少无关 3.基本规律: ⑴.先后规律:一种氧化剂氧化两种还原剂或一种还原剂还原两种氧化剂时有先后顺序.其规则是: “强者 先反应. ⑵.强弱规律:同一氧化还原反应中.氧化剂的氧化性强于氧化产物,还原剂的还原性强于还原产物. ⑶.归中规律:同种元素不同价态间得失电子的 “归中反应 .电子转移方向遵循 “归中不交叉 的规则. ⑷.守恒规律:氧化还原反应中.得失电子总数守恒.化合价升降总数守恒 4.有关氧化还原反应的计算 有关氧化还原反应的计算常常应用的关系有 “电子得失守恒 “电荷数守恒 等.
网址:http://m.1010jiajiao.com/timu_id_3747674[举报]
 元素X的单质及X与元素Y形成的化合物存在如图所示的关系(其中m≠n,且均为正整数).下列说法正确的是( )
元素X的单质及X与元素Y形成的化合物存在如图所示的关系(其中m≠n,且均为正整数).下列说法正确的是( )| A、X一定是金属元素 | B、(n-m)一定等于1 | C、由X生成1mol XYm时转移的电子数目一定为4NA | D、三个化合反应一定都是氧化还原反应 |
(2011?南昌一模)氧化还原反应实际上包含氧化反应和还原反应两个过程,一个还原反应过程的离子方程式为:NO
+4H++3e-═NO↑+2H2O.
下列四种物质:KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质甲,滴加少量稀硝酸,能使上述反应过程发生.
(1)被还原的元素是
(2)写出并配平该氧化还原反应方程式:
(3)反应生成0.3mol H2O,则转移电子的数目为
(4)若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂的物质的量之比将
查看习题详情和答案>>
- 3 |
下列四种物质:KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质甲,滴加少量稀硝酸,能使上述反应过程发生.
(1)被还原的元素是
N
N
;还原剂是KI
KI
.(2)写出并配平该氧化还原反应方程式:
6KI+8HNO3═6KNO3+2NO↑+3I2+4H2O
6KI+8HNO3═6KNO3+2NO↑+3I2+4H2O
.(3)反应生成0.3mol H2O,则转移电子的数目为
0.45NA
0.45NA
.(4)若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂的物质的量之比将
增大
增大
(填“增大”、“不变”、“减小”或“不能确定”).Fe是地壳中含量很丰富的元素,也是生物体所必须的元素.
(1)我国南方某些地区的井水取出久置之后,井水由澄清变成少量红棕色絮状沉淀积于缸底,水面浮着一层“锈皮”.这层“锈皮”的主要成分是(写化学式) .
(2)家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是 (填字母代号);
A.4Fe(OH)2+2H2O+O2═4Fe(OH)3 B.2Fe+2H2O+O2═2Fe(OH)2
C.2H2O+O2+4e-═4OH- D.Fe-3e-═Fe3+
(3)某化学研究性学习小组讨论Fe3+和SO32-之间发生怎样的反应,提出了两种可能:一是发生氧化还原反应:2Fe3++SO32-+H2O═2Fe2++SO42-+2H+;二是发生双水解反应:2Fe3++3SO32-+6H2O═2Fe(OH)3(胶体)+3H2SO3.为了证明是哪一种反应,同学们设计并实施了下列实验,请填写下列空白:
①实验Ⅰ,取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液的颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色.这种红褐色液体是 .向红褐色液体中逐滴加入稀盐酸至过量,可以观察到的现象是 .将溶液分成两等份,其中一份加入KSCN溶液,溶液变为血红色,反应的离子方程式为 .另一份加入BaCl2稀溶液,有少量白色沉淀生成,产生该白色沉淀的离子方程式 .
②实验Ⅱ,换用稀释的FeCl3和Na2SO3溶液重复实验Ⅰ,产生的现象完全相同.由上述实验得出的结论是 .
③若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的化学方程式是 .
④从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
Ⅰ. ;
Ⅱ. ;
(4)自然界中铁矿石主要有赤铁矿和磁铁矿,应用高炉能冶炼制得金属铁.Fe3O4在高炉中有下列反应:Fe3O4+CO═3FeO+CO2
反应形成的固体混合物(FeO、Fe3O4)中,元素氧和铁的质量比用m(O):m(Fe)表示.设Fe3O4被CO还原的质量分数为x,则x与混合物中m(O):m(Fe)的关系式(用含m(O)、m(Fe)的代数式表示):x= .
查看习题详情和答案>>
(1)我国南方某些地区的井水取出久置之后,井水由澄清变成少量红棕色絮状沉淀积于缸底,水面浮着一层“锈皮”.这层“锈皮”的主要成分是(写化学式)
(2)家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
A.4Fe(OH)2+2H2O+O2═4Fe(OH)3 B.2Fe+2H2O+O2═2Fe(OH)2
C.2H2O+O2+4e-═4OH- D.Fe-3e-═Fe3+
(3)某化学研究性学习小组讨论Fe3+和SO32-之间发生怎样的反应,提出了两种可能:一是发生氧化还原反应:2Fe3++SO32-+H2O═2Fe2++SO42-+2H+;二是发生双水解反应:2Fe3++3SO32-+6H2O═2Fe(OH)3(胶体)+3H2SO3.为了证明是哪一种反应,同学们设计并实施了下列实验,请填写下列空白:
①实验Ⅰ,取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液的颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色.这种红褐色液体是
②实验Ⅱ,换用稀释的FeCl3和Na2SO3溶液重复实验Ⅰ,产生的现象完全相同.由上述实验得出的结论是
③若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的化学方程式是
④从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
Ⅰ.
Ⅱ.
(4)自然界中铁矿石主要有赤铁矿和磁铁矿,应用高炉能冶炼制得金属铁.Fe3O4在高炉中有下列反应:Fe3O4+CO═3FeO+CO2
反应形成的固体混合物(FeO、Fe3O4)中,元素氧和铁的质量比用m(O):m(Fe)表示.设Fe3O4被CO还原的质量分数为x,则x与混合物中m(O):m(Fe)的关系式(用含m(O)、m(Fe)的代数式表示):x=
(2013?闵行区一模)氧化还原反应在生产、生活中具有广泛的用途,贯穿古今.
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
a.煤的形成 b.原电池工作
c.简单机械织布 d.我国古代烧制陶器
(2)水是人体的重要组成部分,是人体中含量最多的一种物质.“四种基本反应类型与氧化还原反应的关系”可用下图表示.

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2.配平下列化学方程式并标明电子转移的方向和数目:
(4)已知:还原性HSO3->I-,若加入的NaHSO3过量,还可能与上述生成物中的
查看习题详情和答案>>
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
c
c
(选填编号).a.煤的形成 b.原电池工作
c.简单机械织布 d.我国古代烧制陶器
(2)水是人体的重要组成部分,是人体中含量最多的一种物质.“四种基本反应类型与氧化还原反应的关系”可用下图表示.

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
2F2+2H2O=4HF+O2或2Na+2H2O=2NaOH+H2↑或C+H2O
CO+H2
| ||
2F2+2H2O=4HF+O2或2Na+2H2O=2NaOH+H2↑或C+H2O
CO+H2
.
| ||
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2.配平下列化学方程式并标明电子转移的方向和数目:
4
4
NaIO3+10
10
NaHSO3→2
2
I2+7
7
Na2SO4+3
3
H2SO4+2
2
H2O(4)已知:还原性HSO3->I-,若加入的NaHSO3过量,还可能与上述生成物中的
I2
I2
反应,离子方程式为H2O+I2+HSO3-=2I-+SO42-+3H+
H2O+I2+HSO3-=2I-+SO42-+3H+
.在如图转化关系中,固体甲的焰色反应呈黄色,M为常见的液体物质,I为常见金属,且I与G的稀溶液不反应,只能与G的浓溶液在加热条件下反应;H可制作耐火材料(图中部分产物没有列出).回答下列问题:
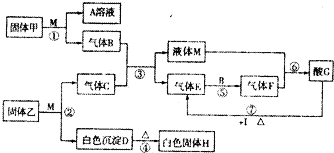
(I)固体甲的电子式为, ;固体乙与M反应的化学方程式为
(2)反应①一⑦中属于氧化还原反应的是 (填写反应序号).
(3)工业上常采用浓氨水吸收废气中的气体E,通过处理既可以制得化肥又可以获得较纯的E而循环利用,写出用过量的浓氨水吸收E的化学方程式:
(4)用惰性电极电解I与G反应所得的盐溶液200mL,需要加入0.8g I的氧化物才能将溶液恢复原状,则阴极上通过的电子数是 ,如果忽略溶液体积变化,电解后所得溶液的pH=
(5)模拟工业上催化氧化E,450℃在一个恒压密闭容器中充入2mol E和1mol B达到平衡后测得F的体积分数为80%,放出热量60kJ,该条件下反应的热化学方程式为 .
查看习题详情和答案>>

(I)固体甲的电子式为,
(2)反应①一⑦中属于氧化还原反应的是
(3)工业上常采用浓氨水吸收废气中的气体E,通过处理既可以制得化肥又可以获得较纯的E而循环利用,写出用过量的浓氨水吸收E的化学方程式:
(4)用惰性电极电解I与G反应所得的盐溶液200mL,需要加入0.8g I的氧化物才能将溶液恢复原状,则阴极上通过的电子数是
(5)模拟工业上催化氧化E,450℃在一个恒压密闭容器中充入2mol E和1mol B达到平衡后测得F的体积分数为80%,放出热量60kJ,该条件下反应的热化学方程式为