摘要:根据反应:Fe+CuSO4=FeSO4+Cu和Cu+2AgNO3=Cu(NO3)2+2Ag.判断三种金属的还原性由强到弱的顺序是 ,阳离子的氧化性由强到弱的顺序是 .
网址:http://m.1010jiajiao.com/timu_id_3744798[举报]
(8分)请根据反应:Fe + Cu2+ = Fe 2++ Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
(8分)请根据反应 :Fe + Cu2+ = Fe 2++Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
查看习题详情和答案>>
(8分)请根据反应 :Fe + Cu2+ = Fe 2++ Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
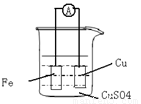
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
查看习题详情和答案>>
请根据反应 Fe+CuSO4=Fe SO4+Cu,设计原电池,完成以下问题.负极:
正极:
查看习题详情和答案>>
Fe
Fe
,其电极反应式为:Fe-2e-=Fe2+
Fe-2e-=Fe2+
正极:
Cu;
Cu;
,其电极反应式为:Cu2++2e-=Cu
Cu2++2e-=Cu
电解质溶液:CuSO4
CuSO4
,电池的离子反应式为:Fe+Cu2+=Fe2++Cu
Fe+Cu2+=Fe2++Cu
.将洁净的金属片Fe、Zn、A、B分别与Cu用导线连接浸在合适的电解质溶液里.实验并记录电压指针的移动方向和电压表的读数如下表所示:
根据实验记录,完成以下填空:
(1)构成两电极的金属活动性相差越大,电压表的读数越
(2)Zn、A、B三种金属活动性由强到弱的顺序是
(3)Cu与A组成的原电池,
(4)A、B形成合金,露置在潮湿空气中,
(5)铝热反应中的铝热剂的成分是
查看习题详情和答案>>
| 金属 | 电子流动方向 | 电压/V |
| Fe | Fe→Cu | +0.78 |
| Zn | Zn→Cu | +1.10 |
| A | Cu→A | -0.15 |
| B | B→Cu | +0.3 |
(1)构成两电极的金属活动性相差越大,电压表的读数越
大
大
.(填“大”、“小”).(2)Zn、A、B三种金属活动性由强到弱的顺序是
Zn>B>A
Zn>B>A
.(3)Cu与A组成的原电池,
Cu
Cu
为负极,此电极反应式为Cu-2e-=Cu2+
Cu-2e-=Cu2+
.(4)A、B形成合金,露置在潮湿空气中,
B
B
先被腐蚀.(5)铝热反应中的铝热剂的成分是
铝粉和金属氧化物的混合物
铝粉和金属氧化物的混合物
,工业上常用的铝的冶炼的化学方程式为2Al2O3
4Al+3O2↑
| ||
2Al2O3
4Al+3O2↑
.
| ||