网址:http://m.1010jiajiao.com/timu_id_3744676[举报]
通过常见的酸和碱的学习,我们认识了“酸”和“碱”,请回答下列问题:
(1)常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在有相同的离子________(填符号),因此,它们有很多相似的化学性质,如:________________、________________(写两条即可).
(2)碱有氢氧化钠、氢氧化钙等,氢氧化钠可作某些气体的干燥剂,如:干燥________等气体,氢氧化钙可由生石灰与水反应制得,其化学方程式为:________.
通过常见的酸和碱的学习,我们认识了“酸”和“碱”,请回答下列问题:
(1)常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在有相同的离子________(填符号),因此,它们有很多相似的化学性质,如:________、________(写两条即可).
(2)碱有氢氧化钠、氢氧化钙等,氢氧化钠可作某些气体的干燥剂,如:干燥________等气体,氢氧化钙可由生石灰与水反应制得,其化学方程式为:________.
探究l:研究常见的物质---氢氧化钠和盐酸的反应程度.
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 固体化台物______. | ______ | 盐酸过量 |
通过探究实验,同学们发现硫酸和盐酸溶液都可以和锌反应产生氢气.产生这种共同现象的原因为______
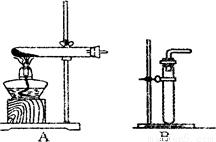
探究3:探索未知---浓硝酸和铜制取气体.
已知Cu+4HN03(浓)=Cu( NO3)2+H2O+2N02↑.N02能和水反应生成硝酸和N0.NO和NO2都是空气的污染物.
(1)利用该反应制取二氧化氮的发生装置,应选用图所示装置中的______.收集N02的方法为______.
(2)反应NO+X→N02中,X的化学式应为______;若用浓硝酸和铜制取NO,应采用的收集方法是______.
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入l0g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,请你计算所加碳酸钠溶液的溶质质量分数?
 查看习题详情和答案>>
查看习题详情和答案>>
 (2013?许昌一模)某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
(2013?许昌一模)某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.探究l:研究常见的物质---氢氧化钠和盐酸的反应程度.
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 固体化台物 Na2CO3(或CaCO3), Na2CO3(或CaCO3), . |
有气泡产生 有气泡产生 |
盐酸过量 |
通过探究实验,同学们发现硫酸和盐酸溶液都可以和锌反应产生氢气.产生这种共同现象的原因为
探究3:探索未知---浓硝酸和铜制取气体.
已知Cu+4HN03(浓)=Cu( NO3)2+H2O+2N02↑.N02能和水反应生成硝酸和N0.NO和NO2都是空气的污染物.
(1)利用该反应制取二氧化氮的发生装置,应选用图所示装置中的
(2)反应NO+X→N02中,X的化学式应为
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入l0g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,请你计算所加碳酸钠溶液的溶质质量分数?
某小组同学用盐酸和氢氧化钙,对酸和碱的中和反应进行探究.请你参与.
甲同学向装有氢氧化钙溶液的烧杯中加入盐酸,无明显现象.结论:两种物质未发生反应.
乙同学向滴有酚酞的氢氧化钙溶液的试管中慢慢滴加盐酸,溶液由 色变为无色.结论:两种物质发生了反应.反应的化学方程式为 .
大家认为乙的实验证明盐酸与氢氧化钙发生了中和反应.并对甲的实验继续探究.
[提出问题]甲实验后的溶液中有什么溶质?
[作出猜想]猜想一,只有CaCl2;猜想二有CaCl2和Ca(OH)2;猜想三,有CaCl2和HCl.
[实验探究]为验证猜想,丙同学设计了方案1和方案2,并按方案进行实验.
| 方案编号 | 方案1 | 方案2 | 方案3 |
| 实验操作(分别取少量甲实验后的溶液于试管中) |  | 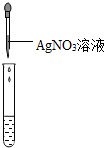 |  |
| 实验现象 | 对比标准比色卡:pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有HCl | 溶液中有CaCl2 |
[实验评价]丙的实验操作和方案中有不足之处,其不足之处是 .
大家讨论后通过方案3即证明了猜想三正确,其实验中应观察到的现象为 .
[实验拓展]为节约资源和避免实验废液对环境污染,小组同学将方案1和方案3及甲实验后烧杯中剩余溶液混合(混合时未见明显现象),并对混合液中的盐分离回收,请将相关内容填入下表.
| 要分离的盐 | 所用试剂 | 主要操作 |
| | | |