摘要:18.在如图所示的装置中.若通入直流电5 min时.铜电极质量增加2.16 g.试回答: (1)电源电极X名称为 . (2)pH变化:A .B .C . (填“增大 “减小 或“不变 ) (3)通电5 min时.B中共收集224 mL气体.溶液体积为200 mL.则通电前CuSO4溶液的物质的量浓度为 (设电解前后溶液体积无变化). (4)若A中KCl溶液的体积也是200 mL.电解后.溶液的pH为 (设电解前后溶液体积无变化). 解析:(1)C装置的铜电极质量增加.说明铜极上有金属析出.即溶液中的银离子被还原生成银单质.故铜极为阴极.由此可确定X极为负极. (2)A装置电解KCl溶液.生成氢气.氯气和氢氧化钾.B装置生成Cu.O2和H2SO4.溶液中氢离子浓度增大.C装置阴极析出银单质.阳极上的银失去电子变成银离子.理论上溶液的物质的量浓度不变. (3)B装置两极上电子转移的数目与C装置中转移的电子数目相同.C装置中转移的电子为=0.02 mol.经判断.B装置两极上的反应为: 阴极:Cu2++2e-===Cu,2H++2e-===H2↑ 阳极:4OH--4e-===O2↑+2H2O 根据题意可得: 2n(H2)+2n(Cu)=4n(O2)=0.02 mol. n(H2)+n(O2)=. 解得n(Cu)=0.005 mol.CuSO4溶液的物质的量浓度为:0.005 mol/0.2 L=0.025 mol/L (4)A装置的反应为: 2KCl+2H2O2KOH+H2↑+Cl2↑ 即反应中电子转移的物质的量与生成的氢氧根离子的物质的量相等.为0.02 mol. c(OH-)==0.1 mol/L. 故pH=13. 答案:增大 减小 不变 (3)0.025 mol/L (4)13
网址:http://m.1010jiajiao.com/timu_id_3743734[举报]
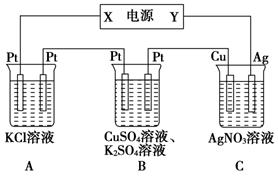
 在如图所示的装置中,若通入直流电5min时,铜电极质量增加2.16g,试回答:
在如图所示的装置中,若通入直流电5min时,铜电极质量增加2.16g,试回答:(1)pH变化:A
增大
增大
,B减小
减小
,C不变
不变
.(填“增大”“减小”或“不变”)
(2)请写出C池中发生反应的离子方程式
阳极为Ag-e-═Ag+,阴极为Ag++e-═Ag
阳极为Ag-e-═Ag+,阴极为Ag++e-═Ag
.(3)通电5min时,B中共收集224mL气体(标准状况),溶液体积为100mL.则通电前CuSO4溶液的物质的量浓度为
0.05 mol/L
0.05 mol/L
mol?L-1(设电解前后溶液体积无化).(4)若A中KCl溶液的体积是200mL,电解后,溶液的pH为
13
13
(设电解前后溶液体积无变化).(10分)在如图所示的装置中,若通入直流电5 min时,铜电极质量增加2.16g。试回答:
(1)电源中Y电极为直流电源的__________极。
(2)pH变化:A:________B:________ (填“增大”、“减小”或“不变”)。
(3) 若A中KCl溶液的体积是200 mL,电解后,溶液的pH为__________(设电解前后溶液体积无变化)。
(4)B中电解CuSO4溶液的电极总反应:
查看习题详情和答案>>
(10分)在如图所示的装置中,若通入直流电5 min时,铜电极质量增加2.16g。试回答:
(1)电源中Y电极为直流电源的__________极。
(2)pH变化:A:________B:________ (填“增大”、“减小”或“不变”)。
(3) 若A中KCl溶液的体积是200 mL,电解后,溶液的pH为__________(设电解前后溶液体积无变化)。
(4)B中电解CuSO4溶液的电极总反应: