摘要:11.P单质在下列反应中4P+3KOH+3 H2O=3KH2PO2+P H3的变化是 A.被氧化 B.被还原 C.既被氧化又被还原 D.既未被氧化又未被还原
网址:http://m.1010jiajiao.com/timu_id_3739578[举报]
U、V、W、X、Y为短周期元素,且原子半径依次增大,U、V同主族,V、W、X、Y处于同周期,U的最高价氧化物所对应的水化物与其气态氢化物反应生成盐A,U、W、Y的最高价氧化物对应的水化物能互相反应生成盐,Z为血红蛋白中所必需的金属元素,且U、W、Z分别能与氧元素形成U203、W2O3、Z2O3.
回答下列问题:
(1)U的气态氢化物分子的电子式为
 ,盐A中阳离子的检验方法是
,盐A中阳离子的检验方法是
(2)元素V、W、X、Y的第一电离能的大小关系是:
(3)W的单质与Y的最高价氧化物对应的水化物的溶液反应,其离子方程式是
(4)z单质与水在一定条件下反应的化学方程式为
(5)已知:Z(s)+
(g)=ZO(s)△H=-272.0KJ.mol-1
W(s)+
(g)=W2O3(s)△H=-1675.7KJ.mol-1
W的单质和ZO反应的热化学方程式是
查看习题详情和答案>>
回答下列问题:
(1)U的气态氢化物分子的电子式为


取少量A于试管中,加入氢氧化钠溶液,加热,产生一种能够使湿润的红色石蕊试纸变蓝的气体,则证明阳离子是铵根离子
取少量A于试管中,加入氢氧化钠溶液,加热,产生一种能够使湿润的红色石蕊试纸变蓝的气体,则证明阳离子是铵根离子
;(2)元素V、W、X、Y的第一电离能的大小关系是:
P>Mg>Al>Na
P>Mg>Al>Na
,Z原子的最外层电子排布式4s2
4s2
;(3)W的单质与Y的最高价氧化物对应的水化物的溶液反应,其离子方程式是
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
;(4)z单质与水在一定条件下反应的化学方程式为
3Fe+4H2O
Fe3O4+4H2↑
| ||
3Fe+4H2O
Fe3O4+4H2↑
;
| ||
(5)已知:Z(s)+
| 1 |
| 202 |
W(s)+
| 3 |
| 202 |
W的单质和ZO反应的热化学方程式是
3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△H=-859.7kJ/mol
3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△H=-859.7kJ/mol
.(2013?资阳二模)A、B、C、D、E、F为前四周期的元素.其中,A元素和B元素的原子都有一个未成对电子,A3+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解性在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4,其最高价氧化物对应的水化物可以用于制取炸药和制作铅蓄电池;E元素的基态原子核外有六种运动状态的电子;F元素的单质为紫红色固体,可通过“湿法冶金”而得.请回答下列问题:
(1)CB3分子中心原子的杂化类型是
(2)F元素的原子的外围电子排布式为
(3)B、D元素最高价氧化物对应的水化物的酸性强弱:
(4)用导线将A和F的单质做成的电极连接起来,插入到盛有C的最高价氧化物的水化物的浓溶液中构成原电池,试写出在单质A表面发生反应的电极反应式:
(5)分子R是由C元素与氢元素形成的18电子分子,R的电子式为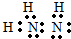
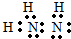 .
.
(6)24g E的单质在33.6L氧气(标准状况)中燃烧,至反应物全部耗尽,放出x kJ热量.则1mol E与O2反应生成E的低价氧化物时的热化学方程式为
查看习题详情和答案>>
(1)CB3分子中心原子的杂化类型是
sp3
sp3
.
(2)F元素的原子的外围电子排布式为
3d104s1
3d104s1
;如图所示为F与Au以3:1形成的合金晶胞图,在图中的括号内写出对应的元素符号.(3)B、D元素最高价氧化物对应的水化物的酸性强弱:
HClO4>H2SO4
HClO4>H2SO4
(填化学式).(4)用导线将A和F的单质做成的电极连接起来,插入到盛有C的最高价氧化物的水化物的浓溶液中构成原电池,试写出在单质A表面发生反应的电极反应式:
2H++NO3-+e-=NO2↑+H2O
2H++NO3-+e-=NO2↑+H2O
.(5)分子R是由C元素与氢元素形成的18电子分子,R的电子式为
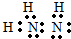
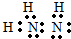
(6)24g E的单质在33.6L氧气(标准状况)中燃烧,至反应物全部耗尽,放出x kJ热量.则1mol E与O2反应生成E的低价氧化物时的热化学方程式为
C(s)+
O2(g)=CO(g)△H=-(x-y)kJ/mol
| 1 |
| 2 |
C(s)+
O2(g)=CO(g)△H=-(x-y)kJ/mol
(已知:E的燃烧热为y kJ/mol).| 1 |
| 2 |
(2008?上海)四种短周期元素的性质或结构信息如下表.请根据信息回答下列问题.
(1)B元素在周期表中的位置
(2)写出C单质与水反应的化学方程式
(3)D元素最高价氧化物晶体的硬度
(4)A、B两元素非金属性较强的是(写元素符号)
查看习题详情和答案>>
| 元素 | A | B | C | D |
| 性质 结构 信息 |
室温下单质呈粉末状固体,加热易熔化. 单质在氧气中燃烧,发出明亮的蓝紫色火焰. |
单质常温、常压下是气体,能溶于水. 原子的M层有1个未成对的p电子. |
单质质软、银白色固体、导电性强. 单质在空气中燃烧发出黄色的火焰. |
原子最外层电子层上s电子数等于p电子数. 单质为空间网状晶体,具有很高的熔、沸点. |
第三周期ⅦA
第三周期ⅦA
,写出A原子的电子排布式1s22s22p63s23p4
1s22s22p63s23p4
.(2)写出C单质与水反应的化学方程式
2Na+2H2O=2NaOH+H2↑
2Na+2H2O=2NaOH+H2↑
.A与C形成的化合物溶于水后,溶液的pH>
>
7(填“大于”、“等于”或“小于”).(3)D元素最高价氧化物晶体的硬度
小(或大)
小(或大)
(填“大”、“小”),其理由是二氧化碳是分子晶体(或二氧化硅是原子晶体)
二氧化碳是分子晶体(或二氧化硅是原子晶体)
.(4)A、B两元素非金属性较强的是(写元素符号)
Cl
Cl
.写出证明这一结论的一个实验事实高氯酸的酸性大于硫酸的酸性或氯化氢稳定比硫化氢强
高氯酸的酸性大于硫酸的酸性或氯化氢稳定比硫化氢强
.已知B、C为常见的两种金属单质,E、I为常见的两种非金属单质,A为硫酸盐反应②为D的溶液与C在加热条件下的反应,P溶液和G溶液中具有相同的阳离子,请根据要求回答下列问题.

(1)B元素在周期表的位置:
(2)物质I的电子式:
 .
.
(3)Y转变为X的现象是:
(4)写出反应④的化学反应方程式:
(5)向沸水中加入H的饱和溶液,可得到红褐色溶液,其溶液所具有性质
A.具有丁达尔效应
B.处加直流电源阳极附近溶液颜色加深
C.加入盐酸溶液出现先沉淀后溶解的现象
D.能透过半透膜,不能透过滤纸
(6)向含1molG的溶液中加入1molNa2O2,所发生的离子反应方程式:
查看习题详情和答案>>

(1)B元素在周期表的位置:
第四周期第ⅤⅢ族
第四周期第ⅤⅢ族
,(2)物质I的电子式:


(3)Y转变为X的现象是:
白色絮状沉淀迅速变为灰绿色,最终转化为红褐色
白色絮状沉淀迅速变为灰绿色,最终转化为红褐色
.涉及的反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
.(4)写出反应④的化学反应方程式:
Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
.物质F与HI水溶液的离子反应方程式 式:Fe3O4+2I-+8H+=I2+3Fe2++4H2O
Fe3O4+2I-+8H+=I2+3Fe2++4H2O
.(5)向沸水中加入H的饱和溶液,可得到红褐色溶液,其溶液所具有性质
AC
AC
.A.具有丁达尔效应
B.处加直流电源阳极附近溶液颜色加深
C.加入盐酸溶液出现先沉淀后溶解的现象
D.能透过半透膜,不能透过滤纸
(6)向含1molG的溶液中加入1molNa2O2,所发生的离子反应方程式:
4Fe 2++4Na2O2+6H2O═4Fe(OH)3↓+8Na++O2↑
4Fe 2++4Na2O2+6H2O═4Fe(OH)3↓+8Na++O2↑
. 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2.E的阳离子与A的阴离子核外电子层结构完全相同.
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2.E的阳离子与A的阴离子核外电子层结构完全相同.回答下列问题:
(1)五种元素的名称:A
氧
氧
,B磷
磷
,C硫
硫
,D氯
氯
,E铝
铝
.(2)B、C、D元素的原子半径由大到小的顺序为
r(P)>r(S)>r(Cl)
r(P)>r(S)>r(Cl)
,它们的最高价氧化物对应水化物的酸性强弱顺序为HClO4>H2SO4>H3PO4
HClO4>H2SO4>H3PO4
.(3)写出C单质在足量A单质中燃烧后的产物与D单质同时通入水中的化学方程式
SO2+Cl2+2H2O═H2SO4+2HCl
SO2+Cl2+2H2O═H2SO4+2HCl
.(4)A与E形成的化合物的化学式是
Al2O3
Al2O3
,它的性质决定了它在物质的分类中应属于两性氧化物
两性氧化物
.(5)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量时,观察到的现象是
有白色沉淀生成,当达到最大量时又逐渐减少,最终沉淀完全消失,变成澄清溶液
有白色沉淀生成,当达到最大量时又逐渐减少,最终沉淀完全消失,变成澄清溶液
,有关反应的离子方程式为Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O
Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O
.