摘要:已知同温同压下混合气体的密度是一种简单气体A的密度的倍数:=
网址:http://m.1010jiajiao.com/timu_id_3735400[举报]
 已知某可逆反应:mA(g)+nB(g)?pC(g)△H 在密闭容器器中进行,如图所示,反应在不同时间t,温度T和压强P与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是( )
已知某可逆反应:mA(g)+nB(g)?pC(g)△H 在密闭容器器中进行,如图所示,反应在不同时间t,温度T和压强P与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是( )
查看习题详情和答案>>
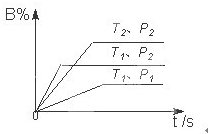 已知某可逆反应m A(g)+n B(g)?p C(g)△H,在密闭容器中进行,如图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线.由曲线分析,下列判断正确的是( )
已知某可逆反应m A(g)+n B(g)?p C(g)△H,在密闭容器中进行,如图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线.由曲线分析,下列判断正确的是( )
查看习题详情和答案>>
 已知某可逆反应mA(g)+nB(g)?pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )
查看习题详情和答案>>
 已知298K时:
已知298K时:反应Ⅰ:2H2(g)+O2(g)=2H2O(g)△H=-484.0kJ?mol-1
反应Ⅱ:CO(g)+1/2O2(g)?CO2(g)△H=-283.0kJ?mol-1
(1)298K时,将a mol CO2与b mol H2混合气体充入容积为1L的密闭容器中,2min后反应达到平衡状态时测得产物CO的浓度为c mol?L-1.则:
①v(H2)=
| c |
| 2 |
| c |
| 2 |
②CO2与H2发生反应生成CO和水蒸气的热化学方程式为
CO2(g)+H2(g)?CO(g)+H2O(g)△H=+41.0kJ?mol-1
CO2(g)+H2(g)?CO(g)+H2O(g)△H=+41.0kJ?mol-1
.若不同温度下发生上述反应,其化学平衡常数K(700℃)<
<
K(830℃)(填写“<”、“>”或“=”)(2)向容积为1L的密闭容器中加入0.050mol CO和0.025mol O2,在一定温度下发生反应Ⅱ,达平衡后测得c(CO2)=0.040mol?L-1.则:①能说明反应Ⅱ已经达到化学平衡状态的是
bc
bc
(填写序号).a.v(CO2)=2v (O2) b.容器内压强保持不变
c.v逆(CO)=2v正(O2) d.容器内气体的密度保持不变
②该温度条件下,反应Ⅱ的化学平衡常数K=
56.56
56.56
.③某温度下,CO的平衡转化率(a)与体系总压强(P)的关系如下图所示.
平衡状态由a变到b时,平衡常数K(a)
=
=
K(b)(填“>”、“<”或“=”).已知体积为2L的恒容密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g),请根据化学反应的有关原理同答下列问题
(1)一定条件下,充入2mol SO2(g)和2mol O2(g),20s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为 ,此时,该密闭容器内混合气体的压强是反应前的 倍.
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号) .
①v正(SO2)=2v正(O2) ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各气体的浓度都不再发生变化
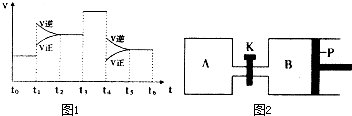
(3)图1表示该反应的速率(v)随时间(t)的变化的关系.则下列不同时间段中,SO3的百分含量最高的是
A、t0→t1 B、t2→t3 C、t3→t4 D、t5→t6
据图分析:你认为t3时改变的外界条件可能是 ;t6时保持体积不变向体系中充入少量SO3,再次平衡后SO2的体积百分含量比t6时 (填“大”、“小”或“等于”).
(4)图2中P是可自由平行滑动的活塞.在相同温度时,向A容器中充入4mol SO3(g),关闭K,向B容器中充入2mol SO3(g),两容器分别发生反应.已知起始时容器A和B的体积均为aL.试回答:
①反应达到平衡时容器B的体积为1.2a L,容器B中SO3转化率为
②若打开K,一段时间后重新达到平衡,容器B的体积为 L(连通管中气体体积忽略不计,且不考虑温度的影响).
(5)已知单质硫的燃烧热为△H=-296kJ/mol,经测定由S(s)生成120gSO3(g)可放热592.5kJ,请写出SO2(g)氧化生成SO3(g)的热化学方程式 .
查看习题详情和答案>>

(1)一定条件下,充入2mol SO2(g)和2mol O2(g),20s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)
①v正(SO2)=2v正(O2) ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各气体的浓度都不再发生变化
(3)图1表示该反应的速率(v)随时间(t)的变化的关系.则下列不同时间段中,SO3的百分含量最高的是
A、t0→t1 B、t2→t3 C、t3→t4 D、t5→t6
据图分析:你认为t3时改变的外界条件可能是
(4)图2中P是可自由平行滑动的活塞.在相同温度时,向A容器中充入4mol SO3(g),关闭K,向B容器中充入2mol SO3(g),两容器分别发生反应.已知起始时容器A和B的体积均为aL.试回答:
①反应达到平衡时容器B的体积为1.2a L,容器B中SO3转化率为
②若打开K,一段时间后重新达到平衡,容器B的体积为
(5)已知单质硫的燃烧热为△H=-296kJ/mol,经测定由S(s)生成120gSO3(g)可放热592.5kJ,请写出SO2(g)氧化生成SO3(g)的热化学方程式