网址:http://m.1010jiajiao.com/timu_id_3735393[举报]
实验一:取mg该药片,研成粉末放入硬质玻璃管中,加热,充分反应后测得装置C增重2.16g,装置D增重0.44g.

(1)装置C和D中盛放的药品是:C
(2)实验开始前先通入一段时间空气,其目的是
实验二:另取m g该药片,加入100mL1mol/L的稀硫酸,充分反应后滤去不溶物,向滤液中逐渐加入1mol/L的NaOH溶液,产生沉淀的物质的量与加入NaOH溶液体积之间的关系如图:
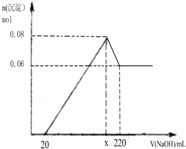
(3)根据以上所给数据求出x=
(4)通过计算确定铝碳酸镁的化学式为
(5)有医生建议患有严重胃溃疡的患者最好慎用该药,试用你所学的知识解释这样建议的理由是
(6)有同学认为,不需要做实验一,只需要在实验二的基础上再得知两个数据就可以求出铝碳酸镁的化学式,你认为这两个数据应该是:
(10分)在一容积为2 L的密闭容器中,加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应:N2(g)+3H2(g)  2NH3(g) ΔH<0
2NH3(g) ΔH<0
反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题: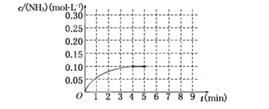
(1)根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)为______________.
(2)该反应达到平衡时H2的转化率________.
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,达到新平衡时NH3的物质的量浓度不可能为____________.(填序号)
A、0.20 mol·L-1 b、0.12 mol·L-1 c、0.10 mol·L-1 d、0.08 mol·L-1
(4)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol·L-1),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线.
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时NH3的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(N2)、n(H2)、n(NH3)分别为a、b、c,则a、b、c之间应该满足的关系式为:
(6)若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1 K2(填“>” “="”" 或 “<” )。
(10分)在一容积为2 L的密闭容器中,加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应:N2(g)+3H2(g)  2NH3(g) ΔH<0
2NH3(g) ΔH<0
反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:

(1)根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)为______________.
(2)该反应达到平衡时H2的转化率________.
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,达到新平衡时NH3的物质的量浓度不可能为____________.(填序号)
A、0.20 mol·L-1 b、0.12 mol·L-1 c、0.10 mol·L-1 d、0.08 mol·L-1
(4)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol·L-1),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线.
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时NH3的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(N2)、n(H2)、n(NH3)分别为a、b、c,则a、b、c之间应该满足的关系式为:
(6)若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1 K2(填“>” “=” 或 “<” )。
查看习题详情和答案>>
大气中的部分碘源于O3对海水中Iˉ的氧化。将O3持续通入NaI酸性溶液溶液中进行模拟研究。
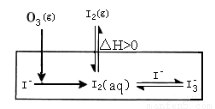
(1)O3将Iˉ氧化成I2的过程可发生如下反应:
①Iˉ(aq)+ O3(g)= IOˉ(aq) + O2(g) △H1
②IOˉ(aq)+H+(aq)  HOI(aq) △H2
HOI(aq) △H2
③HOI(aq) + Iˉ(aq) + H+(aq)  I2(aq) + H2O(l)? △H3
I2(aq) + H2O(l)? △H3
④O3(g)+2Iˉ(aq)+2H+(aq)= I2(aq) + O2(g)+ H2O(l)? △H4
则△H3与△H1、△H2、△H4之间的关系是:△H3? = ????? 。
(2)在溶液中存在化学平衡: I2(aq) + Iˉ(aq)  I3ˉ(aq)其平衡常数表达式为????? 。在反应的整个过程中I3ˉ物质的量浓度变化情况是????? 。
I3ˉ(aq)其平衡常数表达式为????? 。在反应的整个过程中I3ˉ物质的量浓度变化情况是????? 。
(3)为探究温度 对I2(aq) + Iˉ(aq)  I3ˉ(aq)? △H5? 反应的影响。在某温度T1下,将一定量的0.2 mol·L-1NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与 Iˉ反应),在t时刻,测得容器中I2(g)的浓度。然后分别在温度为T2、T3、T4、T5下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得I2(g)浓度,得到趋势图(见图一)。则:
I3ˉ(aq)? △H5? 反应的影响。在某温度T1下,将一定量的0.2 mol·L-1NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与 Iˉ反应),在t时刻,测得容器中I2(g)的浓度。然后分别在温度为T2、T3、T4、T5下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得I2(g)浓度,得到趋势图(见图一)。则:
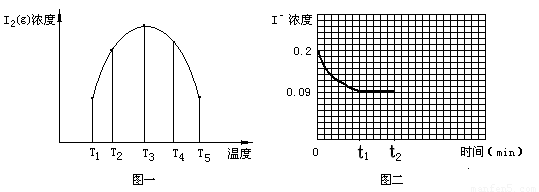
①若在T3时,容器中无O3, T4~T5温度区间容器内I2(g)浓度呈现如图一所示的变化趋势,则△H5????? 0(填>、=或<);该条件下在温度为T4时,溶液中Iˉ浓度随时间变化的趋势曲线如图二所示。在t2时,将该反应体系温度上升到T5,并维持该温度。请在图2中画出t2时刻后溶液中 Iˉ浓度变化总趋势曲线。
??? ②若在T3时,容器中还有O3,则T1~T2温度区间容器内I2(g)浓度呈现如图一所示的变化趋势,其可能的原因是????? 。(任写一点)
(4)利用反应④和图2的信息,计算0-t1时间段内用I2(aq)表示的化学反应速率????? 。
查看习题详情和答案>>
(10分)在一容积为2 L的密闭容器中,加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
(1)根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)为______________.
(2)该反应达到平衡时H2的转化率________.
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,达到新平衡时NH3的物质的量浓度不可能为____________.(填序号)
A、0.20 mol·L-1 b、0.12 mol·L-1 c、0.10 mol·L-1 d、0.08 mol·L-1
(4)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol·L-1),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线.
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时NH3的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(N2)、n(H2)、n(NH3)分别为a、b、c,则a、b、c之间应该满足的关系式为:
(6)若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1 K2(填“>” “=” 或 “<” )。
查看习题详情和答案>>