摘要:(二).离子共存问题 1.复分解型:在溶液中.若离子间能发生反应.如生成沉淀.弱电解质.气体等难电离的物质.(能使反应中离子浓度减小) 2.氧化还原反应型:Fe3+ .MnO4-(H+).NO3-(H+).ClO-与S2-.HS-.SO32-.I-.S2O32-.Fe2+ NO3-只有在酸性条件下才有强氧化性, ClO- 在所有条件下都有强氧化性 3.强烈双水解反应:Al3+与AlO2-.S2-.HS-.SO32-.HCO3-.CO32- Fe3+ 与HCO3-.CO32-等离子 4.络合类:Fe3+与SCN-.C6H5O-(H+)(紫色) Cu2+.Ag+与NH3 注意隐含条件的限制.如①离子的颜色:无色溶液.蓝色溶液等 ②.溶液的酸碱性:pH=3或13.pH试纸变红或变蓝.酚酞变红.甲基橙变红.溶液中c(H+)=1×10-14 mol·L-1或c(OH-)=1×10-14 mol·L-1 ③.因发生氧化还原反应不能共存的 ④.能与铝反应产生氢气的溶液可能是酸性.也可能是碱性,水电离出的H+(或OH-)的浓度是1×10-14 mol·L-1的溶液可能是酸性.也可能是碱性 ⑤.先能共存.后加入盐酸或通入NH3有变化的 ⑥.既能溶解Al(OH)3.又能溶解H2SiO3等
网址:http://m.1010jiajiao.com/timu_id_3734024[举报]
为测试一铁片中铁元素的含量,某课外活动小组提出下面两种方案并进行了实验(以下数据为多次平行实验测定结果的平均值):
方案一:将a g铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.
请回答下列问题:
(1)配平下面的化学方程式(将有关的化学计量数填入答题卡的横线上):
(2)在滴定实验中不能选择
(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为
和
;(铁的相对原子质量以55.9计)
(4)高锰酸钾是化学中常用强氧化剂.在实验室中可用下式配制少量高锰酸钾溶液:
1)、配平系数
2)、根据以上信息,下列各组离子在溶液中不能大量共存的是
A.Na+、K+、H+、Cl-、NO3-、MnO4- B.Na+、K+、H+、SO42-、BiO3-、Cl-
C.Na+、Al3+、H+、NO3-、SO42-、MnO4- D.Na+、K+、Mn2+、NO3-、SO42-、Cl-.
查看习题详情和答案>>
方案一:将a g铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将
| a |
| 10 |
请回答下列问题:
(1)配平下面的化学方程式(将有关的化学计量数填入答题卡的横线上):
2
2
KMnO4+10
10
FeSO4+8
8
H2SO4=5
5
Fe2(SO4)3+2
2
MnSO4+1
1
K2SO4+8
8
H2O(2)在滴定实验中不能选择
碱
碱
式滴定管,理由是KMnO4是强氧化剂,它会腐蚀乳胶管
KMnO4是强氧化剂,它会腐蚀乳胶管
;(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为
| 1.45 |
| a |
| 1.45 |
| a |
| 1.40 |
| a |
| 1.40 |
| a |
(4)高锰酸钾是化学中常用强氧化剂.在实验室中可用下式配制少量高锰酸钾溶液:
2
2
Mn2++5
5
NaBiO3+14
14
H+=2
2
MnO4-+5
5
Bi3++5
5
Na++7
7
H2O1)、配平系数
2)、根据以上信息,下列各组离子在溶液中不能大量共存的是
AB
AB
A.Na+、K+、H+、Cl-、NO3-、MnO4- B.Na+、K+、H+、SO42-、BiO3-、Cl-
C.Na+、Al3+、H+、NO3-、SO42-、MnO4- D.Na+、K+、Mn2+、NO3-、SO42-、Cl-.
为测试一铁片中铁元素的含量,某课外活动小组提出下面两种方案并进行了实验(以下数据为多次平行实验测定结果的平均值):
方案一:将a g铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.
请回答下列问题:
(1)配平下面的化学方程式(将有关的化学计量数填入答题卡的横线上):
______KMnO4+______FeSO4+______H2SO4=______Fe2(SO4)3+______MnSO4+______K2SO4+______H2O
(2)在滴定实验中不能选择______式滴定管,理由是______;
(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为______和______;(铁的相对原子质量以55.9计)
(4)高锰酸钾是化学中常用强氧化剂.在实验室中可用下式配制少量高锰酸钾溶液:
______Mn2++______NaBiO3+______H+=______MnO4-+______Bi3++______Na++______H2O
1)、配平系数
2)、根据以上信息,下列各组离子在溶液中不能大量共存的是______
A.Na+、K+、H+、Cl-、NO3-、MnO4- B.Na+、K+、H+、SO42-、BiO3-、Cl-
C.Na+、Al3+、H+、NO3-、SO42-、MnO4- D.Na+、K+、Mn2+、NO3-、SO42-、Cl-.
查看习题详情和答案>>
方案一:将a g铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将
| a |
| 10 |
请回答下列问题:
(1)配平下面的化学方程式(将有关的化学计量数填入答题卡的横线上):
______KMnO4+______FeSO4+______H2SO4=______Fe2(SO4)3+______MnSO4+______K2SO4+______H2O
(2)在滴定实验中不能选择______式滴定管,理由是______;
(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为______和______;(铁的相对原子质量以55.9计)
(4)高锰酸钾是化学中常用强氧化剂.在实验室中可用下式配制少量高锰酸钾溶液:
______Mn2++______NaBiO3+______H+=______MnO4-+______Bi3++______Na++______H2O
1)、配平系数
2)、根据以上信息,下列各组离子在溶液中不能大量共存的是______
A.Na+、K+、H+、Cl-、NO3-、MnO4- B.Na+、K+、H+、SO42-、BiO3-、Cl-
C.Na+、Al3+、H+、NO3-、SO42-、MnO4- D.Na+、K+、Mn2+、NO3-、SO42-、Cl-.
为测试一铁片中铁元素的含量,某课外活动小组提出下面两种方案并进行了实验(以下数据为多次平行实验测定结果的平均值):
方案一:将a g铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将 g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.
请回答下列问题:
(1)配平下面的化学方程式(将有关的化学计量数填入答题卡的横线上):
______KMnO4+______FeSO4+______H2SO4=______Fe2(SO4)3+______MnSO4+______K2SO4+______H2O
(2)在滴定实验中不能选择______式滴定管,理由是______;
(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为______和______;(铁的相对原子质量以55.9计)
(4)高锰酸钾是化学中常用强氧化剂.在实验室中可用下式配制少量高锰酸钾溶液:
______Mn2++______NaBiO3+______H+=______MnO4-+______Bi3++______Na++______H2O
1)、配平系数
2)、根据以上信息,下列各组离子在溶液中不能大量共存的是______
A.Na+、K+、H+、Cl-、NO3-、MnO4- B.Na+、K+、H+、SO42-、BiO3-、Cl-
C.Na+、Al3+、H+、NO3-、SO42-、MnO4- D.Na+、K+、Mn2+、NO3-、SO42-、Cl-.
查看习题详情和答案>>
方案一:将a g铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将
 g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.请回答下列问题:
(1)配平下面的化学方程式(将有关的化学计量数填入答题卡的横线上):
______KMnO4+______FeSO4+______H2SO4=______Fe2(SO4)3+______MnSO4+______K2SO4+______H2O
(2)在滴定实验中不能选择______式滴定管,理由是______;
(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为______和______;(铁的相对原子质量以55.9计)
(4)高锰酸钾是化学中常用强氧化剂.在实验室中可用下式配制少量高锰酸钾溶液:
______Mn2++______NaBiO3+______H+=______MnO4-+______Bi3++______Na++______H2O
1)、配平系数
2)、根据以上信息,下列各组离子在溶液中不能大量共存的是______
A.Na+、K+、H+、Cl-、NO3-、MnO4- B.Na+、K+、H+、SO42-、BiO3-、Cl-
C.Na+、Al3+、H+、NO3-、SO42-、MnO4- D.Na+、K+、Mn2+、NO3-、SO42-、Cl-.
查看习题详情和答案>>
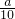 g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.