摘要:AC 2.A 3.A 4.B 5.B 6.C 讲析:2.在酸性条件下.弱酸根离子.氢氧根离子.酸式弱酸根离子不能大量存在.MnO4-离子为紫红色.3.NH4Cl分解生成HCl和NH3.HCl和NH3冷却后又生成NH4Cl.NH4I分解生成NH3和HI.HI不稳定.继续分解生成H2和I2.4.HCl.NH3.SO2完全溶解于水.标准状况下.所得溶液的物质的量浓度为1/22.4mol/L.设NO2体积为1L.则物质的量为1/22.4mol.NO2与水反应生成HNO3和NO.生成HNO3 0.298mol.溶液的体积为2/3L.其浓度为.0446mol/L. 5.氨气和氯气反应生成氯化铵和氮气.其方程式: 8NH3 + 3Cl2 = 6NH4Cl + N2 根据同温同压下.压强比等于物质的量比.
网址:http://m.1010jiajiao.com/timu_id_3731572[举报]
根据元素周期表,填写下列空白:
(1)最活泼的非金属元素位于周期表中第 周期第 族、第 纵行。某元素B含有8个质子、10个中子,用 ![]() 表示B原子的组成 , B的原子结构示意图为 。
表示B原子的组成 , B的原子结构示意图为 。
(2)在第三周期中,A、C两元素的原子序数之差为4,它们组成化合物AC的化学式为_____
(3)1mol某物质含有不同周期的三种元素各1mol,其核电荷总数为20mol,该物质的化学式为 ;它是 化合物(离子或共价)。
查看习题详情和答案>>
下图中A是一种无色液体,G是极易溶于水的碱性气体,Y是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应⑤是工业制X的主要反应之一.
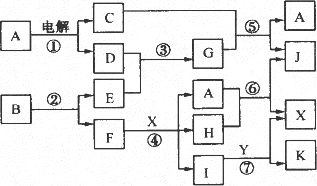
试填空:
(1)写出下列物质的化学式A________E________F________Y________.
(2)反应⑤的化学方程式为________.
(3)1 mol B通过②得到1 mol F,B中F的质量分数为72%,则B的化学式为________.
(4)写出下列反应的化学方程式________.
①A![]() C+D; ②C+G→A+J;
C+D; ②C+G→A+J;
③F+X→A+H+I; ④B→E+F;
⑤D+E→G; ⑥A+H→J+X;
⑦Y+I→X+K
几种短周期元素的原子半径及某些化合价见下表.分析判断下列说法正确的是( )
|
查看习题详情和答案>>
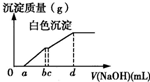 向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图所示,则原混合溶液中MgCl2与FeCl3的物质的量之比为( )
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图所示,则原混合溶液中MgCl2与FeCl3的物质的量之比为( )